
- •Глава 2. Молекулы
- •Механическая модель физической молекулы
- •Подходы к построению волновой функции
- •Вопросы для самоконтроля
- •2.1. Метод вс
- •2.1.1. Построение базисного набора
- •2.1.2. Описание молекулы водорода методом вс
- •Симметрия волновой функции
- •Энергетические характеристики молекулы водорода
- •Влияние межъядерного расстояния
- •2.1.3. Общая формулировка метода вс
- •2.1.4. Теория резонанса
- •Вопросы для самоконтроля
- •2.2. Метод мо
- •2.2.1. Молекулярные орбитали
- •Вопросы для самоконтроля
- •2.2.2. Описание молекулы водорода методом мо
- •Вычисление энергии в методе мо
- •Орбитальные энергии
- •Конфигурационное взаимодействие
- •2.2.3. Общая формулировка метода мо
- •Канонические мо
- •Локальные характеристики молекулы в методе кмо
- •Электронная плотность атомов
- •Порядок химической связи
- •Индекс свободной валентности
- •Молекулярные диаграммы
- •Поляризуемости
- •Вопросы для самоконтроля
- •2.2.4. Метод мо Хюккеля
- •Молекула этилена
- •Молекула циклобутадиена
- •Общие решения в методе Хюккеля
- •Молекулы с гетероатомами в методе мох
- •Система параметров Стрейтвизера
- •Вопросы для самоконтроля
- •2.2.5. Метод лмо
- •Гибридизация ао
- •Эффекты сопряжения
- •Индуктивные эффекты
- •Вопросы для самоконтроля
- •2.3. Ядерный остов молекул
- •Вопросы для самоконтроля
- •2.4. Спиновые состояния ядерного остова
- •Вопросы для самоконтроля
- •Рекомендуемая литература Основная
- •Дополнительная
- •Типовые задачи
2.1.4. Теория резонанса
Вследствие больших вычислительных проблем метод ВС редко применяется в полном виде. Чаще можно встретить различные упрощенные варианты, примером которых может служить полуколичественная "теория резонанса", широко используемая в органической химии. В основе этой теории лежит основополагающая идея метода ВС о том, что волновая функция молекулы может быть получена в виде суперпозиции базисных волновых функций резонансных форм:
молекулы=С11+С22+ ... +Сnn
Однако, в отличие от полного метода ВС, в теории резонанса учитывают не все базисные функции (резонансные формы), а только их небольшое число. Иначе говоря, дело сводится к "урезанию" базисного набора, что чрезвычайно упрощает математические проблемы метода ВС.
Например, для молекулы воды можно представить более 60 миллионов РФ, отличающихся способом распределения 10 электронов по трем одноядерным сегментам разрезанной молекулы. Из них можно оставить только две группы аналогичных РФ:

Если суперпозицию волновых функций РФ распространить на сами РФ, то получится нечто среднее — т.н. "резонансный гибрид" или "мезомерная (т.е. промежуточная, усредненная) структура", в которой:
а) на атомах водорода будет наблюдаться избыточный положительный заряд (пропорциональный квадрату коэффициента С2);
б) на атоме кислорода будет наблюдаться избыточный отрицательный заряд (пропорциональный удвоенному квадрату коэффициента С2);
в) порядки ковалентных связей О—Н будут иметь величину между 1 и 0 (пропорционально квадрату коэффициента С1).
Для пояснения основной идеи теории резонанса можно привести механическую аналогию, которую в свое время привлекали для анализа данной проблемы. Механический осциллятор (например, маятник) всегда колеблется между двумя крайними положениями. В результате действия сил трения, осциллятор со временем переходит в равновесное (неподвижное) состояние, всегда расположенное между крайними состояниями максимального отклонения. Зная, каковы эти крайние состояния, всегда можно предсказать, каким будет состояние равновесия. Если искусственно приготовить молекулу в состоянии, точно соответствующем одной из резонансных форм, то это состояние окажется неустойчивым. Электронные облака такой искусственной молекулы придут в колебательное движение, которое очень быстро закончится их переходом в устойчивое равновесное состояние — мезомерную форму. Трение в молекуле возникает из-за того, что колеблющиеся электроны испускают электромагнитные волны, уносящие энергию колебательного движения ("радиационное трение"). Такие колебания происходят с определенной частотой, что и привело к использованию характерного термина "резонанс". Таким образом, каждая резонансная форма описывает молекулу, находящуюся в одном из неустойчивых состояний, время жизни которого очень мало (порядка 10–8с). Поэтому можно быть уверенным, что все подобные молекулы, с которыми приходится иметь дело на практике, уже успели перейти в устойчивое состояние, описываемое мезомерной формой.
Основная проблема метода резонанса — рациональный отбор резонансных форм (резонансных структур). Наиболее полезным в этом отношении является правило, связывающее вклад данной РФ с ее энергией: чем выше энергия РФ, тем меньше ее вклад. Соответственно, в методе резонанса ограничиваются только теми РФ, энергии которых особенно низки. К ним относятся:
а) атомная РФ(состоящая из нейтральных атомов) в которой электроны распределены в соответствии с зарядами ядер,
б) ионные РФ, в которых избыточное число электронов принадлежит наиболее электроотрицательным атомам; при этом, как правило, рассматриваются только РФ с единичными зарядами атомов.
Дополнительно можно отметить, что часто в теории резонанса используют не полные, а частичные резонансные формы, в которых атомной локализации подвергаются не все электроны молекулы, а только некоторые из них, обладающие особенно высокой энергией. Частичная резонансная форма отличается тем, что ее можно однозначно изобразить классической структурной формулой или формулой Льюиса.
Например, молекулу диоксида углерода можно рассматривать как резонансный гибрид ковалентной и ионной форм, отличающихся локализацией подвижных электронных пар двойных связей (-электроны):
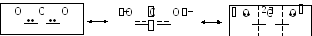
Аналогично, молекула монооксида углерода представляется в виде резонансного гибрида структур, отличающихся состояниями неподеленной пары электронов кислорода и вакантной АО атома углерода:

При описании молекулы бензола можно вообще не учитывать ионные резонансные структуры, имеющие в данном случае гораздо более высокие энергии, чем ковалентные, так как в молекуле нет атомов с высокой электроотрицательностью:

Таким образом, теория резонанса позволяет использовать основные идеи метода ВС и получать без особых математических затруднений качественные или даже полуколичественные результаты, которые достаточны для решения многих чисто химических задач, требующих привлечения сведений об электронном строении молекул.
