
- •Глава 2. Молекулы
- •Механическая модель физической молекулы
- •Подходы к построению волновой функции
- •Вопросы для самоконтроля
- •2.1. Метод вс
- •2.1.1. Построение базисного набора
- •2.1.2. Описание молекулы водорода методом вс
- •Симметрия волновой функции
- •Энергетические характеристики молекулы водорода
- •Влияние межъядерного расстояния
- •2.1.3. Общая формулировка метода вс
- •2.1.4. Теория резонанса
- •Вопросы для самоконтроля
- •2.2. Метод мо
- •2.2.1. Молекулярные орбитали
- •Вопросы для самоконтроля
- •2.2.2. Описание молекулы водорода методом мо
- •Вычисление энергии в методе мо
- •Орбитальные энергии
- •Конфигурационное взаимодействие
- •2.2.3. Общая формулировка метода мо
- •Канонические мо
- •Локальные характеристики молекулы в методе кмо
- •Электронная плотность атомов
- •Порядок химической связи
- •Индекс свободной валентности
- •Молекулярные диаграммы
- •Поляризуемости
- •Вопросы для самоконтроля
- •2.2.4. Метод мо Хюккеля
- •Молекула этилена
- •Молекула циклобутадиена
- •Общие решения в методе Хюккеля
- •Молекулы с гетероатомами в методе мох
- •Система параметров Стрейтвизера
- •Вопросы для самоконтроля
- •2.2.5. Метод лмо
- •Гибридизация ао
- •Эффекты сопряжения
- •Индуктивные эффекты
- •Вопросы для самоконтроля
- •2.3. Ядерный остов молекул
- •Вопросы для самоконтроля
- •2.4. Спиновые состояния ядерного остова
- •Вопросы для самоконтроля
- •Рекомендуемая литература Основная
- •Дополнительная
- •Типовые задачи
2.1.2. Описание молекулы водорода методом вс
Для иллюстрации описанных выше общих принципов метода ВС рассмотрим конкретный объект — молекулу водорода. Ввиду того, что эта молекула содержит всего два ядра, прибор будет устроен чрезвычайно просто — он содержит всего одну перегородку, разделяющую молекулу на две одноядерных подсистемы ("атома"):

Первый этап описания заключается в перечислении всех возможных исходов такого разрезания молекулы в отношении способа распределения электронов по двум отсекам. При этом нужно учесть не только сам факт попадания электрона в конкретный "атом", но и его состояние — характер пространственного и спинового движения, выражающийся двумя сомножителями волновой функции (АСО). Можно также полагать, что в результате процедуры разрезания образующиеся атомы водорода могут получаться не только в основном (1s), но и в одном из возбужденных состояний (2s, 2pи т.д.), причем каждая такая АО может иметь в качестве спинового множителя либо-, либо-функцию. В идеале все возможные варианты должны быть учтены. Ясно, однако, что этот идеал недостижим, так как число возможных вариантов бесконечно велико. На практике приходится использовать ограниченный базис, включающий только такие исходы, вероятность которых достаточно велика. Правило, согласно которому осуществляется отбор, сводится к следующему:вероятность реализации некоторой резонансной формы тем больше, чем меньше ее энергия.
Поэтому в первом приближении можно полагать, что атомы, составляющие резонансные формы, могут находиться только в основном электронном состоянии 1s. Тогда для каждого электрона возможны всего два состояния, описываемые двумя АСО: (1s) и (1s). При этом пространственная часть АСО будет центрирована либо на ядре Ha, либо на ядре Hb. Для упрощения записи обозначим эти пространственные части буквамиАиВсоответственно. Теперь легко перечислить все допустимые исходы разрезания молекулы водорода на два "атома" — резонансные формы. Для удобства разобьем их на группы.
1. Синглетные РФ ковалентного типа (суммарный спин S= 0)

2. Триплетные РФ ковалентного типа (суммарный спин S= 1)

3. Синглетные РФ ионного типа
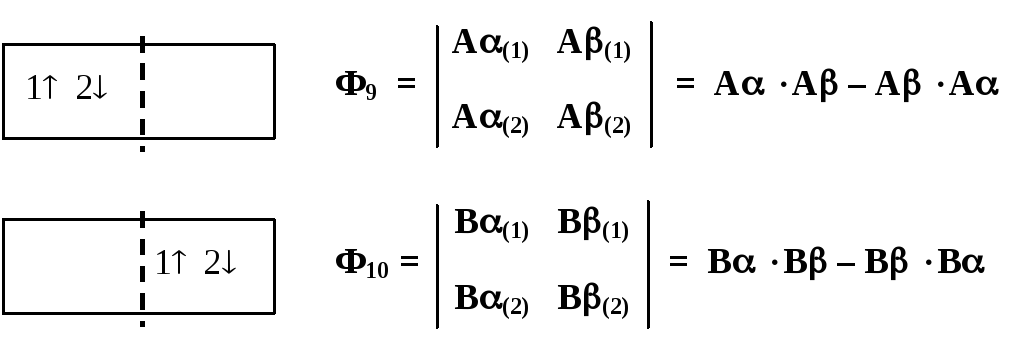
В первых восьми вариантах молекула водорода разрезана на два электрически нейтральных фрагмента — атома: Н2= Н—Н (поэтому такие формы и называютсяковалентными). Волновые функции РФ построены в виде произведения двух АСО, причем на первой позиции всегда стоит АСО, относящаяся к электрону № 1, а на второй — к электрону № 2. Если номера электронов указывать в явном виде, то порядок следования сомножителей в функции-произведении оказывается не существенным.
Ф1 = АВ = А(1)(1)В(2)(2) = В(2)(2)А(1)(1)
В двух последних вариантах РФ молекула водорода разрезана на два электрически заряженных фрагмента — иона: Н2= Н+Н–(поэтому такие формы и называютсяионными). Для ионных РФ волновые функции построены в виде определителя Слэтера, поскольку каждая из них фактически представляет собой двухэлектронный "атом" — гидрид-анион Н–.
Теперь волновую функцию молекулы можно записать в виде комбинации десяти базисных волновых функций, описывающих найденные РФ:
Ф = С1 Ф1 + С2 Ф2 + ... + С10 Ф10
Нерешенной остается вторая часть проблемы: определение величин десяти коэффициентов С1,С2, …,С10 . Эту задачу можно решить разными способами, например, вариационным (ЕEmin). Однако, в большинстве случаев, задачу можно значительно упростить, если обратиться к анализу общих свойств волновых функций. Особенно полезным является анализ симметрии.
