
- •Нарушения кислотно-основного состояния
- •1. Что понимают под кислотно-основным состоянием (кос)?
- •2. Какими основными показателями характеризуется кос в организме.
- •3. Какие буферные системы существуют в организме? Какова их роль в стабилизации кос?
- •4. Какую роль выполняют легкие, почки и печень в компенсации нарушений кос?
- •6. Какие виды ацидоза существуют? 11. Какие виды алкалоза существуют ?
- •7. Какие причины и последствия газового (дыхательного) ацидоза? 8. Каким образом компенсируются нарушения в организме при газовом ацидозе? Газовый ацидоз
- •9. Каковы причины и последствия негазового (метаболического) ацидоза? 10. Каков механизм компенсации метаболического ацидоза? Негазовый ацидоз
- •12. Каковы причины и последствия газового алкалоза? 13. Какие системы организма участвуют в компенсации изменений при газовом алкалозе? Газовый алкалоз
- •14. Каковы причины и последствия негазового алкалоза? 15. Каков механизм компенсации негазового алкалоза? Негазовый алкалоз
- •16. При каких состояниях могут возникать сочетания нарушения кос? Сочетанные нарушения кислотно-основного состояния
- •2. Каковы причины и последствия нарушения синтеза белка?3. Каковы причины и последствия дефицита незаменимых аминокислот? 4. При каких условиях нарушается синтез незаменимых аминокислот?
- •5. Каковы последствия нарушения синтеза отдельных белков?
- •6. Каковы причины, механизм и последствия усиления распада белков?
- •7. Что понимается под отрицательным и положительным азотистым балансом?
- •8. Каковы причины и последствия нарушения процессов дезаминирования, переаминирования, декарбоксилирования аминокислот?
- •9. Как осуществляется конечный этап обмена белков и аминокислот?
- •10. Каковы причины и последствия нарушения синтеза мочевины?
- •14. Как изменяются обменные процессы в разные периоды голодания?
- •15. Чем характеризуется белково-калорийная недостаточность?
- •3. Каковы причины и последствия нарушения переваривания и всасывания липидов?
- •4. Что такое «липопротеины»? На какие группы они делятся?
- •18. Какую роль в развитии атеросклероза играет нарушение обмена липопротеинов? Какие существуют теории развития атеросклероза?
- •Основные гипо- и гипервитаминозы
- •Причины, патогенез и основные проявления недостатка и избытка калия в организме
- •Причины, патогенез и основные проявления недостатка и избытка кальция в организме
- •Причины, патогенез и основные проявления недостатка и избытка фосфатов в организме
- •Причины, патогенез и основные проявления недостатка и избытка магния в организме
- •Распространенные гипомикроэлементозы
- •Распространенные гипермикроэлементозы
- •3. Чем может определяться нейрогуморальная дизрегуляция водно-электролитного обмена?
- •4. Каковы потери и потребность в воде человека в норме и при патологии?
- •5. Что такое «обезвоживание»? Какие виды обезвоживания существуют?
- •6. Каковы причины ограничения поступления воды в организм?
- •7. Каковы причины избыточной потери воды?
- •9. Какое влияние на организм оказывает обезвоживание?
- •10. Какие причины и виды задержки воды в организме выделяют?
- •11. Что такое «отек» и «водянка»?
- •12. Каким образом классифицируют отеки по этиологии и патогенезу?
- •13. Каковы общие механизмы развития отеков?
- •14. Какова роль изменения гидростатического давления в развитии отеков?
- •15. В чем заключается роль изменения онкотического давления в развитии отеков?
- •16. Какую роль в патогенезе отеков играет повышение проницаемости сосудистой стенки?
- •17. Какова роль лимфатического фактора в развитии отеков?
- •18. Какова роль активной задержки воды и натрия в организме в развитии отеков?
- •19. Каков механизм развития сердечных отеков?
- •20. Каков механизм развития почечных нефротических отеков?
- •21. Каков механизм развития почечных нефритических отеков?
- •22. Каков механизм развития асцита и отека при циррозе печени?
- •23. Каков механизм развития мембраногенных отеков
- •24. Каково значение отека для организма?
- •25. В чем заключаются основные принципы терапии нарушений водно-электролитного обмена?
- •Патофизиология энергетического (основного) и углеводного обменов
- •1. Каковы причины нарушения основного обмена? 2. Какова роль внутренних и внешних факторов в изменении основного обмена?
- •Патофизиология энергетического и основного обмена Нарушения обмена энергии
- •Нарушения основного обмена
- •3. Что такое “метод прямой калориметрии” и “метод непрямой калориметрии”?
- •Патофизиология углеводного обмена
- •4. Каковы причины нарушения расщепления и всасывания углеводов пищи? 5. Какие существуют механизмы нарушения расщепления и всасывания углеводов пищи?
- •Нарушение углеводного обмена на этапе переваривания (расщепления) и всасывания
- •6. Какие выделяют причины и механизмы нарушения синтеза и распада гликогена? Нарушение углеводного обмена на этапе депонирования гликогена
- •7. Что такое “гликогенозы”?
- •8. Каковы причины, механизмы и последствия промежуточного обмена углеводов? Нарушения промежуточного обмена углеводов
- •Нарушение выделения глюкозы почками
- •12. Что такое “гипогликемия”, “гипергликемия”? Каковы их причины, виды и проявления? 13. В чем заключается механизм развития гипогликемии? Нарушения углеводного обмена
- •Диагностика нарушений углеводного обмена
- •19. В чем заключается механизм нарушений основного и углеводного обмена при сд 1 типа?
- •20. В чем заключается механизм нарушений основного и углеводного обмена при сд 2 типа? 21. Что такое “инсулинорезистентность”? в чем заключается ее роль в развитии сд 2 типа?
- •23. Что относят к метаболическим осложнениям сахарного диабета? 24. Какие ранние и поздние осложнения сахарного диабета выделяют? Метаболические осложнения сахарного диабета
- •25. Что такое «диабетическая (гипергликемическая) кома»? Каковы ее виды? 26. В чем заключается механизм развития гипогликемической комы?
- •27. В чем заключается механизм развития макро- и микроангиопатий? Каковы их последствия?
- •28. Что такое «диабетическая нейропатия»? Каковы механизм ее развития и последствия?
8. Каковы причины, механизмы и последствия промежуточного обмена углеводов? Нарушения промежуточного обмена углеводов
Промежуточный обмен углеводов — осуществляется на уровне клетки и включает в себя все превращения с момента их поступления в клетку до образования конечных продуктов.
• В нормальных условиях глюкоза в клетке может использоваться для синтеза гликогена, окисляться до пирувата и лактата или до СО, (в цикле Кребса и в меньшей степени в пентозофосфатном цикле), а также превращаться в жирные кислоты.
• В тканях, где нет или очень мало митохондрий (эритроциты, белые мышечные волокна, кл. сетчатки глаза, мозг. слоя надпочечников), основной путь обмена глюкозы – гликолиз, в р-те которого образуется лактат.
• Когда поступление углеводов в составе пищи уменьшается, содержание глюкозы в крови поддерживается за счет гликогенолиза в печени, где запасы гликогена невелики и они истощаются уже к 6-10 ч голодания. При продолжении голодания до 24 ч включается глюконеогенез в печени, энтероцитах и корковом веществе почек, обеспечивающий синтез 80-100 г глюкозы в сутки.
Причины, механизмы и последствия нарушения промежуточного обмена углеводов:
1. Гипоксия — возникает при снижении рО2 во вдыхаемом воздухе, недостаточности дыхания и кровообращения, анемиях, интоксикациях, инфекциях, переключает клеточный метаболизм с преимущественного аэробного окисления субстратов на анаэробный.
• При распаде глюкозы в процессе гликолиза образуется избыток лактата, что приводит к лактоацидозу.
2. Нарушения функции печени. Возникновению лактоацидоза способствует нарушение глюконеогенеза в гепатоцитах, где часть молочной кислоты в норме ресинтезируется в глюкозу и гликоген.
• При острых и хронических гепатитах, циррозах, отравлениях гепатотропными ядами этот процесс нарушается, молочная кислота выходит в кровь, развивается лактоацидоз.
3. Гиповитаминоз В1. При недостаточности витамина В1 возникает дефицит тиаминдифосфата ⇒ подавление синтеза ацетил-КоА из пировиноградной кислоты, которая накапливается и частично переходит в молочную кислоту, содержание которой в связи с этим возрастает, и возникает лактоацидоз. Торможение окисления ПВК снижает синтез ацетилхолина и нарушает передачу нервных импульсов.
• При возрастании концентрации ПВК в 2-3 раза по сравнению с нормой возникают нарушения чувствительности, невриты, параличи.
4. Наследственные дефекты ферментов: дефект ферментов глюконеогенеза; недостаточность глюкозо-6-фосфатазы при гликогенозе 1 типа (болезнь Гирке) ⇒ выраженный лактоацидоз.
5. Ятрогенные факторы. Применение ряда ЛС (бигуанидов (блокаторы глюконеогенеза)), при лечении СД может привести к коме с лактоацидозом.
Нарушение выделения глюкозы почками
Нарушения выделения глюкозы почками связаны с уменьшением фильтрации глюкозы в клубочках или снижением ее реабсорбции в проксимальных канальцах нефрона.
• В клубочках почек глюкоза фильтруется, затем в эпителии проксимальных канальцев реабсорбируется путем вторично-активного транспорта с затратой энергии АТФ по градиенту концентрации Na+.
• При увеличении конц. глюкозы в сыворотке крови более 8,8-9,9 ммоль/л она начинает выделяться с мочой.
• Почечный порог – показатель гликемий, при котором появляется глюкозурия.
• На выделение глюкозы с мочой влияет скорость клубочковой фильтрации, которая в норме =ок. 130 мл/мин.
• При снижении фильтрации глюкоза не определяется в моче даже при гликемии, превышающей почечный порог, т.к. фильтруется меньше глюкозы и вся она успевает реабсорбироваться в прокс. канальцах почек.
• В случае патологии канальцев (тубулопатии) при нарушении реабсорбции глюкоза может определяться в моче даже в условиях нормо- или гипогликемии (почечный диабет).
9. Каков главный критерий, характеризующий уровень углеводного обмена? 10. Какие гормоны повышают уровень глюкозы в крови? 11. Какие гормоны снижают уровень глюкозы в крови?
Нарушение регуляции углеводного обмена
Концентрация глюкозы в крови — жесткая гомеостатическая константа и критерий адекватности углеводного обмена. Нормальный уровень гликемии поддерживается работой ЦНС, кишечника, печени, почек, поджелудочной железы, надпочечников, жировой ткани и других органов.
Регуляция углеводного обмена:
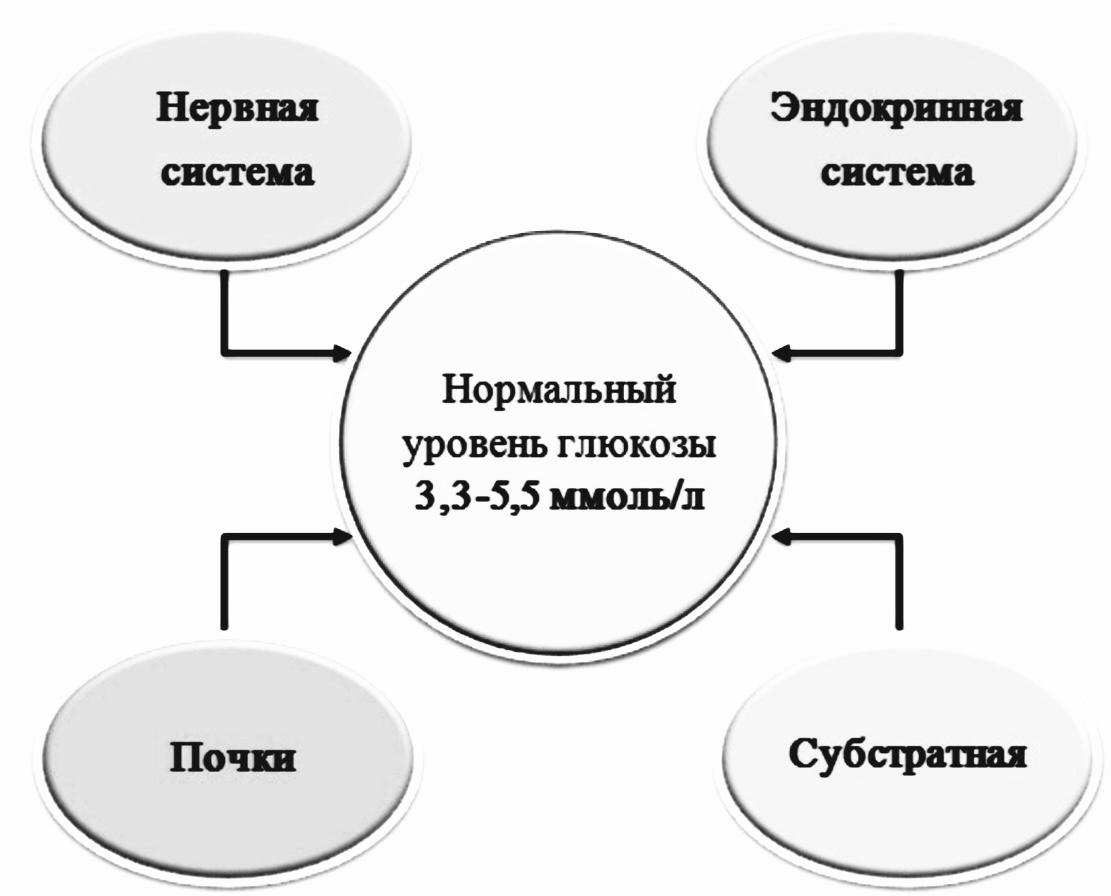
Субстратная регуляция.
• Уровень гликемии – основной фактор, определяющий метаболизм глюкозы.
• Пограничная концентрация глюкозы — продукция в печени = потреблению периф.тк. = 5,5-5,8 ммоль/л.
Если ↓ – печень поставляет глюкозу в кровь; если ↑ – доминирует синтез гликогена в печени и мышцах.
Нервная регуляция.
• Симпатическая импульсация ⇒ освобождение адреналина из надпочечников, который стимулирует гликогенолиз ⇒ гипергликемия.
• Раздражение парасимпатических нервных волокон ⇒ усиление выделения инсулина поджелудочной железой, поступление глюкозы в клетку и гипогликемический эффект.
Почечная регуляция. Норм. работа почек поддерживает ур. глюкозы с помощью фильтрации и реабсорбции.
Гормональная регуляция.
• На ур. глюкозы в крови влияет много гормонов, НО только инсулин вызывает гипогликемический эффект.
• Контринсулярным действием с повышением уровня глюкозы крови обладают следующие гормоны: глюкагон, адреналин, глюкокортикоиды, АКТГ, СТГ, ТТГ, тиреоидные.
• При низкой концентрации инсулина, в частности при голодании, усиливаются гипергликемические эффекты других гормонов, таких как глюкагон, адреналин, глюкокортикоиды и СТГ.
Гормоны, контролирующие гомеостаз глюкозы
Гормон |
Место образования |
Механизм действия и ткани-мишени |
Инсулин |
Бета-клетки островков Лангерганса поджелудочной железы |
Увеличивает: - потребление глюкозы клетками (мышцы, жировая ткань) - синтез гликогена и белков (печень, мышцы) - липогенез (печень, жировая ткань) Снижает: - липолиз (жировая ткань) - глюконеогенез и кетогенез (печень) - протеолиз (мышцы) |
Глюкагон |
Альфа-клетки островков Лангерганса поджелудочной железы |
Увеличивает: - гликогенолиз, глюконеогенез и кетогенез (печень) - липолиз (жировая ткань) |
Адреналин |
Мозговое в-во надпочечников |
Увеличивает: - гликогенолиз (печень, мышцы) - липолиз (жировая ткань) |
СТГ |
Эозинофильные клетки аденогипофиза |
Увеличивает: - гликогенолиз (печень) - липолиз (жировая ткань) |
АКТГ |
Базофильные клетки аденогипофиза |
Стимулирует освобождение глюкокортикоидов (надпочечники) Увеличивает липолиз (жировая ткань) |
Глюкокортикоиды |
Пучковая зона коркового вещества надпочечников |
Увеличивает: - глюконеогенез и синтез гликогена (печень) - протеолиз (мышцы) Снижает: потребление глюкозы клетками (мышцы, жир. тк.) |
Гормоны ЩЖ |
Тироциты |
Увеличивает: утилизацию глюкозы клетками, липолиз и протеолиз (опосредованно через усиление основного обмена) – все ткани. Активирует: инсулиназу (печень) |
Инсулин – видоспецифичный гормон. Представляет собой полипептид, состоящий из двух аминокислотных цепей (А- и В-цепи), соединенных между собой двумя дисульфидными мостиками.
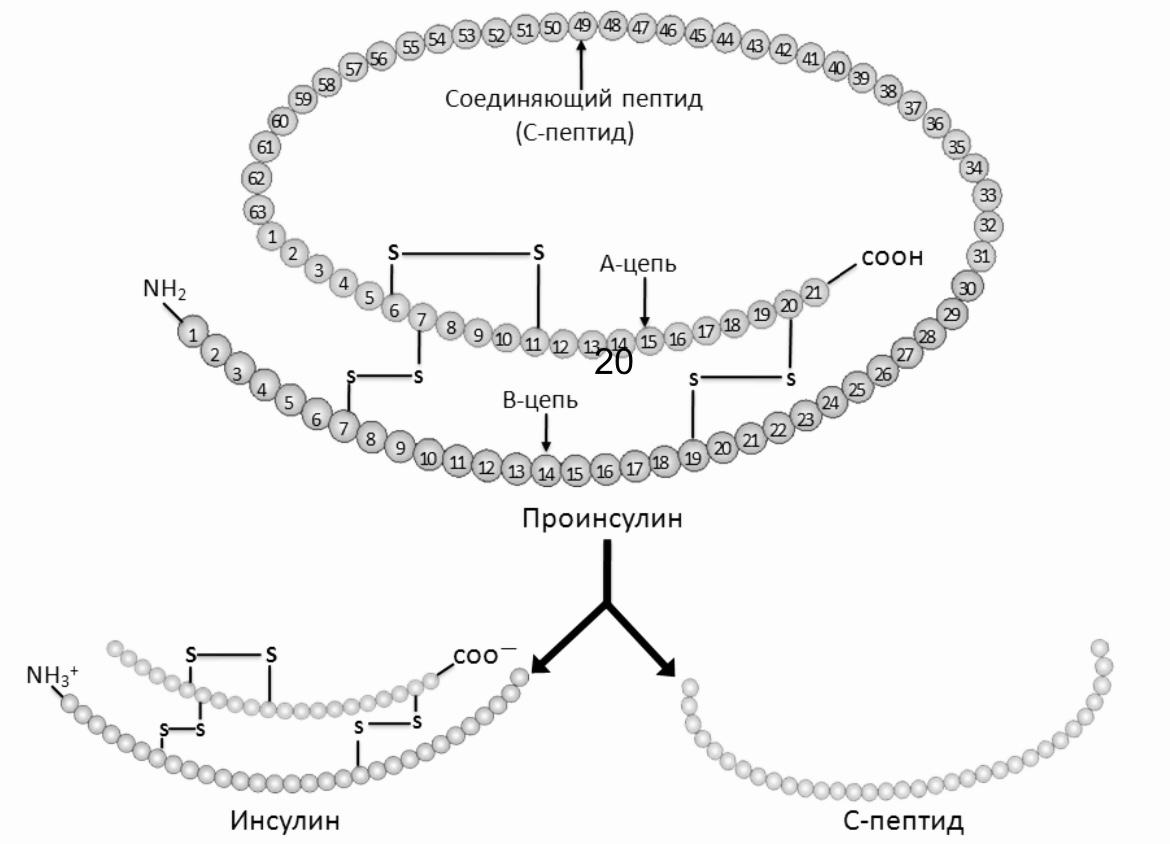
Нарушения секреции инсулина могут являться результатом:
• недостаточного питания плода ⇒ нарушение внутриутробного развития поджелудочной железы;
• недостаточного питания в постнатальном периоде;
• глюкозотоксичности (при хронической гипергликемии);
• генетических дефектов в механизмах секреции инсулина (мутации генов инсулина, глюкокиназы, GLUT 2).
Нарушения секреции инсулина могут выражаться:
• снижением в ответ на глюкозу и другие стимуляторы (аргинин, лейцин);
• нарушением пульсирующей секреции инсулина и превращения проинсулина в инсулин, что приводит к повышению содержания проинсулина в крови.
Инсулин – главный анаболический гормон, обладающий широким спектром действия на транспорт и обмен углеводов, аминокислот, ионов, липидов, а также на процесс в репликации и транскрипции, клеточной дифференцировки, пролиферации и трансформации.
• Высокие концентрации инсулина в крови – анаболическое действие на обмен веществ,
• Низкие – катаболическое действие на обмен веществ.
Метаболические эффекты инсулина:
1) гипогликемический:
• увеличение проницаемости мембран клеток мышц и жировой ткани для глюкозы;
• активация фермента гексокиназы, фосфорилирующего глюкозу во всех тканях организма;
• усиление синтеза гликогена в печени (инсулин активирует гликогенсинтазу);
• ускорение использования продуктов превращения глюкозы в ЦТК и пентозофосфатном пути;
2) анаболический:
• увеличение прониц. мембран клеток инсулинозависимых тканей для АК, К+,Na+; кетоновых тел в мышцах;
• усиление липогенеза (инсулин активирует синтез ТАГ из углеводов, повышает активность липопротеиновой липазы адипоцитов);
• активация синтеза белков и подавление их распада;
3) антикатаболический:
• снижение распада гликогена (инсулин подавляет активность гликогенфосфорилазы);
• уменьшение интенсивности глюконеогенеза, посредством снижения активности ферментов;
4) митогенный – инсулин стимулирует пролиферацию клеток, связываясь с рецепторами инсулиноподобных факторов.
Инсулин полипептидная молекула ⇒ не способна проникать через клеточную мембрану, поэтому все эффекты инсулина осуществляются через специальные рецепторы на ее поверхности.
• Инсулиновый рецептор относится к рецепторам с тирозинкиназной активностью, обеспечивающим фосфорилирование специфических внутриклеточных белков – IRS.
Глюкагон – одноцепочечный полипептид, состоящий из 29 аминокислотных остатков, его эффекты противоположны эффектам инсулина.
• Основные клетки-мишени для глюкагона – печень и жировая ткань.
• Связываясь с рецепторами клеток-мишеней, ускоряет мобилизацию гликогена в печени и мобилизацию липидов в жировой ткани, активируя через аденилатциклазный каскад гормончувствительную ТАГ-липазу.
• В бета-клетках поджелудочной железы глюкагон стимулирует секрецию инсулина из гранул в условиях высокой гликемии в течение абсорбтивного периода.
