
- •Химия учебное пособие
- •Оглавление
- •Введение
- •Тема 1. Систематика химических законов.
- •1.1 Основные стехиометрические законы и расчеты по уравнениям реакций Содержание материала для самостоятельного изучения
- •Основные теоретические положения
- •Решение типовых задач
- •112 Г железа выделяет 67,2 л водорода 5,6 .103 г железа выделяет vх л водорода
- •Задачи для самостоятельного решения
- •1.2 Основные классы неорганических соединений
- •Основные теоретические положения
- •Характер взаимодействия и генетическая связь между основными классами неорганических соединений представлены на рисунке.
- •Решение типовых задач
- •Тема 2. Строение вещества
- •2.1. Строение атома. Периодическая система элементов д.И.Менделеева Содержание материала для самостоятельного изучения
- •Литература: [1 – гл.1, §§ 1.1…1.4]; [2 – гл.1, §§ 1.1….1.4]; [3 – гл.Іі, §§ 17…19; гл.III, §§ 25…34]. Решение типовых задач
- •Задачи для самостоятельного решения
- •2.2. Химическая связь и строение простых молекул
- •Основные теоретические положения
- •Решение типовых задач
- •2.3. Окислительно-восстановительные реакции
- •Задачи для самостоятельного решения
- •Тема 3. Общие закономерности химических процессов
- •3.1 Энергетика химических процессов. Химическое сродство
- •Литература: [1 – гл.5, §§ 5.1…5.4]; [2 – гл.І,іі §§ 1.1…1.4, 2.1…2.3]; [3 – гл.Vі, §§ 55,56,66…68].
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •3.2. Химическая кинетика и равновесие
- •Литература: [1 – гл.V, §§ 5.5, 7.1-7.3]; [2 – гл.VI, §§ 6.1-6.6];
- •Основные теоретические положения
- •Решение типовых задач
- •Согласно уравнению Вант–Гоффа:
- •Задачи для самостоятельного решения
- •Тема 4. Растворы
- •4.1. Способы выражения концентрации растворов Содержание материала для самостоятельного изучения
- •Литература: [1 – гл.4, § 4.1]; [2 – гл.7, §§7.1, 7.2]; [3 – гл.VII§§ 73…77]. Основные теоретические положения
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •Решение типовых задач
- •Константы диссоциации некоторых слабых электролитов при 25оС
- •Задачи для самостоятельного решения
- •4.3 Водородный показатель рН.
- •Отсюда находим водородный показатель раствора сн3соон:
- •Решение. Соль nh4no3 образована слабым основанием nh4oh и сильной кислотой hno3. При растворении она диссоциирует на ионы:
- •Задачи для самостоятельного решения
- •4.4 Жесткость воды и методы ее устранения Содержание материала для самостоятельного изучения
- •Литература: [1 - гл.12, § 12.3]; [2 - гл.VIII, § 8.6]; [3 - гл.VII, § 69; гл. XIX, §§ 211,212]. Основные теоретические положения
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •Тема 5. Электрохимические системы
- •5.1. Электродные потенциалы и электродвижущие силы Содержание материала для самостоятельного изучения
- •Основные теоретические положения
- •Решение типовых задач
- •Стандартные электродные потенциалы в водных растворах
- •Задачи для самостоятельного решения
- •5.2. Электролиз Содержание материала для самостоятельного изучения
- •Задачи для самостоятельного решения
- •Коррозия и защита металлических конструкций Содержание материала для самостоятельного изучения
- •Тема 6. Специальные разделы химии
- •6.1. Гетерогенные дисперсные системы Содержание материала для самостоятельного изучения
- •Литература: [1 - гл.8, 15, §§ 8.7; 15.3]; [2 – гл.7, § 7.8]; [3-гл.Х, §§ 105…109; 112…114]. Основные теоретические положения
- •Молекулы пав обозначены общепринятым символом:
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •6.2. Основы химии неорганических вяжущих веществ Содержание материала для самостоятельного изучения
- •Основные теоретические положения
- •Задачи для самостоятельного решения
- •6.3. Органические соединения. Полимеры
- •Основные теоретические положения
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •Библиографический список
- •Заключение
- •Варианты контрольных заданий
6.3. Органические соединения. Полимеры
Содержание материала для самостоятельного изучения
Основные положения теории химического строения. Углеводороды и их производные. Строение, свойства и применение в строительной практике.
Полимеры. Методы получения, строение свойства и применение в качестве органических вяжущих веществ.
Литература:[1 – гл. 13, 14, §§ 13,1…14,4]; [2-гл. XI, §§11,1, 11,2];
[3 - гл. XV, §§160…177].
Основные теоретические положения
Основные положения теории химического строения изложены А.М. Бутлеровым. Каждое химическое соединение имеет определенный порядок связи атомов в молекуле, т.е. химическое строение. Свойства вещества определяются его качественным, количественным составом, а также химическим, пространственным и электронным строением.
Предельные углеводороды – алканы (СnH2n+2) содержат только δ–связи, не вступают в реакции присоединения. Для них характерны реакции замещения, окисления, расщепления (крекинг). Механизм реакций радикальный.
Реакции замещения:
h,υ
R-H + Hal2 → R-Hal + Hhal(Hal – F,Cl, Br) – галогенирование
R-H + H2SO4→ R-SO3H + H2O – сульфирование
Реакции расщепления (кренинг):
to
C 4H10
C3H8,
C3H6,
C2H6,
C2H4
4H10
C3H8,
C3H6,
C2H6,
C2H4
Реакции окисления: Алкан → гидроперекись → спирт → альдегид → карбоновая кислота → углекислый газ и вода.
Непредельные углеводороды – алкены (этиленовые углеводороды) и алкины (ацетиленовые углеводороды) имеют двойные и тройные связи. π-Связи менее прочные по сравнению с δ-связями, поэтому непредельные углеводороды проявляют высокую реакционную способность.
Реакции присоединения:
CH2 = CH2 +Cl 2 → CH2Cl – CH2Cl ; СH ≡ CH + HCl → CH2 = CH – Cl
дихлорэтан
Реакции полимеризации алкенов:
nCH2 = CH2 → (– CH2 – CH2 –) n
этилен полиэтилен
Реакции окисления:
CH2 = CH2 → CH2OH ─ CH2OH - этиленгликоль
СH ≡ CH → HOOC ─ COOH - щавелевая кислота.
Ароматические
углеводороды (бензол и его гомологи)
содержат группировку атомов – бензольное
кольцо
![]() .
Молекула бензола – кольцевая сопряженная
система, все связи равноценны, поэтому
бензол и его гомологи, несмотря на
высокую ненасыщенность, довольно
устойчивы. Реакции окисления и
присоединения протекают с трудом. Для
ароматических углеводородов характерны
реакции электрофильного замещения
бензольного кольца.
.
Молекула бензола – кольцевая сопряженная
система, все связи равноценны, поэтому
бензол и его гомологи, несмотря на
высокую ненасыщенность, довольно
устойчивы. Реакции окисления и
присоединения протекают с трудом. Для
ароматических углеводородов характерны
реакции электрофильного замещения
бензольного кольца.
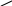 SO3H
SO3H
+ H2SO4→ + H2O
R R
алкилбензолсульфокислота
Производные углеводородов – спирты, фенолы, альдегиды, кислоты –получают при замещении атомов водорода в углеводородах на другие атомы или группы атомов
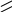 ОН
O
ОН
O
R
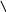 – OH,
,
R
– C
– OH,
,
R
– C
спирты R фенолы H
альдегиды
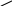
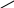 O
O
O
O
R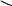
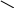 – C
, R
– NH2
, R
– C
– C
, R
– NH2
, R
– C
OH NH2
кислоты амины амиды
Полимеры – высокомолекулярные соединения характеризуются большой молекулярной массой (от нескольких тысяч до миллионов). Молекулы полимеров называют макромолекулами. Они состоят из большого числа повторяющихся звеньев.
Органические полимеры подразделяют на природные и синтетические, карбоцепные и гетероцепные, на линейные, разветвленные и сетчатые.
Существует два основных метода получения полимеров: полимеризация и поликонденсация.
Полимеризацией называется реакция последовательного соединения молекул мономера за счет разрыва двойных связей. При этом не происходит выделения побочных продуктов и изменения элементарного состава мономера.
 nА
(А)n
, (n
– степень
полимеризации)
nА
(А)n
, (n
– степень
полимеризации)
мономер полимер
В зависимости от характера активного центра различают радикальную (активным центром является радикал R∙) и ионную полимеризацию (активные центры анион и катион)
Полимеризация проходит через стадию образования активных центров (радикалов или ионов), роста и обрыва цепи.
Поликонденсацией называется реакция синтеза полимера путем взаимодействия функциональных групп мономеров, сопровождающаяся выделением низкомолекулярных веществ (H2O, HCL, NH3 и др.). Мономеры должны иметь две или более функциональные группы. В случае бифункциональных мономеров при поликонденсации образуются линейные полимеры. Если число функциональных групп более двух, то образуются разветвленные или пространственные полимеры.
nHO–R–OH+nHOOC–R–COOH → H [- O–R–O–OC–R–CO-] n OH .
спирт кислота полиэфир (линейный полимер)
