
- •Химия учебное пособие
- •Оглавление
- •Введение
- •Тема 1. Систематика химических законов.
- •1.1 Основные стехиометрические законы и расчеты по уравнениям реакций Содержание материала для самостоятельного изучения
- •Основные теоретические положения
- •Решение типовых задач
- •112 Г железа выделяет 67,2 л водорода 5,6 .103 г железа выделяет vх л водорода
- •Задачи для самостоятельного решения
- •1.2 Основные классы неорганических соединений
- •Основные теоретические положения
- •Характер взаимодействия и генетическая связь между основными классами неорганических соединений представлены на рисунке.
- •Решение типовых задач
- •Тема 2. Строение вещества
- •2.1. Строение атома. Периодическая система элементов д.И.Менделеева Содержание материала для самостоятельного изучения
- •Литература: [1 – гл.1, §§ 1.1…1.4]; [2 – гл.1, §§ 1.1….1.4]; [3 – гл.Іі, §§ 17…19; гл.III, §§ 25…34]. Решение типовых задач
- •Задачи для самостоятельного решения
- •2.2. Химическая связь и строение простых молекул
- •Основные теоретические положения
- •Решение типовых задач
- •2.3. Окислительно-восстановительные реакции
- •Задачи для самостоятельного решения
- •Тема 3. Общие закономерности химических процессов
- •3.1 Энергетика химических процессов. Химическое сродство
- •Литература: [1 – гл.5, §§ 5.1…5.4]; [2 – гл.І,іі §§ 1.1…1.4, 2.1…2.3]; [3 – гл.Vі, §§ 55,56,66…68].
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •3.2. Химическая кинетика и равновесие
- •Литература: [1 – гл.V, §§ 5.5, 7.1-7.3]; [2 – гл.VI, §§ 6.1-6.6];
- •Основные теоретические положения
- •Решение типовых задач
- •Согласно уравнению Вант–Гоффа:
- •Задачи для самостоятельного решения
- •Тема 4. Растворы
- •4.1. Способы выражения концентрации растворов Содержание материала для самостоятельного изучения
- •Литература: [1 – гл.4, § 4.1]; [2 – гл.7, §§7.1, 7.2]; [3 – гл.VII§§ 73…77]. Основные теоретические положения
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •Решение типовых задач
- •Константы диссоциации некоторых слабых электролитов при 25оС
- •Задачи для самостоятельного решения
- •4.3 Водородный показатель рН.
- •Отсюда находим водородный показатель раствора сн3соон:
- •Решение. Соль nh4no3 образована слабым основанием nh4oh и сильной кислотой hno3. При растворении она диссоциирует на ионы:
- •Задачи для самостоятельного решения
- •4.4 Жесткость воды и методы ее устранения Содержание материала для самостоятельного изучения
- •Литература: [1 - гл.12, § 12.3]; [2 - гл.VIII, § 8.6]; [3 - гл.VII, § 69; гл. XIX, §§ 211,212]. Основные теоретические положения
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •Тема 5. Электрохимические системы
- •5.1. Электродные потенциалы и электродвижущие силы Содержание материала для самостоятельного изучения
- •Основные теоретические положения
- •Решение типовых задач
- •Стандартные электродные потенциалы в водных растворах
- •Задачи для самостоятельного решения
- •5.2. Электролиз Содержание материала для самостоятельного изучения
- •Задачи для самостоятельного решения
- •Коррозия и защита металлических конструкций Содержание материала для самостоятельного изучения
- •Тема 6. Специальные разделы химии
- •6.1. Гетерогенные дисперсные системы Содержание материала для самостоятельного изучения
- •Литература: [1 - гл.8, 15, §§ 8.7; 15.3]; [2 – гл.7, § 7.8]; [3-гл.Х, §§ 105…109; 112…114]. Основные теоретические положения
- •Молекулы пав обозначены общепринятым символом:
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •6.2. Основы химии неорганических вяжущих веществ Содержание материала для самостоятельного изучения
- •Основные теоретические положения
- •Задачи для самостоятельного решения
- •6.3. Органические соединения. Полимеры
- •Основные теоретические положения
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •Библиографический список
- •Заключение
- •Варианты контрольных заданий
Решение типовых задач
Задача 1. Составьте уравнение электролитической диссоциации веществ: H2CO3, Mg(OH)2 и Mg(HCO3)2. Для слабых электролитов напишите выражение констант диссоциации.
Решение. Количественной мерой силы электролита является константа диссоциации и чем она меньше, тем слабее электролит. Угольная кислота и гидроксид магния – слабые электролиты, диссоциируют в две ступени. Каждая ступень диссоциации характеризуется своей константой (см. табл. 4.2.1)
Для Н2СО3:
1. H2CO3
↔ H+
+ HCO3-
,
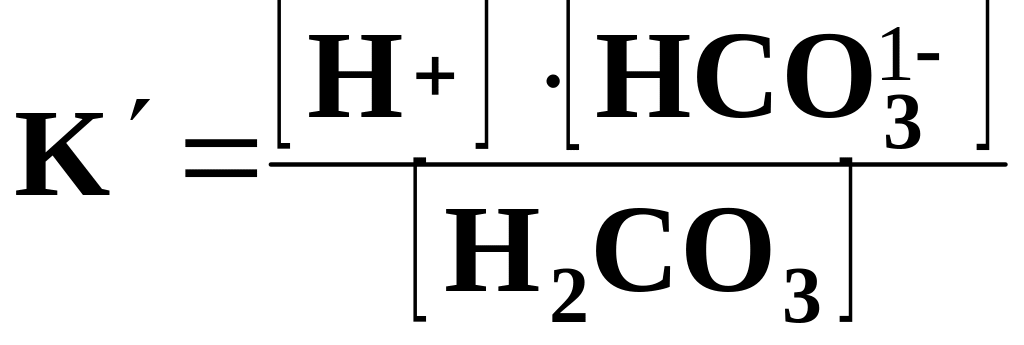 =
4,5 · 10-7
=
4,5 · 10-7
2.
HCO3-
↔ H+ +
CO32-
,
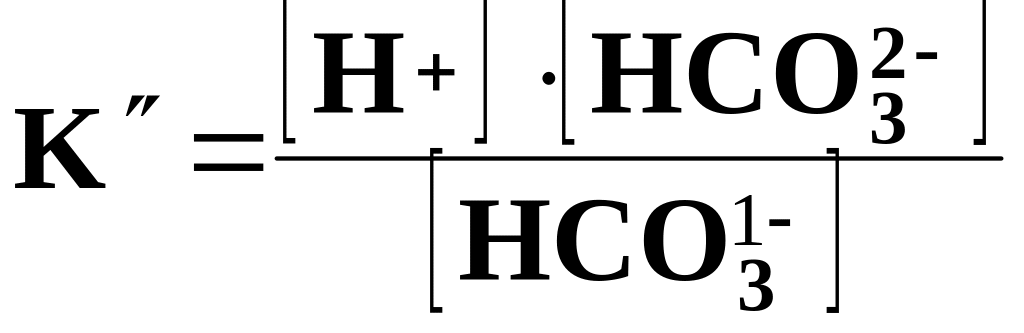 =
4, 7 · 10-11
=
4, 7 · 10-11
Таблица 4.2.1
Константы диссоциации некоторых слабых электролитов при 25оС
Вещество |
Формула |
КI |
КII |
КIII |
|
Вода |
H2O |
1,82 · 10-16 |
- |
- |
|
Кислоты |
|||||
Азотистая |
HNO2 |
5,1 · 10-4 |
- |
- |
|
Борная |
H3BO3 |
5,8 · 10-10 |
1,8 · 10-13 |
1,6 · 10-14 |
|
Кремниевая |
H2SiO3 |
2,2 · 10-10 |
1,6 · 10-12 |
- |
|
плавиковая |
HF |
6,8
· 10-4 |
- |
- |
|
Сернистая |
H2SO3 |
1,7 · 10-2 |
6,2 · 10-8 |
- |
|
Сероводородная |
H2S |
1,0 · 10-7 |
1,0 · 10-14 |
- |
|
Синильная |
HCN |
6,2 · 10-10 |
- |
- |
|
Угольная |
H2CO3 |
4,5 · 10-7 |
4,8 · 10-11 |
- |
|
Уксусная |
CH3COOH |
1,8 · 10-5 |
- |
- |
|
Фосфорная |
H3PO4 |
7,6 · 10-3 |
6,2 · 10-8 |
4,2 · 10-13 |
|
Основания |
|||||
Гидроксид |
|||||
аммония |
NH4OH |
1,79 · 10-5 |
- |
- |
|
алюминия |
Al(OH)3 |
- |
- |
1,38 · 10-9 |
|
железа (II) |
Fe(OH)2 |
- |
1,82 · 10-11 |
- |
|
кальция |
Ca(OH)2 |
- |
4,3 · 10-2 |
- |
|
магния |
Mg(OH)2 |
- |
2,6 · 10-3 |
- |
|
марганца |
Mn(OH)2 |
- |
5,0 · 10-4 |
- |
|
меди (II) |
Cu(OH)2 |
- |
3,4 · 10-7 |
- |
|
никеля |
Ni(OH)2 |
- |
2,5 · 10-5 |
- |
|
свинца (II) |
Pb(OH)2 |
9,6 · 10-4 |
3,0 · 10-8 |
- |
|
хрома (III) |
Cr(OH)3 |
- |
- |
1,02 · 10-10 |
|
цинка |
Zn(OH)2 |
- |
4,0 · 10-5 |
- |
|
Таблица 4.2.2
Растворимость некоторых солей и оснований в воде
(р – растворимое вещество, м – малорастворимое, н – практически нерастворимое; прочерк означает, что вещество не существует или разлагается водой.)
КАТИОНЫ |
А Н И О Н Ы |
||||||||||||
Cl- |
Br- |
I- |
NO3- |
S2- |
SO32- |
SO42- |
CO32- |
SiO32- |
CrO42- |
PO43- |
CH3COO- |
OH- |
|
Li+ |
р |
р |
р |
р |
р |
р |
р |
р |
р |
р |
н |
р |
р |
NH4+ |
р |
р |
р |
р |
- |
р |
р |
р |
- |
р |
р |
р |
- |
Na+,K+ |
р |
р |
р |
р |
р |
р |
р |
р |
р |
р |
р |
р |
р |
Mg2+ |
р |
р |
р |
р |
р |
н |
р |
н |
н |
р |
н |
р |
н |
Ca2+ |
р |
р |
р |
р |
м |
н |
м |
н |
н |
м |
н |
р |
м |
Ba2+ |
р |
р |
р |
р |
р |
н |
н |
н |
н |
н |
н |
р |
р |
Zn2+ |
р |
р |
р |
р |
н |
н |
р |
н |
н |
н |
н |
р |
н |
Cr3+ |
р |
р |
р |
р |
- |
- |
р |
- |
н |
р |
н |
р |
н |
Fe2+ |
р |
р |
р |
р |
н |
н |
р |
н |
н |
- |
н |
р |
н |
Fe3+ |
р |
р |
р |
р |
н |
н |
р |
н |
н |
- |
н |
р |
н |
Cu2+ |
р |
р |
р |
р |
н |
н |
|
н |
н |
н |
н |
р |
н |
Ag+ |
н |
н |
н |
р |
н |
н |
м |
н |
н |
н |
н |
р |
- |
Sn2+ |
р |
р |
р |
- |
н |
- |
р |
- |
- |
- |
н |
р |
н |
Pb2+ |
м |
м |
н |
р |
н |
н |
н |
н |
н |
н |
н |
р |
н |
Bi3+ |
- |
- |
- |
р |
н |
н |
- |
н |
- |
н |
н |
- |
н |
Al3+ |
р |
р |
р |
р |
- |
- |
р |
- |
н |
- |
н |
м |
н |
Mn2+ |
р |
р |
р |
р |
н |
н |
р |
н |
н |
н |
н |
р |
н |
Для Mg(OH)2:
Mg(OH)2 ↔ MgOH+ + OH- ,
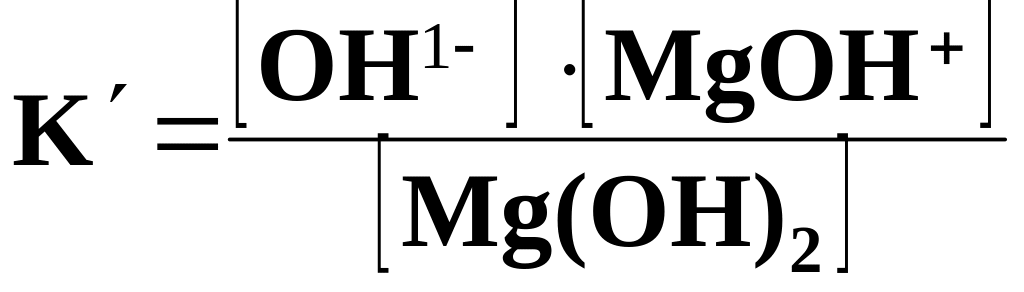 ;
;
2.
MgOH+ ↔ Mg2+
+ OH- , ![]() =
2,5 · 10-3
=
2,5 · 10-3
Соли – сильные электролиты, в воде полностью распадаются на основной и кислотный остаток, константы диссоциации для них не имеют смысла:
Mg(HCO3)2 ↔ Mg2+ + 2 HCO3- .
Задача 2. Степень диссоциации сульфата алюминия в его I M растворе 0,75. Найдите молярную концентрацию ионов алюминия и сульфат-ионов в растворе.
Решение. Степень электролитической диссоциации (α) – отношение числа продиссоциированных молекул сульфата алюминия к общему числу его молекул. В нашем примере:
α = [Al2 (SO4)3]дисc./ [Al2 (SO4)3]общ.;
0,75 = [Al2 (SO4)3]дисc. / 1 ;
следовательно [Al2 (SO4)3]дисс. = 0,75 моль.
Из уравнения диссоциации сульфата алюминия
Al2(SO4)3 ↔ 2 Al3+ + 3 SO42-
видно, что I моль соли распадается на 2 моль ионов Al3+ и 3 моль ионов SO42-. Следовательно, при диссоциации 0,75 моль Al2(SO4)3 образуется 1,5 моль ионов Al3+ и 2,25 моль ионов SO42-.
Задача 3. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между BaCl2 и Na2SO4, Na2CO3 и H2SO4, CH3COONa и HCl, Fe(OH)3 и HNO3.
Решение. В растворах электролитов реакции происходят между ионами и только в том случае, если в результате взаимодействия образуют труднорастворимые (см. табл.4.2.2), газообразные соединения или слабые электролиты. При составлении ионно-молекулярных уравнений эти соединения записывают в молекулярной форме, сильные растворимые электролиты – в виде ионов.
В нашем случае:
BaCl2 + Na2SO4 →BaSO4 + 2 NaCl
Ba2+ + 2 Cl- + 2 Na+ + SO42- →BaSO4↓ + 2 Na+ + 2 Cl-,
Ba2+ + SO42- → BaSO4↓.
Реакция возможна, так как она сопровождается образованием труднорастворимого соединения BaSO4.
Na2CO3 + H2SO4 → Na2SO4 + H2O + CO2↑
2 Na+ + CO32- + 2 H+ + SO42- → 2 Na+ + SO42- + H2O + CO2↑
2 H+ + CO32- → H2O + CO2↑.
Реакция протекает, так как сопровождается образованием газообразного соединения CO2.
CH3COONa + HCl → CH3COOH + NaCl,
CH3COO- + Na+ + H+ + Cl1- → CH3COOH + Na+ + Cl1-,
CH3COO- + H+ → CH3COOH.
В результате этой реакции образуется слабый электролит CH3COOH.
Fe(OH)3 + 3 HNO3 → Fe(NO3)3 + 3 H2O
Fe(OH)3 + 3 H+ + 3 NO3- → Fe3+ + 3 NO3-+ 3 H2O
Fe(OH)3 + 3 H+ → Fe3+ + 3 H2O.
Реакция обратима, так как и среди исходных веществ, и среди продуктов реакции есть слабые электролиты, связывающие ионы ОН1-.
