
- •1. Биохимия - молекулярная логика живых организмов. Состав живой материи
- •1.1. Химическая организация клетки. Основные классы биомолекул, общие принципы их строения
- •1.2. Строение и функции клетки эукариотов и прокариотов. Внутриклеточные органеллы.
- •1.3. Особенности организации биосинтетических процессов в клетках прокариот и эукариот
- •2. Аминокислоты и белки
- •Строение и классификация аминокислот
- •Стереоизомерия.
- •Кислотно-основные свойства аминокислот
- •2.2. Пептиды. Строение пептидов. Особенности пептидной связи.
- •2.3. Белки и их основные признаки. Классификации белков. Биологические функции белков и пептидов (ферменты, гормоны, транспортные белки, структурные белки, иммуноглобулины, рецепторы).
- •Классификация белков
- •Биологические функции белков
- •Пространственное расположение полипептидных цепей (Конформация пептидных цепей в белках)
- •2.6.Четвертичная структура белка. Свойства олигомерных белков. Роль четвертичной структуры в проявлении определенных функций белка.
- •К инетика оксигенирования миоглобина и гемоглобина
- •Транспорт двуокиси углерода
- •Молекулярная основа эффекта Бора
- •Регуляция 2,3-бисфосфоглицератом
- •Изофункциональные белки
- •3.Биологический катализ. Ферменты.
- •Особенности ферментов как биокатализаторов
- •Ферменты
- •Принципы построения рабочего названия фермента
- •Список ферментов
- •Механизм действия ферментов. Активный центр ферментов
- •Механизм действия ферментов (на примере фермента холинэстеразы)
- •Причины высокой каталитической активности.
- •3.2.Субстратная специфичность. Специфичность пути превращения.
- •Специфичность пути превращения
- •6.2. Линеризация уравнения Михаэлиса-Ментен
- •Зависимость скорости ферментативной реакции от температуры
- •Зависимость скорости ферментативной реакции от рН
- •Обратимое конкурентное ингибирование аналогами субстрата
- •Обратимое неконкурентное ингибирование
- •Необратимое ингибирование
- •Регуляция количества фермента путем регуляции скорости его синтеза и распада
- •Превращение ферментов в активные формы
- •Регуляция активности ферментов путем их ковалентной модификации
- •Регуляция белковыми ингибиторами
- •Аллостерическая регуляция
- •Ингибирование по принципу обратной связи
- •4. Строение, состав и физиологическая роль клеточной стенки и цитоплазматической мембраны.
- •Функции мембран
- •Мембранные липиды. Образование липидного бислоя мембран.
- •Мембранные белки. Жидко-мозаичное строение мембран
- •Функции мембранных гликолипидов, гликопротеинов, белков:
- •Свойства биологических мембран
- •Пассивный транспорт
- •Активный транспорт
- •Экзо- и эндоцитоз
- •Системы унипорта, симпорта и антипорта
- •4.3. Строение клеточной стенки грамположительных и грамотрицательных бактерий.
- •5. Пути и механизмы преобразования энергии в живых системах
- •5.1. Метаболизм. Катаболизм и анаболизм
- •Макроэргические соединения
- •Фазы освобождения энергии из питательных веществ
- •Роль высокоэнергетических фосфатов в улавливании энергии. Субстратное и окислительное фосфорилирование
- •Организация дыхательной цепи в митохондриях
- •Механизм сопряжения окисления и фосфорилирования
- •Строение атф-синтазы и синтез атф
- •Коэффициент окислительного фосфорилирования
- •Дыхательный контроль
- •Энергетический обмен и теплопродукция
- •5.4. Фотосинтез и хемосинтез. Фотосинтез
- •Световая стадия фотосинтеза
- •Механизм световой фазы фотосинтеза
- •Темновая фаза фотосинтеза
- •Хемосинтез
- •6. Основные метаболические пути углеводов.
- •6.1. Общая схема превращения глюкозы. Метаболизм глюкозы в печени
- •Энергетический выход аэробного распада глюкозы
- •6.3. Пентозфосфатный путь.
- •Биосинтез глюкозы (глюконеогенез)
- •Субстраты для глюконеогенеза
- •Биосинтез гликогена (гликогенез)
- •Распад гликогена (гликогенолиз)
- •П ревращение в жирные кислоты и холестерол
- •6.4. Брожение.
- •6.5. Биосинтез глюкозы. Обходные пути глюконеогенеза. Биосинтез глюкозы (глюконеогенез)
- •Субстраты для глюконеогенеза
- •Биосинтез гликогена (гликогенез)
- •Распад гликогена (гликогенолиз)
- •П ревращение в жирные кислоты и холестерол
- •6.6. Биосинтез глюкозы из двухуглеродных соединений (глиоксилатный цикл).
- •7. Обмен липидов.
- •7.1. Катаболизм глицерина.
- •Окисление до со2 и образование атф
- •7.3. Биосинтез липидов.
- •8. Обмен белков
- •8.1. Общая схема метаболизма аминокислот. Механизмы транспорта аминокислот в клетку. Метаболизм аминокислот в печени
- •8.2. Дезаминирование аминокислот: окислительное дезаминирование, трансаминирование, непрямое дезаминирование (трансдезаминирование).
- •8.3. Превращения углеродного скелета аминокислот. Кетогенные и гликогенные аминокислоты.
- •8.4. Декарбоксилирование аминокислот. Биогенные амины.
- •8.5. Азотфиксация.
- •8.6. Биосинтез заменимых и незаменимых аминокислот.
- •9. Вторичные метаболиты бактерий и растений
- •Библиография
8.6. Биосинтез заменимых и незаменимых аминокислот.
По особенностям биосинтеза протеиногенные аминокислоты подразделяются на пять семейств. Члены каждого семейства имеют общих предшественников, которые образуются в цитратном цикле или при катаболизме углеводов. Пути биосинтеза приведены схематически:
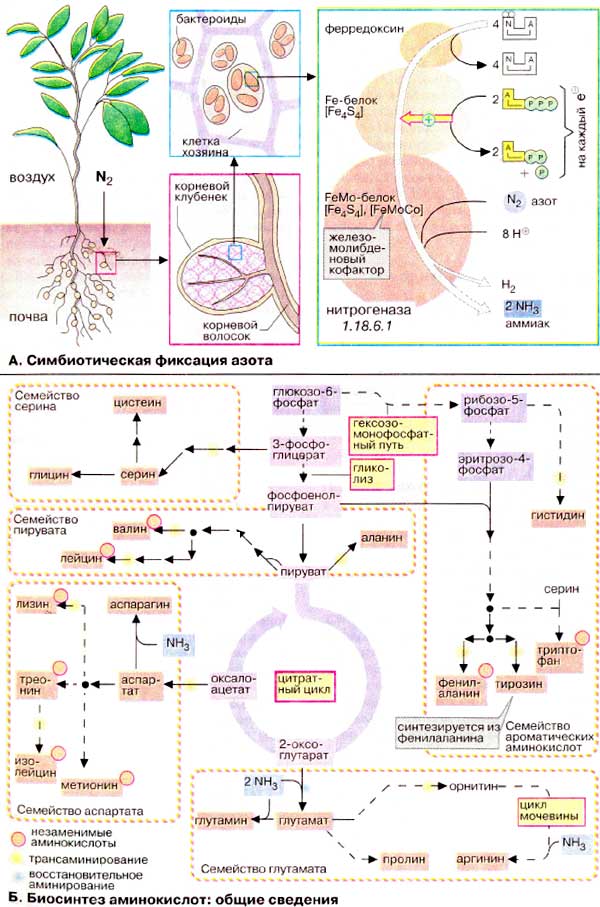
В то время как растения и микроорганизмы могут вполне синтезировать все аминокислоты, млекопитающие в ходе эволюции утратили способность к синтезу примерно половины из 20 протеиногенных аминокислот. Поэтому незаменимые аминокислоты должны поступать с пищей. Так, организм высших организмов не способен синтезировать ароматические аминокислоты de novo (тирозин не является незаменимой аминокислотой только потому, что может образоваться из фенилаланина). К незаменимым аминокислотам принадлежат аминокислоты с разветвленной боковой цепью: валин и изолейцин, а также лейцин, треонин, метионин и лизин. Гистидин и аргинин являются незаменимыми для крыс, но касается ли это также человека — спорно. Наличие незаменимых аминокислот в рационе питания, по-видимому, существенно по крайней мере во время роста организма. Питательная ценность белков решающим образом зависит от содержания незаменимых аминокислот. Растительные белки зачастую бедны лизином или метионином. В то же время животных белки содержат все аминокислоты в сбалансированных соотношениях.
Заменимые аминокислоты (аланин, аспарагиновая и глутаминовая кислоты и их амиды, аспарагин и глутамин) образуются в результате трансаминирования из промежуточных метаболитов — 2-кетокислот. Пролин синтезируется в достаточных количествах из глутамата, а представители серинового семейства (серин, глицин и цистеин) сами являются естественными метаболитами организма животных.
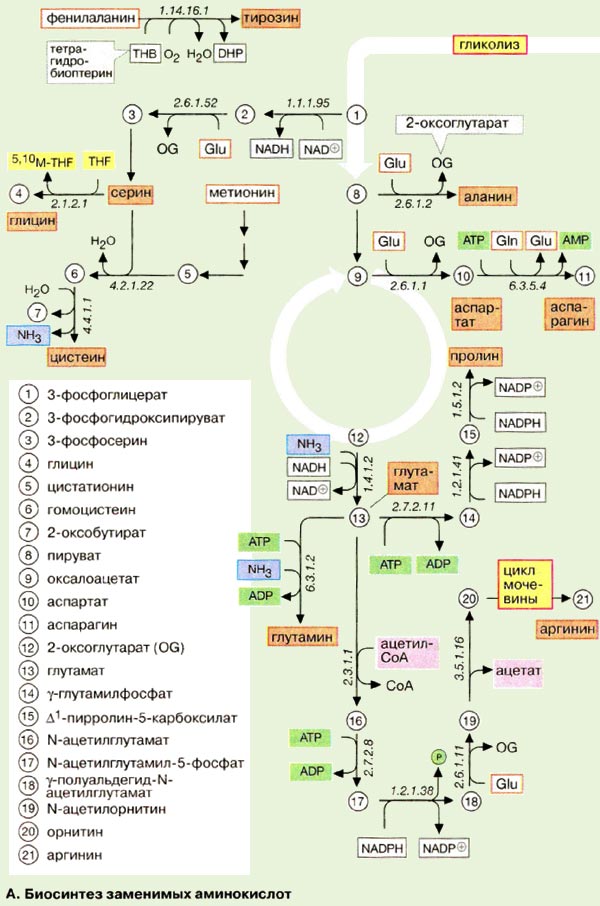
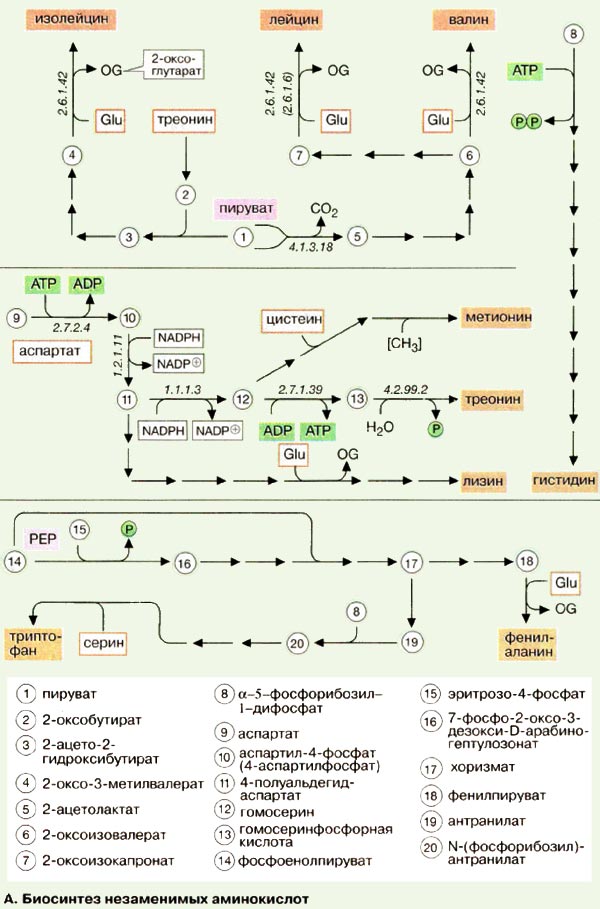
9. Вторичные метаболиты бактерий и растений
Вторичные метаболиты (идиолиты) – низкомолекулярные соединения, не требующиеся для роста в чистой культуре. Они производятся ограниченным числом таксономических групп и часто представляют собой смесь близкородственных соединений, относящихся к одной и той же химической группе. К вторичным метаболитам относятся антибиотики, алкалоиды, гормоны роста растений и токсины.
Микроорганизмы, производящие вторичные метаболиты, вначале проходят стадию быстрого роста – тропофазу – во время которой синтез вторичных веществ незначителен. По мере замедления роста из-за истощения одного или нескольких питательных веществ в культуральной среде микроорганизм переходит в идиофазу. В этот период синтезируются идиолиты. В случае антибиотиков большинство микроорганизмов в процессе тропофазы чувствительны к собственным антибиотикам, однако во время идиофазы они становятся к ним устойчивыми. Чтобы уберечь микроорганизмы, продуцирующие антибиотики, от самоуничтожения, важно быстро достичь идиофазы и затем культивировать микроорганизмы в этой фазе.
Среди вторичных метаболитов ведущее место по объему производства занимают антибиотики.
Антибиотики.
Антибиотики – самый большой класс фармацевтических соединений, синтез которых осуществляется микробными клетками. К этому классу относятся противогрибковые агенты, противоопухолевые лекарства и алкалоиды. Открытие антибиотиков произвело переворот в лечении инфекционных заболеваний. Несмотря на то, что некоторые вопросы о физиологических функциях антибиотиков, их месте в метаболизме и процессах эволюции окончательно не решены, можно сказать, что они появились в борьбе за существование почвенных биоценозов, поэтому многие из них служат средствами защиты и нападения в клетке. Кроме того, антибиотики могут участвовать в процессах детоксикации вредных метаболитов, контролировать некоторые стороны обмена веществ, служить запасными питательными веществами.
Количество открываемых антибиотиков постоянно растет. Если в 1940 г. было известно всего 6 антибиотиков, то в настоящее время описано более 12000 аналогичных соединений, из которых в медицинской практике применяют около 200 препаратов. 97 % известных антибиотиков токсичны, поэтому в практике не используются.
Вначале антибиотики классифицировали по их продуцентам – грибам, эубактериям, актиномицетам. В настоящее время в зависимости от химической природы и ряда других свойств антибиотики делят на ряд классов:
ß-Лактамные (пенициллин, цефалоспорин);
тетрациклины;
макролиды (эритромицин, олеандомицин);
аминогликозиды (гентамицин);
гликопептиды (ванкомицин);
амфениколы (левомицетин);
линкосамиды (линкомицин);
противогрибковые (нистатин, леворин);
противоопухолевые (блеомицин).
Большой вклад в установление структуры ряда антибиотиков внесли М.М. Шемякин, Ю.А. Овчинников, В.Т. Иванов, А.С. Хохлов, Г.Б. Локшин, М.Н. Колосов и др.
Начиная с середины 1960-х гг. в связи с возросшей сложностью выделения эффективных антибиотиков и распространением устойчивости к наиболее широко применяемым соединениям у большого числа патогенных бактерий исследователи перешли от поиска новых антибиотиков к модификации структуры уже имеющихся. Устойчивость к пенициллинам и цефалоспоринам связана с наличием ферментов ß-лактамаз у бактерий, актиномицетов, цианобактерий и дрожжей. Фермент гидролизует амидную связь ß-лактамного цикла в молекуле антибиотика с образованием пенициллиновой кислоты, которая лишена антимикробной активности. Исследователями был открыт новый класс ß-лактамных антибиотиков – тиенамицины, чрезвычайно эффективный против грампозитивных и грамнегативных бактерий, а также способный ингибировать ß-лактамазы. К природным ингибиторам ß-лактамаз относятся клавулановая и оливановая кислоты.
Антибиотики вырабатываются в результате совместного действия продуктов 10-30 генов, поэтому практически невозможно обнаружить отдельные спонтанные мутации, приводящие к повышению выхода антибиотика. В настоящее время большинство высокопродуктивных штаммов продуцентов антибиотиков получено в результате последовательных циклов мутагенеза и селекции. Например, 21 цикл мутагенеза и селекции, продолжавшийся более двадцати лет, позволил четырем группам исследователей увеличить выход пенициллина в 55 раз. В настоящее время промышленный выход пенициллина в 10000 раз превышает выход, полученный в 1941 г. Флори и Чейном.
Биосинтез антибиотиков возрастает в конце тропофазы и достигает максимума в идиофазе. Исследователи считают, что в конце тропофазы изменяется энзиматический статус клеток, появляются индукторы вторичного метаболизма. Поэтому любые механизмы, тормозящие активный рост клеток, стрессовые ситуации, активируют образование антибиотиков.
Процесс культивирования идиолитов проходит две фазы. На первой фазе происходит накопление достаточного количества биомассы, которая выращивается в среде для роста микроорганизмов. Эта фаза должна быть быстрой, а среда дешевой. На второй фазе осуществляются запуск и активный синтез антибиотика. Ферментацию ведут на продуктивной среде, т.к. образование антибиотика регулируется условиями культивирования.
Многие антибиотики происходят от промежуточных соединений обмена первичных метаболитов, поэтому их биосинтез регулируется путем ретроингибирования. Например, биосинтез пенициллина культурой гриба Penicillium chrysogenum контролируется по принципу обратной связи лизином. Этот эффект объясняется тем, что биосинтез как пенициллина, так и лизина осуществляется через общий предшественник – α-аминоадипиновую кислоту. Ингибирование лизином фермента гомоцитратсинтетазы приводит к недостатку α-аминоадипиновой кислоты, что снижает выход антибиотика. Добавление в питательную среду α-аминоадипиновой кислоты предотвращает ингибирующий эффект лизина и активирует биосинтез пенициллина.
ɑ-кетоглутарат + ацетил-КоА

гомоцитратсинтаза

гомоцитрат

гомоизоцитрат
α-аминоадипинат


лизин бензилпенициллин
Рис. Ингибирование лизином биосинтеза бензилпенициллина
Таким образом, регуляция метаболизма имеет большое значение при получении как первичных, так и вторичных метаболитов. Это необходимо учитывать при реализации биотехнологического процесса.
Растения отличаются поразительным многообразием синтетических процессов, конечные продукты которых представлены соединениями самого разного химического строения. В современной медицине применяют жирные кислоты, масла, полисахариды растительного происхождения, а также удивительно разнообразные вторичные метаболиты. Вторичный метаболизм, в отличие от общего для всех организмов первичного обмена, характеризуется таксономическим своеобразием. Вторичный метаболизм растений - это особенность дифференцированных растительных клеток и тканей, он присущ только специализированным органам, приурочен к определённым фазам жизненного цикла. К основным классам вторичных метаболитов относятся алкалоиды, изопреноиды и фенольные соединения. В растениях также синтезируются цианогенные гликозиды, поликетиды, витамины. Из 30 известных витаминов около 20 поступает в организм человека с растительной пищей. Некоторые из перечисленных классов соединений, а также растения, из которых они выделяются, представлены в таблице.
Вторичные метаболиты |
Растение-источник |
Алкалоиды |
Мак снотворный. Красавка белладонна. Барвинок. Раувольфия. Безвременник. Хинное дерево. Табак. |
Изопреноиды: таксолы |
Тиссовое дерево |
сердечные гликозиды, или карденолиды |
Наперстянка. Лиана строфант. Ландыш майский. |
тритерпеновые гликозиды,или сапонины |
Женьшень. Солодка. Аралия. |
стероидные гликозиды |
Лианы диоскорея. |
Фенольные соединения: флавоноиды |
Солодка. Пустырник. Бессмертник. |
Алкалоиды. К настоящему времени известно около 10 тысяч алкалоидов, и они обладают высокой фармакологической активностью. Содержание алкалоидов в растительном сырье обычно не превышает нескольких процентов, но в коре хинном дерева их количество достигает 15-20%. Алкалоиды могут концентрироваться в различных органах и тканях. При этом часто они накапливаются не в тех тканях, где синтезируются. Например, никотин синтезируется в корнях табака, а запасается в листьях. Среди наиболее известных алкалоидов можно назвать морфин, кодеин, папаверин, которые были выделены из коробочек мака снотворного (Papaver somniferum). Алкалоиды красавки белладонны (Atropa belladonna), которую иначе называют «сонной одурью», входят в состав многих медицинских препаратов, таких как, бесалол, беллалгин, беллатаминал, солутан. Широкое распространение в современной онкологии получили алкалоиды из барвинка (Catharanthus roseus) – винбластин и винкристин, а резерпин и аймалин из корней раувольфии (Rauvolfia serpentina) используются в качестве психотропных средств и для понижения давления.
Изопреноиды. По числу выделенных соединений изопреноиды превосходят все другие классы вторичных метаболитов (их более 23 тысяч), но по фармакологической активности они уступают алкалоидам. В данную группу объединены разные по строению соединения. Некоторые из них невозможно заменить синтетическими препаратами, например, таксолы, выделенные из коры тиссового дерева. Они являются чрезвычайно активными цитостатиками, действуя на раковые клетки в очень малых дозах. На них в настоящее время в онкологии возлагают большие надежды.
Наиболее важную группу изопреноидов составляют сердечные гликозиды, или карденолиды. Например, из двух видов наперстянки пурпуровой (Digitalis purpurea) и наперстянки шерстистой (D. lanata) выделено около 50 карденолидов, в том числе дигитоксин. Широко вошёл в медицинскую практику природный гликозид к-строфантозид, являющийся незаменимым средством для оказания скорой помощи: он действует на сердце через 1-3 мин. после внутривенного введения. Этот препарат выделяют из семян лианы Strophanthus kombe, произрастающей в тропических лесах Африки, где местное население использовало сок этого растения в качестве яда для стрел. Сердечные гликозиды из ландыша майского (Cjnvallaria majalis) по активности превосходят другие сердечные гликозиды (например, дигитоксин).
Другие важные для медицины группы изопреноидов представляют собой тритерпеновые гликозиды, или сапонины. Большинство представителей этой группы имеют высокую биологическую активность, которая обусловливает их лечебное действие и применение таких известных биостимуляторов, как женьшень, аралия, солодка.
Стероидные гликозиды отличаются по биологической активности от тритерпеновых. Для современной медицины это исходное сырьё для синтеза многих гормонов и противозачаточных средств. Начиная с 40-х годов прошлого столетия для получения стероидного сырья, в основном, используют гликозид диосгенин из корневищ различных видов лиан из рода Dioscorea. В настоящее время из него получают более 50% всех стероидных лекарственных средств. Исследования последних лет выявили у соединений этой группы и другие важные для медицины свойства.
Фенольные соединения. Самая многочисленная и широко распространённая в растениях группа фенольных соединений - флавоноиды. Они накапливаются в корнях солодки (Glycyrrhiza glabra), траве пустырника (Leonurus cordiaca), цветках бессмертника (Helichryzum arenarium). Флавоноиды отличаются широким спектром фармакологического действия. Они обладают желчегонным, бактерицидным, спазмолитическим, кардиотоническим действием, уменьшают ломкость и проницаемость сосудов (например, рутин), способны связывать и выводить из организма радионуклиды, у них также выявлен противораковый эффект.
Поражающие воображение биосинтетические возможности растений ещё далеко не раскрыты. Из 250 тыс. обитающих на Земле видов обследовано не более 15%, и лишь для некоторых лекарственных растений получены культуры клеток. Так, культуры клеток женьшеня и диоскореи являются основой биотехнологического процесса получения тритерпеновых и стероидных гликозидов. На внедрение этих новых технологий возлагают большие надежды, так как многие редкие или вообще не произрастающие в наших климатических условиях растения можно использовать в виде каллусных или суспензионных культур. К сожалению, техногенный характер цивилизации на нашей планете наносит непоправимый ущерб дикорастущей флоре. Изменяется не только биосфера Земли - среда обитания человека, но и уничтожаются огромные неисследованные кладовые здоровья и долголетия.
