
- •1. Биохимия - молекулярная логика живых организмов. Состав живой материи
- •1.1. Химическая организация клетки. Основные классы биомолекул, общие принципы их строения
- •1.2. Строение и функции клетки эукариотов и прокариотов. Внутриклеточные органеллы.
- •1.3. Особенности организации биосинтетических процессов в клетках прокариот и эукариот
- •2. Аминокислоты и белки
- •Строение и классификация аминокислот
- •Стереоизомерия.
- •Кислотно-основные свойства аминокислот
- •2.2. Пептиды. Строение пептидов. Особенности пептидной связи.
- •2.3. Белки и их основные признаки. Классификации белков. Биологические функции белков и пептидов (ферменты, гормоны, транспортные белки, структурные белки, иммуноглобулины, рецепторы).
- •Классификация белков
- •Биологические функции белков
- •Пространственное расположение полипептидных цепей (Конформация пептидных цепей в белках)
- •2.6.Четвертичная структура белка. Свойства олигомерных белков. Роль четвертичной структуры в проявлении определенных функций белка.
- •К инетика оксигенирования миоглобина и гемоглобина
- •Транспорт двуокиси углерода
- •Молекулярная основа эффекта Бора
- •Регуляция 2,3-бисфосфоглицератом
- •Изофункциональные белки
- •3.Биологический катализ. Ферменты.
- •Особенности ферментов как биокатализаторов
- •Ферменты
- •Принципы построения рабочего названия фермента
- •Список ферментов
- •Механизм действия ферментов. Активный центр ферментов
- •Механизм действия ферментов (на примере фермента холинэстеразы)
- •Причины высокой каталитической активности.
- •3.2.Субстратная специфичность. Специфичность пути превращения.
- •Специфичность пути превращения
- •6.2. Линеризация уравнения Михаэлиса-Ментен
- •Зависимость скорости ферментативной реакции от температуры
- •Зависимость скорости ферментативной реакции от рН
- •Обратимое конкурентное ингибирование аналогами субстрата
- •Обратимое неконкурентное ингибирование
- •Необратимое ингибирование
- •Регуляция количества фермента путем регуляции скорости его синтеза и распада
- •Превращение ферментов в активные формы
- •Регуляция активности ферментов путем их ковалентной модификации
- •Регуляция белковыми ингибиторами
- •Аллостерическая регуляция
- •Ингибирование по принципу обратной связи
- •4. Строение, состав и физиологическая роль клеточной стенки и цитоплазматической мембраны.
- •Функции мембран
- •Мембранные липиды. Образование липидного бислоя мембран.
- •Мембранные белки. Жидко-мозаичное строение мембран
- •Функции мембранных гликолипидов, гликопротеинов, белков:
- •Свойства биологических мембран
- •Пассивный транспорт
- •Активный транспорт
- •Экзо- и эндоцитоз
- •Системы унипорта, симпорта и антипорта
- •4.3. Строение клеточной стенки грамположительных и грамотрицательных бактерий.
- •5. Пути и механизмы преобразования энергии в живых системах
- •5.1. Метаболизм. Катаболизм и анаболизм
- •Макроэргические соединения
- •Фазы освобождения энергии из питательных веществ
- •Роль высокоэнергетических фосфатов в улавливании энергии. Субстратное и окислительное фосфорилирование
- •Организация дыхательной цепи в митохондриях
- •Механизм сопряжения окисления и фосфорилирования
- •Строение атф-синтазы и синтез атф
- •Коэффициент окислительного фосфорилирования
- •Дыхательный контроль
- •Энергетический обмен и теплопродукция
- •5.4. Фотосинтез и хемосинтез. Фотосинтез
- •Световая стадия фотосинтеза
- •Механизм световой фазы фотосинтеза
- •Темновая фаза фотосинтеза
- •Хемосинтез
- •6. Основные метаболические пути углеводов.
- •6.1. Общая схема превращения глюкозы. Метаболизм глюкозы в печени
- •Энергетический выход аэробного распада глюкозы
- •6.3. Пентозфосфатный путь.
- •Биосинтез глюкозы (глюконеогенез)
- •Субстраты для глюконеогенеза
- •Биосинтез гликогена (гликогенез)
- •Распад гликогена (гликогенолиз)
- •П ревращение в жирные кислоты и холестерол
- •6.4. Брожение.
- •6.5. Биосинтез глюкозы. Обходные пути глюконеогенеза. Биосинтез глюкозы (глюконеогенез)
- •Субстраты для глюконеогенеза
- •Биосинтез гликогена (гликогенез)
- •Распад гликогена (гликогенолиз)
- •П ревращение в жирные кислоты и холестерол
- •6.6. Биосинтез глюкозы из двухуглеродных соединений (глиоксилатный цикл).
- •7. Обмен липидов.
- •7.1. Катаболизм глицерина.
- •Окисление до со2 и образование атф
- •7.3. Биосинтез липидов.
- •8. Обмен белков
- •8.1. Общая схема метаболизма аминокислот. Механизмы транспорта аминокислот в клетку. Метаболизм аминокислот в печени
- •8.2. Дезаминирование аминокислот: окислительное дезаминирование, трансаминирование, непрямое дезаминирование (трансдезаминирование).
- •8.3. Превращения углеродного скелета аминокислот. Кетогенные и гликогенные аминокислоты.
- •8.4. Декарбоксилирование аминокислот. Биогенные амины.
- •8.5. Азотфиксация.
- •8.6. Биосинтез заменимых и незаменимых аминокислот.
- •9. Вторичные метаболиты бактерий и растений
- •Библиография
Список ферментов
Все известные ферменты занесены в специальный справочник, в котором информация о ферментах суммирована в виде таблицы.
Таблица. Список ферментов
Шифр |
Рабочее название |
Реакция |
Систематическое название |
Примечание |
КФ1.1.1.27 |
Лактатдегидрогеназа |
L-лактат + НАД+ пируват + НАДНН+ |
L-лактат:НАД+-оксидоредуктаза |
Окисляет и др. оксимонокарбоновые кислоты |
В настоящее время существуют постоянно пополняющиеся базы данных, в которых содержится информация обо всех известных ферментах. Эти базы данных доступны в Интернете. Например, адрес в Интернете международной базы данных "Enzyme nomenclature database": http://expasy.hcuge.ch/sprot/enzyme.html
Механизм действия ферментов. Активный центр ферментов
Ферменты (с точки зрения строения) – это глобулярные белки, которые имеют в глобуле полость или щель определенных размеров – активный центр фермента.
4.1.1 Общие черты активного центра фермента:
а.ц.ф. – небольшая часть белковой молекулы;
а.ц.ф. – имеет строго определенную трехмерную структуру и размеры;
а.ц.ф. – формируется из аминокислотных остатков, удаленных в первичной структуре, но сближенных в третичной структуре;
а.ц.ф. – состоит из связывающего и каталитического участков.
Если белок сложный, то простетическая группа входит в состав а.ц. фермента.
Вся белковая молекула укладывается определенным образом в пространстве, образуя единственно возможный (термодинамически устойчивый) вариант третичной структуры данного белка, а следовательно и уникальный активный центр данного фермента.
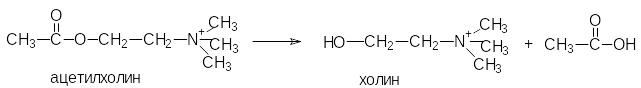
Механизм действия ферментов (на примере фермента холинэстеразы)
Субстрат данного фермента: ацетилхолин – медиатор передачи нервного импульса.
В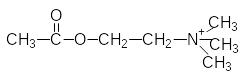
 ответ на выделение окончанием нервного
волокна ацетилхолина, следует ответная
реакция возбуждения нервной клетки.
Чтобы этот процесс протекал непрерывно,
после каждого акта передачи нервного
импульса вызвавшая возбуждение порция
ацетилхолина должна быть гидролизована.
Скорость гидролиза: 1-2 мкг (порция) за
0,1-0,2 мс.
ответ на выделение окончанием нервного
волокна ацетилхолина, следует ответная
реакция возбуждения нервной клетки.
Чтобы этот процесс протекал непрерывно,
после каждого акта передачи нервного
импульса вызвавшая возбуждение порция
ацетилхолина должна быть гидролизована.
Скорость гидролиза: 1-2 мкг (порция) за
0,1-0,2 мс.
Активный центр фермента состоит из двух функционально важных и пространственно разделенных участков:
связывающего, куда входит карбоксильная группа -COO- , электростатически взаимодействующая с заряженным азотом N+ субстрата;
каталитического, ответственного за эстеразную активность фермента, в состав которого входят остатки Ser, His,Tir.
В процессе реакции атом водорода гидроксильной группы Tir активного центра связывается с атомом кислорода ацетилхолина (будущая спиртовая группа продукта реакции – холина). В результате увеличивается положительный заряд на углеродном атоме ацетильной группы субстрата, который атакуется отрицательно заряженным атомом кислорода серина. Отрицательный заряд на атоме кислорода серина возникает в результате образования водородной связи между атомом Н серина и атомом N гистидина. Связь между С (ацетила) и О (холина) разрывается с образованием в качестве промежуточного соединения ацетилсерина. Отщепляющийся от серина протон связывается кислородным атомом тирозина, и первоначальное состояние тирозина восстанавливается. Гидролиз ацетилсерина начинается с диссоциации молекулы воды за счет взаимодействия протона с атомом N гистидина. Освободившийся гидроксил атакует сложноэфирную связь ацетилсерина. Результатом гидролиза является освобождение уксусной кислоты. Ион водорода (Н+), временно связанный с гистидином, освобождается и связывается с кислородом серина. Образовавшиеся холин и уксусная кислота освобождаются из активного центра за счет диффузии.
Все описанные выше процессы более или менее одновременно. Гидролиз ацетилхолина происходит благодаря согласованному действию всех функциональных групп активного центра.
