
- •1. Биохимия - молекулярная логика живых организмов. Состав живой материи
- •1.1. Химическая организация клетки. Основные классы биомолекул, общие принципы их строения
- •1.2. Строение и функции клетки эукариотов и прокариотов. Внутриклеточные органеллы.
- •1.3. Особенности организации биосинтетических процессов в клетках прокариот и эукариот
- •2. Аминокислоты и белки
- •Строение и классификация аминокислот
- •Стереоизомерия.
- •Кислотно-основные свойства аминокислот
- •2.2. Пептиды. Строение пептидов. Особенности пептидной связи.
- •2.3. Белки и их основные признаки. Классификации белков. Биологические функции белков и пептидов (ферменты, гормоны, транспортные белки, структурные белки, иммуноглобулины, рецепторы).
- •Классификация белков
- •Биологические функции белков
- •Пространственное расположение полипептидных цепей (Конформация пептидных цепей в белках)
- •2.6.Четвертичная структура белка. Свойства олигомерных белков. Роль четвертичной структуры в проявлении определенных функций белка.
- •К инетика оксигенирования миоглобина и гемоглобина
- •Транспорт двуокиси углерода
- •Молекулярная основа эффекта Бора
- •Регуляция 2,3-бисфосфоглицератом
- •Изофункциональные белки
- •3.Биологический катализ. Ферменты.
- •Особенности ферментов как биокатализаторов
- •Ферменты
- •Принципы построения рабочего названия фермента
- •Список ферментов
- •Механизм действия ферментов. Активный центр ферментов
- •Механизм действия ферментов (на примере фермента холинэстеразы)
- •Причины высокой каталитической активности.
- •3.2.Субстратная специфичность. Специфичность пути превращения.
- •Специфичность пути превращения
- •6.2. Линеризация уравнения Михаэлиса-Ментен
- •Зависимость скорости ферментативной реакции от температуры
- •Зависимость скорости ферментативной реакции от рН
- •Обратимое конкурентное ингибирование аналогами субстрата
- •Обратимое неконкурентное ингибирование
- •Необратимое ингибирование
- •Регуляция количества фермента путем регуляции скорости его синтеза и распада
- •Превращение ферментов в активные формы
- •Регуляция активности ферментов путем их ковалентной модификации
- •Регуляция белковыми ингибиторами
- •Аллостерическая регуляция
- •Ингибирование по принципу обратной связи
- •4. Строение, состав и физиологическая роль клеточной стенки и цитоплазматической мембраны.
- •Функции мембран
- •Мембранные липиды. Образование липидного бислоя мембран.
- •Мембранные белки. Жидко-мозаичное строение мембран
- •Функции мембранных гликолипидов, гликопротеинов, белков:
- •Свойства биологических мембран
- •Пассивный транспорт
- •Активный транспорт
- •Экзо- и эндоцитоз
- •Системы унипорта, симпорта и антипорта
- •4.3. Строение клеточной стенки грамположительных и грамотрицательных бактерий.
- •5. Пути и механизмы преобразования энергии в живых системах
- •5.1. Метаболизм. Катаболизм и анаболизм
- •Макроэргические соединения
- •Фазы освобождения энергии из питательных веществ
- •Роль высокоэнергетических фосфатов в улавливании энергии. Субстратное и окислительное фосфорилирование
- •Организация дыхательной цепи в митохондриях
- •Механизм сопряжения окисления и фосфорилирования
- •Строение атф-синтазы и синтез атф
- •Коэффициент окислительного фосфорилирования
- •Дыхательный контроль
- •Энергетический обмен и теплопродукция
- •5.4. Фотосинтез и хемосинтез. Фотосинтез
- •Световая стадия фотосинтеза
- •Механизм световой фазы фотосинтеза
- •Темновая фаза фотосинтеза
- •Хемосинтез
- •6. Основные метаболические пути углеводов.
- •6.1. Общая схема превращения глюкозы. Метаболизм глюкозы в печени
- •Энергетический выход аэробного распада глюкозы
- •6.3. Пентозфосфатный путь.
- •Биосинтез глюкозы (глюконеогенез)
- •Субстраты для глюконеогенеза
- •Биосинтез гликогена (гликогенез)
- •Распад гликогена (гликогенолиз)
- •П ревращение в жирные кислоты и холестерол
- •6.4. Брожение.
- •6.5. Биосинтез глюкозы. Обходные пути глюконеогенеза. Биосинтез глюкозы (глюконеогенез)
- •Субстраты для глюконеогенеза
- •Биосинтез гликогена (гликогенез)
- •Распад гликогена (гликогенолиз)
- •П ревращение в жирные кислоты и холестерол
- •6.6. Биосинтез глюкозы из двухуглеродных соединений (глиоксилатный цикл).
- •7. Обмен липидов.
- •7.1. Катаболизм глицерина.
- •Окисление до со2 и образование атф
- •7.3. Биосинтез липидов.
- •8. Обмен белков
- •8.1. Общая схема метаболизма аминокислот. Механизмы транспорта аминокислот в клетку. Метаболизм аминокислот в печени
- •8.2. Дезаминирование аминокислот: окислительное дезаминирование, трансаминирование, непрямое дезаминирование (трансдезаминирование).
- •8.3. Превращения углеродного скелета аминокислот. Кетогенные и гликогенные аминокислоты.
- •8.4. Декарбоксилирование аминокислот. Биогенные амины.
- •8.5. Азотфиксация.
- •8.6. Биосинтез заменимых и незаменимых аминокислот.
- •9. Вторичные метаболиты бактерий и растений
- •Библиография
Особенности ферментов как биокатализаторов
Ферменты как катализаторы имеют ряд особенностей:
Высокоэффективные катализаторы - ускоряют реакцию в 1010раз:
1 моль каталазы при 00 С обеспечивает разложение за 1 мин 5 млн. H2O2, в то время как 1 моль Pt катализирует только 250- 2000 молекул H2O2.
Высокоспецифичны - катализируют, как правило, реакцию одного типа или воздействуют на один субстрат. Это наиболее важное свойство ферментов.
Эффективно работают в мягких условиях.
Синтез аммиака по реакции: N2 + 3H2 = 2NH3 проводят при t = 500-5500C, p = 107-108Па, ферменты, содержащиеся в бобовых культурах обеспечивают протекание подобного процесса при обычных условиях.
Ферменты - это катализаторы, работу которых можно регулировать.
Классификации ферментов и номенклатура.
Классификация ферментов по строению
Ферменты
|
|
|
простые- состоят только из полипептидных цепей |
сложные- в состав сложных входят группы небелковой природы |
|
|
|
|
|
кофермент или простетическая группа (группа небелковой природы) |
апофермент (белковая часть фермента) |
ФЕРМЕНТЫ по уровню организации белковых молекул
могут иметь только третичную структуру (одну полипептидную цепь) и четвертичную структуру (несколько полипептидных цепей). Последние - аллостерические ферменты.
Классификация ферментов по типу катализируемой реакции и номенклатура ферментов
В номенклатуре ферментов, введенной Международным биохимическим союзом (IUB) используется принцип классификации ферментов по типу катализируемой реакции и ее механизму. Основные принципы номенклатуры следующие:
Выделяют 6 классов ферментов, катализирующих 6 типов реакций:
Оксидоредуктазы.
Трансферазы.
Гидролазы.
Лиазы
Изомеразы.
Лигазы.
В каждом из 6 классов имеется несколько подклассов (от 4 до 13).
Систематическое название фермента состоит из 2-х частей: названия субстрата, типа катализируемой реакции и части слова -аза.
Дополнительная информация, если она необходима для уточнения, заключается в скобках.
Н апример:
апример:
L-малат пируват
Фермент L-малат:NAD+оксидоредуктаза (декарбоксилаза)
Каждый фермент обозначается специальным шифром, указывающим номер класса, подкласса, подподкласса и номер фермента в подподклассе. Например: 2.6.1.2 - аланин:оксоглутарат-аминотрасфераза.
Помимо систематического названия указывается рабочее название фермента.
Принципы построения рабочего названия фермента
Оксидоредуктазы - ферменты, катализирующие реакции окисления-восстановления.
Окисление может осуществляться двумя путями:
а) Отщепление от субстрата атомов водорода.
В этом случае рабочее название там, где это, возможно, включает термин дегидрогеназа.
Например:
Н азвание
фермента включает название донора
водорода и термин - дегидрогеназа:
лактатдегидрогеназа.
азвание
фермента включает название донора
водорода и термин - дегидрогеназа:
лактатдегидрогеназа.
Альтернативой этому может быть использование термина - редуктаза. Название редуктаз складывается из названия акцептора атомов водорода и термина - редуктаза.
Например:
Г идроксиметилглутарил-СоА-редуктаза
идроксиметилглутарил-СоА-редуктаза
Термин оксидаза употребляется, когда акцептором водорода является кислород. Например, цитохромоксидаза.
б) Включение в молекулу субстрата кислорода.
Ферменты, катализирующие данную реакцию, называются оксигеназами (монооксигеназами или диоксигеназами, в зависимости от количества атомов кислорода, включенных в молекулу субстрата).
Пример:
Ф енилаланинмонооксигеназа
енилаланинмонооксигеназа
Трансферазы катализируют реакции переноса различных групп от одного субстрата, который является донором, к другому - акцептору. В зависимости от переносимых групп ферменты носят названия метилтрансферазы, аминотрансферазы, ацетилтрансферазы и т.д.
Рабочее название трасфераз обычно строится по типу: акцептор - переносимая группа - термин трансфераза.
Х олинацетилтрансфераза
олинацетилтрансфераза
Реже название фермента складывается по типу: донор - переносимая группа - трансфераза. такой тип названия характерен для аминотрансфераз.
А ланинаминотрансфераза
(т.к. 2-оксоглутарат-универсальный
сборщик аминогрупп).
ланинаминотрансфераза
(т.к. 2-оксоглутарат-универсальный
сборщик аминогрупп).
В ряде случаев используются специальные термины, например: киназа переносит фосфатные группы от АТФ на какой-либо акцептор. Название складывается из названия акцептора и термина киназа.
ф осфоенолпируват
осфоенолпируват
Фермент - пируваткиназа.
Гидролазы катализируют разрыв связей в молекуле за счет присоединения молекул воды. Название складывается из названия субстрата + окончание аза.
Ф ермент
- аргиназа.
ермент
- аргиназа.
Некоторые ферменты этого класса имеют название, в состав которого не входит окончание аза.
Например, ацетоацетилкофермент А
Ф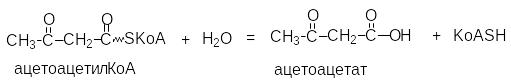 ермент
- ацетоацетилКоАгидролаза.
ермент
- ацетоацетилКоАгидролаза.
К гидролазам относятся все пищевые ферменты, а также ферменты, входящие в состав лизосом - амилолитические, протеолитические, липолитические, нуклеазы, фосфотазы.
Лиазы катализируют разрыв связи в молекуле или отрыв фрагмента с образованием двойной связи. Для ферментов этого класса часто употребляется термины декарбоксилаза, карбоксилаза, дегидратаза, гидратаза, альдолаза. Название строится из названия субстрата + соответствующий термин.
Ф ермент
- пируватдекарбоксилаза.
ермент
- пируватдекарбоксилаза.
Ф ермент
- фумаратгидратаза
ермент
- фумаратгидратаза
Ф ермент
- цитратсинтаза.
ермент
- цитратсинтаза.
Изомеразы катализируют превращения в пределах одной молекулы, т.е. катализируют реакции внутримолекулярной перестройки. Название ферментов зависит от типа реакции изомеризации.
Например:
D-аланин L-аланин (фермент - аланинрацемаза)
глюкозо-6-фосфат фруктозо-6-фосфат (фермент - глюкозофосфатизомераза).
Лигазы (синтетазы) катализируют присоединение молекул друг к другу за счет энергии макроэргических фосфодиэфирных связей молекулы АТФ. Название складывается следующим образом: конечный продукт реакции + термин «синтетаза»
Ф ермент
- глутаминсинтетаза.
ермент
- глутаминсинтетаза.
В качестве источников энергии могут выступать и другие нуклеотиды (ГТФ).
Ф ермент
- СукцинилКоАсинтетаза.
ермент
- СукцинилКоАсинтетаза.
В реакциях, где одним из исходных соединений является СО2 используют термин карбоксилаза. Название фермента: название субстрата + термин «карбоксилаза».
Ф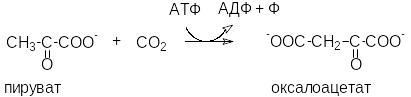 ермент
- пируваткарбоксилаза.
ермент
- пируваткарбоксилаза.
