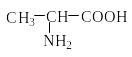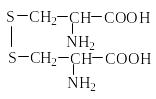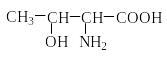- •1. Биохимия - молекулярная логика живых организмов. Состав живой материи
- •1.1. Химическая организация клетки. Основные классы биомолекул, общие принципы их строения
- •1.2. Строение и функции клетки эукариотов и прокариотов. Внутриклеточные органеллы.
- •1.3. Особенности организации биосинтетических процессов в клетках прокариот и эукариот
- •2. Аминокислоты и белки
- •Строение и классификация аминокислот
- •Стереоизомерия.
- •Кислотно-основные свойства аминокислот
- •2.2. Пептиды. Строение пептидов. Особенности пептидной связи.
- •2.3. Белки и их основные признаки. Классификации белков. Биологические функции белков и пептидов (ферменты, гормоны, транспортные белки, структурные белки, иммуноглобулины, рецепторы).
- •Классификация белков
- •Биологические функции белков
- •Пространственное расположение полипептидных цепей (Конформация пептидных цепей в белках)
- •2.6.Четвертичная структура белка. Свойства олигомерных белков. Роль четвертичной структуры в проявлении определенных функций белка.
- •К инетика оксигенирования миоглобина и гемоглобина
- •Транспорт двуокиси углерода
- •Молекулярная основа эффекта Бора
- •Регуляция 2,3-бисфосфоглицератом
- •Изофункциональные белки
- •3.Биологический катализ. Ферменты.
- •Особенности ферментов как биокатализаторов
- •Ферменты
- •Принципы построения рабочего названия фермента
- •Список ферментов
- •Механизм действия ферментов. Активный центр ферментов
- •Механизм действия ферментов (на примере фермента холинэстеразы)
- •Причины высокой каталитической активности.
- •3.2.Субстратная специфичность. Специфичность пути превращения.
- •Специфичность пути превращения
- •6.2. Линеризация уравнения Михаэлиса-Ментен
- •Зависимость скорости ферментативной реакции от температуры
- •Зависимость скорости ферментативной реакции от рН
- •Обратимое конкурентное ингибирование аналогами субстрата
- •Обратимое неконкурентное ингибирование
- •Необратимое ингибирование
- •Регуляция количества фермента путем регуляции скорости его синтеза и распада
- •Превращение ферментов в активные формы
- •Регуляция активности ферментов путем их ковалентной модификации
- •Регуляция белковыми ингибиторами
- •Аллостерическая регуляция
- •Ингибирование по принципу обратной связи
- •4. Строение, состав и физиологическая роль клеточной стенки и цитоплазматической мембраны.
- •Функции мембран
- •Мембранные липиды. Образование липидного бислоя мембран.
- •Мембранные белки. Жидко-мозаичное строение мембран
- •Функции мембранных гликолипидов, гликопротеинов, белков:
- •Свойства биологических мембран
- •Пассивный транспорт
- •Активный транспорт
- •Экзо- и эндоцитоз
- •Системы унипорта, симпорта и антипорта
- •4.3. Строение клеточной стенки грамположительных и грамотрицательных бактерий.
- •5. Пути и механизмы преобразования энергии в живых системах
- •5.1. Метаболизм. Катаболизм и анаболизм
- •Макроэргические соединения
- •Фазы освобождения энергии из питательных веществ
- •Роль высокоэнергетических фосфатов в улавливании энергии. Субстратное и окислительное фосфорилирование
- •Организация дыхательной цепи в митохондриях
- •Механизм сопряжения окисления и фосфорилирования
- •Строение атф-синтазы и синтез атф
- •Коэффициент окислительного фосфорилирования
- •Дыхательный контроль
- •Энергетический обмен и теплопродукция
- •5.4. Фотосинтез и хемосинтез. Фотосинтез
- •Световая стадия фотосинтеза
- •Механизм световой фазы фотосинтеза
- •Темновая фаза фотосинтеза
- •Хемосинтез
- •6. Основные метаболические пути углеводов.
- •6.1. Общая схема превращения глюкозы. Метаболизм глюкозы в печени
- •Энергетический выход аэробного распада глюкозы
- •6.3. Пентозфосфатный путь.
- •Биосинтез глюкозы (глюконеогенез)
- •Субстраты для глюконеогенеза
- •Биосинтез гликогена (гликогенез)
- •Распад гликогена (гликогенолиз)
- •П ревращение в жирные кислоты и холестерол
- •6.4. Брожение.
- •6.5. Биосинтез глюкозы. Обходные пути глюконеогенеза. Биосинтез глюкозы (глюконеогенез)
- •Субстраты для глюконеогенеза
- •Биосинтез гликогена (гликогенез)
- •Распад гликогена (гликогенолиз)
- •П ревращение в жирные кислоты и холестерол
- •6.6. Биосинтез глюкозы из двухуглеродных соединений (глиоксилатный цикл).
- •7. Обмен липидов.
- •7.1. Катаболизм глицерина.
- •Окисление до со2 и образование атф
- •7.3. Биосинтез липидов.
- •8. Обмен белков
- •8.1. Общая схема метаболизма аминокислот. Механизмы транспорта аминокислот в клетку. Метаболизм аминокислот в печени
- •8.2. Дезаминирование аминокислот: окислительное дезаминирование, трансаминирование, непрямое дезаминирование (трансдезаминирование).
- •8.3. Превращения углеродного скелета аминокислот. Кетогенные и гликогенные аминокислоты.
- •8.4. Декарбоксилирование аминокислот. Биогенные амины.
- •8.5. Азотфиксация.
- •8.6. Биосинтез заменимых и незаменимых аминокислот.
- •9. Вторичные метаболиты бактерий и растений
- •Библиография
1.3. Особенности организации биосинтетических процессов в клетках прокариот и эукариот
Впервые серьёзное внимание на существенные отличия микроорганизмов от растений и животных обратил немецкий учёный Э. Геккель. Он предложил выделить все микроорганизмы в самостоятельное царство Протиста (Protista) наряду с царством растений (Plantae) и царством животных (Animalia). Подразделение протист на низшие и высшие произошло в соответствии с двумя выявленными типами клеточной организации – эукариотической и прокариотической. Высшие протисты – микроскопические животные (простейшие), микроскопические водоросли и микроскопические грибы (плесени и дрожжи), подобно растениям и животным, имеют эукариотическое строение клеток. Низшие протисты – бактерии, в том числе актиномицеты и синезелёные водоросли (цианобактерии), имеют прокариотическое строение.
Основные различия прокариот и эукариот:
Прокариоты могут существовать только в аэробных или только в анаэробных условиях, или и в тех и в других. Необходимую энергию они получают в процессе дыхания, брожения, фотосинтеза или хемосинтеза. Эукариоты – относятся к аэробным организмам.
У эукариот генетический материал локализован в структурно оформленном ядре. У прокариот наследственный материал представлен клубком двойной спиральной нити ДНК и не отделён от цитоплазмы какой – либо мембраной.
У прокариот, в отличие от эукариот, отсутствуют внутриклеточные органеллы, имеющие хотя бы элементарную мембрану.
У прокариот рибосомы имеют меньший размер.
Клеточная стенка прокариот содержит специальный полимер пептидогликан, которого нет у эукариот.
Жгутики прокариот состоят из одной или нескольких фибрилл, а у эукариот каждый жгутик состоит из микротрубочек – 9 по периметру и 2 в центре.
Многие прокариоты способны фиксировать молекулярный азот, эукариоты этим свойством не обладают.
Многие прокариоты способны выделять в окружающую среду продукты метаболизма (органические кислоты, витамины, антибиотики и др.)
2. Аминокислоты и белки
2.1. -Аминокислоты как структурные компоненты белков. Классификация аминокислот по характеру боковых заместителей. Кислотно-основные свойства аминокислот
Ключ к пониманию структуры любого белка дает небольшая группа довольно простых молекул - -аминокислот, играющих роль строительных блоков. Для построения всех белков используется один и тот же набор 20 различных, ковалентно связанных друг с другом в определенной, характерной только для данного белка последовательности. Каждая аминокислота благодаря особенностям ее боковой цепи наделена химической индивидуальностью, поэтому всю группу 20 аминокислот можно рассматривать как алфавит "языка" белковой структуры.
Строение и классификация аминокислот
В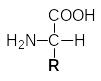 се
20 аминокислот, встречающихся в белках,
характеризуются общей структурной
особенностью - наличием карбоксильной
и аминогруппы, связанных с одним и тем
же атомом углерода. Различаются же
аминокислоты боковыми цепями (R-группами).
се
20 аминокислот, встречающихся в белках,
характеризуются общей структурной
особенностью - наличием карбоксильной
и аминогруппы, связанных с одним и тем
же атомом углерода. Различаются же
аминокислоты боковыми цепями (R-группами).
Формулы и тривиальные названия важнейших аминокислот приведены в таблице. Для биологического функционирования аминокислот в составе белков определяющим является полярность радикала R. По этому признаку аминокислоты разделяют на следующие основные группы.
Таблица. Важнейшие -аминокислоты RCH(NH2)COOH
Формула |
Название |
Обозначение |
pI |
Аминокислоты, содержащие неполярный радикал R
|
|||
|
Глицин |
Gly |
5,97 |
|
Аланин |
Ala |
6,0 |
|
Валин |
Val |
5,96 |
|
Лейцин |
Leu |
5,98 |
|
Изолейцин |
Ile |
6,02 |
|
Фенилаланин |
Phe |
5,48 |
|
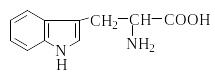
Триптофан |
Trp |
5,89 |
|
Пролин (изгиб пептидной цепи) |
Pro |
6,30 |
|
Метионин |
Met |
5,74 |
|
Цистин |
(Cys)2 |
5,0 |
Аминокислоты, содержащие полярный неионогенный радикал R
|
|||
|
Серин |
Ser |
5,68 |
|
Треонин
|
Thr |
5,60 |
|
Гидроксипролин Не имеет генетический код |
Hyp |
5,8 |
|
Аспаргин |
Asn |
5,41 |
|
Глутамин |
Gln |
5,65 |
Аминокислоты, содержащие полярный положительно заряженный радикал R |
|||
|
Лизин |
Lys |
9,74 |
|
5-Гидроксилизин Не имеет генетич код |
|
9,15 |
|
Аргинин |
Arg |
10,76 |
|
Гистидин |
His |
7,59 |
Аминокислоты, содержащие полярный отрицательно заряженный радикал R |
|||
|
Аспаргиновая кислота |
Asp |
2,77 |
|
Глутаминовая кислота |
Glu |
3,22 |
|
Тирозин |
Tyr |
5,66 |
|
Цистеин |
Cys |
5,07 |
Белки-гистоны содержат много лизина и аргинина.
Аминокислоты, содержащие неполярный радикал R. Такие группы располагаются внутри молекулы белка и обуславливают гидрофобные взаимодействия.
Аминокислоты, содержащие полярный неионогенный радикал R. Аминокислоты этого типа имеют в составе бокового радикала полярные группы, не способные к ионизации в водной среде (спиртовый гидроксил, амидная группа). Такие группы могут располагаться как внутри, так и на поверхности молекулы белка. Они участвуют в образовании водородных связей с другими полярными группами.

Аминокислоты, содержащие радикал R, способный к ионизации в водной среде с образованием положительно или отрицательно запряженных групп. Такие аминокислоты содержат в боковом радикале дополнительный основный или кислотный центр, который в водном растворе может соответственно присоединять или отдавать протон.
В белках ионогенные группы этих аминокислот располагаются, как правило, на поверхности молекулы и обуславливают электростатические взаимодействия.