
- •1. Биохимия - молекулярная логика живых организмов. Состав живой материи
- •1.1. Химическая организация клетки. Основные классы биомолекул, общие принципы их строения
- •1.2. Строение и функции клетки эукариотов и прокариотов. Внутриклеточные органеллы.
- •1.3. Особенности организации биосинтетических процессов в клетках прокариот и эукариот
- •2. Аминокислоты и белки
- •Строение и классификация аминокислот
- •Стереоизомерия.
- •Кислотно-основные свойства аминокислот
- •2.2. Пептиды. Строение пептидов. Особенности пептидной связи.
- •2.3. Белки и их основные признаки. Классификации белков. Биологические функции белков и пептидов (ферменты, гормоны, транспортные белки, структурные белки, иммуноглобулины, рецепторы).
- •Классификация белков
- •Биологические функции белков
- •Пространственное расположение полипептидных цепей (Конформация пептидных цепей в белках)
- •2.6.Четвертичная структура белка. Свойства олигомерных белков. Роль четвертичной структуры в проявлении определенных функций белка.
- •К инетика оксигенирования миоглобина и гемоглобина
- •Транспорт двуокиси углерода
- •Молекулярная основа эффекта Бора
- •Регуляция 2,3-бисфосфоглицератом
- •Изофункциональные белки
- •3.Биологический катализ. Ферменты.
- •Особенности ферментов как биокатализаторов
- •Ферменты
- •Принципы построения рабочего названия фермента
- •Список ферментов
- •Механизм действия ферментов. Активный центр ферментов
- •Механизм действия ферментов (на примере фермента холинэстеразы)
- •Причины высокой каталитической активности.
- •3.2.Субстратная специфичность. Специфичность пути превращения.
- •Специфичность пути превращения
- •6.2. Линеризация уравнения Михаэлиса-Ментен
- •Зависимость скорости ферментативной реакции от температуры
- •Зависимость скорости ферментативной реакции от рН
- •Обратимое конкурентное ингибирование аналогами субстрата
- •Обратимое неконкурентное ингибирование
- •Необратимое ингибирование
- •Регуляция количества фермента путем регуляции скорости его синтеза и распада
- •Превращение ферментов в активные формы
- •Регуляция активности ферментов путем их ковалентной модификации
- •Регуляция белковыми ингибиторами
- •Аллостерическая регуляция
- •Ингибирование по принципу обратной связи
- •4. Строение, состав и физиологическая роль клеточной стенки и цитоплазматической мембраны.
- •Функции мембран
- •Мембранные липиды. Образование липидного бислоя мембран.
- •Мембранные белки. Жидко-мозаичное строение мембран
- •Функции мембранных гликолипидов, гликопротеинов, белков:
- •Свойства биологических мембран
- •Пассивный транспорт
- •Активный транспорт
- •Экзо- и эндоцитоз
- •Системы унипорта, симпорта и антипорта
- •4.3. Строение клеточной стенки грамположительных и грамотрицательных бактерий.
- •5. Пути и механизмы преобразования энергии в живых системах
- •5.1. Метаболизм. Катаболизм и анаболизм
- •Макроэргические соединения
- •Фазы освобождения энергии из питательных веществ
- •Роль высокоэнергетических фосфатов в улавливании энергии. Субстратное и окислительное фосфорилирование
- •Организация дыхательной цепи в митохондриях
- •Механизм сопряжения окисления и фосфорилирования
- •Строение атф-синтазы и синтез атф
- •Коэффициент окислительного фосфорилирования
- •Дыхательный контроль
- •Энергетический обмен и теплопродукция
- •5.4. Фотосинтез и хемосинтез. Фотосинтез
- •Световая стадия фотосинтеза
- •Механизм световой фазы фотосинтеза
- •Темновая фаза фотосинтеза
- •Хемосинтез
- •6. Основные метаболические пути углеводов.
- •6.1. Общая схема превращения глюкозы. Метаболизм глюкозы в печени
- •Энергетический выход аэробного распада глюкозы
- •6.3. Пентозфосфатный путь.
- •Биосинтез глюкозы (глюконеогенез)
- •Субстраты для глюконеогенеза
- •Биосинтез гликогена (гликогенез)
- •Распад гликогена (гликогенолиз)
- •П ревращение в жирные кислоты и холестерол
- •6.4. Брожение.
- •6.5. Биосинтез глюкозы. Обходные пути глюконеогенеза. Биосинтез глюкозы (глюконеогенез)
- •Субстраты для глюконеогенеза
- •Биосинтез гликогена (гликогенез)
- •Распад гликогена (гликогенолиз)
- •П ревращение в жирные кислоты и холестерол
- •6.6. Биосинтез глюкозы из двухуглеродных соединений (глиоксилатный цикл).
- •7. Обмен липидов.
- •7.1. Катаболизм глицерина.
- •Окисление до со2 и образование атф
- •7.3. Биосинтез липидов.
- •8. Обмен белков
- •8.1. Общая схема метаболизма аминокислот. Механизмы транспорта аминокислот в клетку. Метаболизм аминокислот в печени
- •8.2. Дезаминирование аминокислот: окислительное дезаминирование, трансаминирование, непрямое дезаминирование (трансдезаминирование).
- •8.3. Превращения углеродного скелета аминокислот. Кетогенные и гликогенные аминокислоты.
- •8.4. Декарбоксилирование аминокислот. Биогенные амины.
- •8.5. Азотфиксация.
- •8.6. Биосинтез заменимых и незаменимых аминокислот.
- •9. Вторичные метаболиты бактерий и растений
- •Библиография
Макроэргические соединения
Энергия, освобождающаяся при реакциях гидролиза разных веществ, обычно невелика. Если она превышает 30 кДж/моль, то такую связь называют высокоэнергетической. Энергия гидролиза некоторых субстратов приведена в таблице.
Макроэргические соединения можно разделить на две группы:
Соединения, образующиеся в ходе процессов катаболизма и служащие для превращения энергии в качестве передаточного звена (АТФ; 1,3-дифосфоглицерат и фосфоенолпируват – промежуточные метаболиты катаболизма углеводов).
Соединения, которые могут быть использованы тканями в качестве "аварийного" источника энергии (креатинфосфат локализован в основном в мышцах и служит дополнительным источником энергии при стремительных кратковременных нагрузках).
Соединение |
-G', кДж/моль |
Фосфоенолпируват |
67,9 |
1,3-Дифосфоглицерат (продукт: 3-фосфоглицерат) |
49,3 |
Креатинфосфат |
43,1 |
АТФ АДФ + Ф |
30,5 |
АДФ АМФ + Ф |
27,6 |
Пирофосфат |
27,6 |
Глюкозо-1-фосфат |
20,9 |
АМФ |
14,2 |
Среднее положение АТФ по величине стандартной свободной энергии гидролиза позволяет ему служить донором высокоэнергетического фосфата для соединений, имеющих меньшую, чем АТФ величину стандартной свободной энергии гидролиза. В то же время при наличии соответствующих ферментных систем АДФ может акцептировать высокоэнергетический фосфат (с образованием АТФ) от тех соединений, которые обладают большей величиной стандартной свободной энергии гидролиза. Т.о., цикл АДФ/АТФ связывает процессы, генерирующие высокоэнергетический фосфат, с процессами, потребляющими энергию высокоэнергетических фосфатов.
Фазы освобождения энергии из питательных веществ
Характер метаболизма в тканях во многом определяется питанием. У человека метаболическим превращениям подвергаются, главным образом, глюкоза, жиры и аминокислоты. Глюкоза и аминокислоты - структурные компоненты белков и углеводов. Таким образом, необходимыми компонентами пищи являются белки углеводы и жиры.
В ходе извлечения энергии из различных субстратов можно условно выделить три фазы катаболизма питательных веществ.
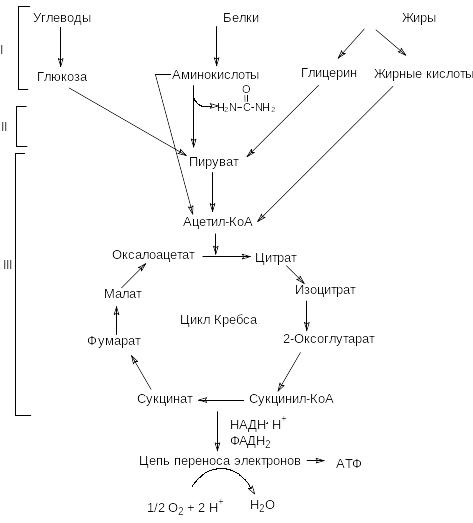
Рис. Фазы катаболизма белков, жиров, углеводов
Первая фаза - подготовительная. Она необходима для превращения полимеров, поступающих с пищей или находящихся внутри клетки, в удобную для извлечения энергии форму - мономеры. На этом этапе освобождается около 1% всей энергии, запасенной в питательных веществах. Эта энергия рассеивается в форме теплоты.
Вторая фаза - частичный распад мономеров до ключевых промежуточных продуктов: пирувата, ацетил-КоА и некоторых метаболитов цикла Кребса. На этом этапе освобождается около 20% энергии. Эта стадия называется промежуточный обмен. Реакции промежуточного обмена протекают в цитоплазме.
Третья фаза - окончательный распад всех веществ до CO2 и H2O. Этот этап включает реакции общего пути катаболизма (окислительное декарбоксилирование пирувата, цикл Кребса) и цепь переноса электронов. Примерно 80% всей энергии химических связей освобождается в данной фазе. Все реакции этой фазы локализуются в митохондриях.
