
- •1. Биохимия - молекулярная логика живых организмов. Состав живой материи
- •1.1. Химическая организация клетки. Основные классы биомолекул, общие принципы их строения
- •1.2. Строение и функции клетки эукариотов и прокариотов. Внутриклеточные органеллы.
- •1.3. Особенности организации биосинтетических процессов в клетках прокариот и эукариот
- •2. Аминокислоты и белки
- •Строение и классификация аминокислот
- •Стереоизомерия.
- •Кислотно-основные свойства аминокислот
- •2.2. Пептиды. Строение пептидов. Особенности пептидной связи.
- •2.3. Белки и их основные признаки. Классификации белков. Биологические функции белков и пептидов (ферменты, гормоны, транспортные белки, структурные белки, иммуноглобулины, рецепторы).
- •Классификация белков
- •Биологические функции белков
- •Пространственное расположение полипептидных цепей (Конформация пептидных цепей в белках)
- •2.6.Четвертичная структура белка. Свойства олигомерных белков. Роль четвертичной структуры в проявлении определенных функций белка.
- •К инетика оксигенирования миоглобина и гемоглобина
- •Транспорт двуокиси углерода
- •Молекулярная основа эффекта Бора
- •Регуляция 2,3-бисфосфоглицератом
- •Изофункциональные белки
- •3.Биологический катализ. Ферменты.
- •Особенности ферментов как биокатализаторов
- •Ферменты
- •Принципы построения рабочего названия фермента
- •Список ферментов
- •Механизм действия ферментов. Активный центр ферментов
- •Механизм действия ферментов (на примере фермента холинэстеразы)
- •Причины высокой каталитической активности.
- •3.2.Субстратная специфичность. Специфичность пути превращения.
- •Специфичность пути превращения
- •6.2. Линеризация уравнения Михаэлиса-Ментен
- •Зависимость скорости ферментативной реакции от температуры
- •Зависимость скорости ферментативной реакции от рН
- •Обратимое конкурентное ингибирование аналогами субстрата
- •Обратимое неконкурентное ингибирование
- •Необратимое ингибирование
- •Регуляция количества фермента путем регуляции скорости его синтеза и распада
- •Превращение ферментов в активные формы
- •Регуляция активности ферментов путем их ковалентной модификации
- •Регуляция белковыми ингибиторами
- •Аллостерическая регуляция
- •Ингибирование по принципу обратной связи
- •4. Строение, состав и физиологическая роль клеточной стенки и цитоплазматической мембраны.
- •Функции мембран
- •Мембранные липиды. Образование липидного бислоя мембран.
- •Мембранные белки. Жидко-мозаичное строение мембран
- •Функции мембранных гликолипидов, гликопротеинов, белков:
- •Свойства биологических мембран
- •Пассивный транспорт
- •Активный транспорт
- •Экзо- и эндоцитоз
- •Системы унипорта, симпорта и антипорта
- •4.3. Строение клеточной стенки грамположительных и грамотрицательных бактерий.
- •5. Пути и механизмы преобразования энергии в живых системах
- •5.1. Метаболизм. Катаболизм и анаболизм
- •Макроэргические соединения
- •Фазы освобождения энергии из питательных веществ
- •Роль высокоэнергетических фосфатов в улавливании энергии. Субстратное и окислительное фосфорилирование
- •Организация дыхательной цепи в митохондриях
- •Механизм сопряжения окисления и фосфорилирования
- •Строение атф-синтазы и синтез атф
- •Коэффициент окислительного фосфорилирования
- •Дыхательный контроль
- •Энергетический обмен и теплопродукция
- •5.4. Фотосинтез и хемосинтез. Фотосинтез
- •Световая стадия фотосинтеза
- •Механизм световой фазы фотосинтеза
- •Темновая фаза фотосинтеза
- •Хемосинтез
- •6. Основные метаболические пути углеводов.
- •6.1. Общая схема превращения глюкозы. Метаболизм глюкозы в печени
- •Энергетический выход аэробного распада глюкозы
- •6.3. Пентозфосфатный путь.
- •Биосинтез глюкозы (глюконеогенез)
- •Субстраты для глюконеогенеза
- •Биосинтез гликогена (гликогенез)
- •Распад гликогена (гликогенолиз)
- •П ревращение в жирные кислоты и холестерол
- •6.4. Брожение.
- •6.5. Биосинтез глюкозы. Обходные пути глюконеогенеза. Биосинтез глюкозы (глюконеогенез)
- •Субстраты для глюконеогенеза
- •Биосинтез гликогена (гликогенез)
- •Распад гликогена (гликогенолиз)
- •П ревращение в жирные кислоты и холестерол
- •6.6. Биосинтез глюкозы из двухуглеродных соединений (глиоксилатный цикл).
- •7. Обмен липидов.
- •7.1. Катаболизм глицерина.
- •Окисление до со2 и образование атф
- •7.3. Биосинтез липидов.
- •8. Обмен белков
- •8.1. Общая схема метаболизма аминокислот. Механизмы транспорта аминокислот в клетку. Метаболизм аминокислот в печени
- •8.2. Дезаминирование аминокислот: окислительное дезаминирование, трансаминирование, непрямое дезаминирование (трансдезаминирование).
- •8.3. Превращения углеродного скелета аминокислот. Кетогенные и гликогенные аминокислоты.
- •8.4. Декарбоксилирование аминокислот. Биогенные амины.
- •8.5. Азотфиксация.
- •8.6. Биосинтез заменимых и незаменимых аминокислот.
- •9. Вторичные метаболиты бактерий и растений
- •Библиография
5. Пути и механизмы преобразования энергии в живых системах
5.1. Метаболизм. Катаболизм и анаболизм
Катаболизм – это процессы распада сложных веществ до более простых, сопровождающееся выделением энергии.
Анаболизм – процессы синтеза сложных молекул из более простых, сопровождающиеся поглощением энергии.
Совокупность всех катаболических и анаболических процессов, протекающих в организме – метаболизм.
5.2. Принципы биоэнергетики. АТФ – основной источник и аккумулятор энергии в организме. Макроэргические соединения. Фазы катаболизма основных питательных веществ в организме. Роль высокоэнергетических фосфатов в улавливании энергии. Субстратное и окислительное фосфорилирование
Принципы биоэнергетики. АТФ – основной источник и аккумулятор энергии в организме
Химическая термодинамика является теоретической основой биоэнергетики. Биоэнергетика занимается изучением энергетических превращений, сопровождающих биохимические реакции. Все эти превращения осуществляются в полном соответствии с первым и вторым началами термодинамики. Тем не менее, живой организм, как объект для термодинамических исследований, отличается целым рядом специфических особенностей в сравнении с системами, которые служат объектами изучения в технической и химической термодинамики. Из этих особенностей наибольшего внимания заслуживают следующие.
Живой организм представляет собой типично открытую систему, непрерывно обменивающуюся с окружающей средой веществом и энергией. В то же время для биологических систем применимо понятие стационарного состояния. В этом состоянии параметры в системе остаются постоянными, а скорость притока веществ и энергии равна скорости удаления их из системы. Такие системы не изменяют своих свойств во времени и сходны с системами, находящимися в равновесии.
Характер изменения энтропии, имеющий решающее значение при оценке процессов в неживых системах, в случае биологических систем имеет лишь подчиненное значение. Ведь все живые организмы высоко организованы и постоянно поддерживают свой уровень организации, поэтому для биологических систем справедливо неравенство Sокр. + Sсист. > 0 , а не Sсист > 0.
Все биохимические процессы, происходящие в клетках в условиях постоянства температуры и давления, при отсутствии значительных перепадов концентраций, резких изменений объема.
Небиологические системы могут совершать работу за счет тепловой энергии, биологические функционируют в изотермическом режиме и для осуществления процессов жизнедеятельности используют химическую энергию.
Стандартное состояние для биологических объектов отличается от стандартного состояния технических и химических систем. Так, стандартным состоянием химической системы является состояние, при котором концентрации всех веществ равны 1 моль/л (или для газов, входящих в систему, парциальные давления равны 1 атм). Для биологических систем это определение остается в силе за исключением концентрации ионов Н+, которая для стандартного состояния принимается равной 10-7 моль/л. Это соответствует нейтральной среде (рН 7), характерной для биологических объектов.
G0 - стандартная энергия Гиббса для химических систем;
G0 - стандартная энергия Гиббса для биологических систем.
Человек получает энергию за счет разложения органических веществ пищи. Органические вещества являются термодинамически нестабильными. Катаболические превращения этих веществ (распад или окисление) протекают с уменьшением свободной энергии. Такие процессы являются самопроизвольными (экзергоническими -G<0) и могут служить источником энергии для функционирования живой клетки. Все процессы, которые идут с увеличением свободной энергии (эндергонические -G>0), несамопроизвольные и должны быть сопряжены с экзергоническими процессами.
Жизненно важные процессы – реакции синтеза (т.е. анаболические процессы), мышечное сокращение, активный транспорт – являются эндергоническими процессами. Эндергонический процесс не может протекать изолированно. Такие процессы получают энергию путем химического сопряжения с реакциями окисления молекул пищевых веществ (катаболическими процессами), которые являются экзергоническими реакциями. Совокупность метаболических и анаболических процессов есть метаболизм.

Схематически такое сопряжение можно проиллюстрировать следующим образом. Пусть превращение метаболита (промежуточного соединения в цепи реакций) А в метаболит В сопровождается выделением свободной энергии. Оно сопряжено с другой реакцией - превращением метаболита С в метаболит D, которое может происходить лишь при поступлении свободной энергии.
Один из возможных механизмов состоит в образовании промежуточного соединения - общего для обеих реакций.
Примером являются дегидрогеназные реакции (реакции отщепления атомов водорода), промежуточным соединением, в которых является промежуточный переносчик атомов водорода.

Еще один пример сопряжения состоит в синтезе в ходе экзергонических реакций высокоэнергетического соединения, общего для многих процессов, и последующего включения этого соединения в эндергонические реакции, что обеспечивает передачу энергии. Таким общим для многих реакций соединением - энергетической валютой клетки - является аденозинтрифосфат (АТФ).
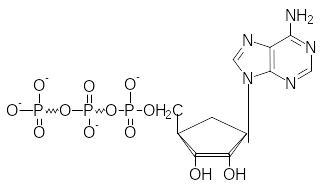
В молекуле АТФ две макроэргические связи, т.е. связи, при гидролизе которых высвобождается энергия. Это позволяет сопрягать большее число экзергонических реакций с большим числом эндергонических.
Главная роль АТФ в организме связана с обеспечением энергией многочисленных биохимических реакций. Являясь носителем двух высокоэнергетических связей, АТФ служит непосредственным источником энергии для множества энергозатратных биохимических и физиологических процессов. Всё это реакции синтеза сложных веществ в организме: осуществление активного переноса молекул через биологические мембраны, в том числе и для создания трансмембранного электрического потенциала; осуществления мышечного сокращения.
В организме АТФ является одним из самых часто обновляемых веществ, так у человека продолжительность жизни одной молекулы АТФ менее 1 мин. В течение суток одна молекула АТФ проходит в среднем 2000—3000 циклов ресинтеза (человеческий организм синтезирует около 40 кг АТФ в день), то есть запаса АТФ в организме практически не создаётся, и для нормальной жизнедеятельности необходимо постоянно синтезировать новые молекулы АТФ.
