
- •Локализованная химическая связь Атомные орбитали
- •Молекулярная орбиталь
- •Методы описания локализованной химической связи
- •Гибридизация
- •Кратные связи
- •Электронная структура молекул. Структуры Льюиса
- •Электроотрицательность
- •Дипольный момент
- •Индуктивный эффект и эффект поля
- •Характеристики связей
- •Типы химических связей
- •Делокализованная химическая связь
- •Правила резонанса
- •Типы молекул с делокализованными связями
- •Ароматичность
- •Резонансный эффект
- •Основы стереохимии Введение
- •Энантиомерия
- •Диастереомерия
- •Динамическая стереохимия
- •Прохиральность
- •Кислоты и основания
- •Теория Бренстеда
- •Кислоты и основания Льюиса
- •Карбокатионы, карбанионы, свободные радикалы, карбены и нитрены
- •Карбокатионы
- •Реакции карбокатионов
- •Влияние различных факторов на устойчивость карбокатионов
- •Карбанионы
- •Реакции карбанионов
- •Свободные радикалы
- •Устойчивость свободных радикалов
- •Карбены
- •Реакции карбенов
- •Нитрены
- •Механизмы реакций и методы их установления
- •Типы механизмов реакций по способу разрыва связей
- •Типы реакций
- •Условия протекания реакций
- •Кинетический и термодинамический контроль реакции
- •Методы установления механизмов реакций
- •Кинетические изотопные эффекты
- •Реакции нуклеофильного замещения
- •Замещение у алифатического атома углерода
- •Механизмы реакций нуклеофильного замещения у алифатического атома углерода
- •Нуклеофильное замещение у аллильного атома углерода
- •Нуклеофильное замещение у тригонального атома углерода
- •Нуклеофильное замещение в ароматических субстратах
- •Влияние различных факторов на реакционную способность в реакциях нуклеофильного замещения
- •Электрофильное замещение
- •Механизмы алифатического электрофильного замещения
- •Важнейшие реакции алифатического электрофильнорго замещения
- •Влияние различных факторов на реакционную способность в реакции se
- •Ароматическое электрофильное замещение
- •Реакционная способность и ориентация в реакциях ароматического электрофильного замещения
- •Соотношение орто- и пара-замещенных продуктов
- •Ориентация в бензольных кольцах, содержащих более одного заместителя
- •Свободнорадикальное замещение
- •Механизмы реакций свободнорадикального замещения
- •Механизмы реакций с ароматическими субстратами
- •Участие соседних групп в свободнорадикальных реакциях
- •Реакционная способность в реакциях радикального замещения
- •Реакции элиминирования
- •Механизмы - элиминирования
- •Ориентация двойной связи
- •Реакционная способность в реакциях элиминирования
- •Пиролитическое элиминирование
- •Ориентация двойной связи при пиролитическом элиминировании
- •Присоединение к кратным связям углерод–углерод
- •Электрофильное присоединение Механизмы электрофильного присоединения
- •Нуклеофильное присоединение
- •Свободнорадикальное присоединение
- •Ориентация и реакционная способность в реакциях присоединения
- •Перециклические реакции
- •Реакции циклоприсоединения
- •Элетроциклические реакции
- •Перегруппировки
- •Нуклеофильные перегруппировки
- •Свободнорадикальные перегруппировки
- •Некоторые важнейшие перегруппировки
- •Сигматропные перегруппировки
- •Метод Мебиуса – Хюккеля
- •Наиболее важные сигматропные перегруппировки
- •Бензидиновая перегруппировка
- •Фотохимия Общие положения
- •Некоторые типы наиболее важных фотохимических реакций
- •Список рекомендуемой литературы
- •Каюков Яков Сергеевич
Динамическая стереохимия
При описании стереохимических особенностей процессов можно различить два типа: стереоспецифичные реакции и стереоселективные реакции.
Стереоспецифичной называется реакция, в которой стереоизомерные исходные вещества при одних и тех же условиях реакции дают стереоизомерные продукты.


Как видно из схемы, исходные вещества в этих стереоспецифичных реакциях представляют собой пары стереоизомеров и продукты также являются стереоизомерами относительно друг друга. Каждая реакция протекает направленно с образованием одного единственного стереоизомера без примеси другого. Пример (1) на схеме являются типичным реакции согласованного син-присоединения по двойной связи в алкенах..
Присоединение дибромкарбена к цис-бутену-2 приводит исключительно к цис-1,1-дибром-2,3-диметилциклопропану, из транс-бутена-2 образуется только транс-1,1-дибром-2,3-диметилциклопропан. Реакции нуклеофильного замещения, протекающие как прямое замещение, сопровождаются обращением конфигурации углеродного атома, связанного с уходящей группой. Так, пример (2) показывает, что при атаке цис-4-метилциклогексил-п-толуолсульфоната тиофенолят-ионом образуется транс-4-метилциклогексилтиофениловый эфир в то время как стереоизомерный транс-п-толуолсульфонат дает цис-тиоэфир.
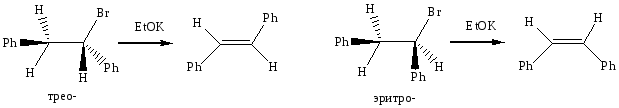
Реакция (3) является примером стереоспецифичного транс-элиминирования алкилгалогенида, в котором переходное состояние требует, чтобы уходящий протон и отрывающийся бромид-ион находились в трансоидном (анти-) положении друг относительно друга. Диастереомерные трео- и эритро-1-бром-1,2-дифенилпропаны подвергаются β-элиминированию, катализируемому основаниями, с образованием стерео-изомерных продуктов.
Стереоселективной называется реакция, в которой один реагент обладает способностью образовывать в определенной реакции два или более стереоизомерных продуктов, но один из них образуется преимущественно.

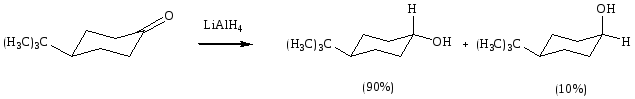

На схеме приведены примеры стереоселективных реакций с различной степенью селективности. При присоединении муравьиной кислоты к норборнену (реакция (3)) в каждой реакции образуется только один стереоизомер, это пример с очень высокой стереоселективностью. Восстановление 4-трет-бутилциклогексанона алюмогидридом лития является типичным для восстановления незатрудненных циклогексанонов, где основным образующимся диастереомером является более устойчивый спирт. Присоединение метилмагнийбромида к 2-фенилпропаналю происходит стереоселективно со среденей степенью селективности; образуется вдвое больше эритро-изомера, чем тpeo-изомера. Селективное образование нового хирального центра с определенной конфигурацией, происходящее в ходе реакции, в которой участвует хиральная молекула, является примером асимметрической индукции. Переходные состояния, ведущие к образованию эритро- и трео-изомеров, являются диастереомерными и имеют различную энергию; следовательно, будет преобладать продукт, соответствующий переходному состоянию с более низкой энергией. Следует также указать, что хотя реакция (1) на схеме написана для присоединения метилмагнийиодида к S-2-фенилпропаналю, идентичные количества диастереомеров будут образовываться и в случае R-2-фенилпропаналя. эритро-Изомер будет также преобладать, и единственное отличие заключается в том, что в случае R-2-фенилпропаналя и эритро-изомер, и образующийся в меньшем количестве трео-изомер будут энантиомерны структурам, приведенным на схеме.
