
- •Локализованная химическая связь Атомные орбитали
- •Молекулярная орбиталь
- •Методы описания локализованной химической связи
- •Гибридизация
- •Кратные связи
- •Электронная структура молекул. Структуры Льюиса
- •Электроотрицательность
- •Дипольный момент
- •Индуктивный эффект и эффект поля
- •Характеристики связей
- •Типы химических связей
- •Делокализованная химическая связь
- •Правила резонанса
- •Типы молекул с делокализованными связями
- •Ароматичность
- •Резонансный эффект
- •Основы стереохимии Введение
- •Энантиомерия
- •Диастереомерия
- •Динамическая стереохимия
- •Прохиральность
- •Кислоты и основания
- •Теория Бренстеда
- •Кислоты и основания Льюиса
- •Карбокатионы, карбанионы, свободные радикалы, карбены и нитрены
- •Карбокатионы
- •Реакции карбокатионов
- •Влияние различных факторов на устойчивость карбокатионов
- •Карбанионы
- •Реакции карбанионов
- •Свободные радикалы
- •Устойчивость свободных радикалов
- •Карбены
- •Реакции карбенов
- •Нитрены
- •Механизмы реакций и методы их установления
- •Типы механизмов реакций по способу разрыва связей
- •Типы реакций
- •Условия протекания реакций
- •Кинетический и термодинамический контроль реакции
- •Методы установления механизмов реакций
- •Кинетические изотопные эффекты
- •Реакции нуклеофильного замещения
- •Замещение у алифатического атома углерода
- •Механизмы реакций нуклеофильного замещения у алифатического атома углерода
- •Нуклеофильное замещение у аллильного атома углерода
- •Нуклеофильное замещение у тригонального атома углерода
- •Нуклеофильное замещение в ароматических субстратах
- •Влияние различных факторов на реакционную способность в реакциях нуклеофильного замещения
- •Электрофильное замещение
- •Механизмы алифатического электрофильного замещения
- •Важнейшие реакции алифатического электрофильнорго замещения
- •Влияние различных факторов на реакционную способность в реакции se
- •Ароматическое электрофильное замещение
- •Реакционная способность и ориентация в реакциях ароматического электрофильного замещения
- •Соотношение орто- и пара-замещенных продуктов
- •Ориентация в бензольных кольцах, содержащих более одного заместителя
- •Свободнорадикальное замещение
- •Механизмы реакций свободнорадикального замещения
- •Механизмы реакций с ароматическими субстратами
- •Участие соседних групп в свободнорадикальных реакциях
- •Реакционная способность в реакциях радикального замещения
- •Реакции элиминирования
- •Механизмы - элиминирования
- •Ориентация двойной связи
- •Реакционная способность в реакциях элиминирования
- •Пиролитическое элиминирование
- •Ориентация двойной связи при пиролитическом элиминировании
- •Присоединение к кратным связям углерод–углерод
- •Электрофильное присоединение Механизмы электрофильного присоединения
- •Нуклеофильное присоединение
- •Свободнорадикальное присоединение
- •Ориентация и реакционная способность в реакциях присоединения
- •Перециклические реакции
- •Реакции циклоприсоединения
- •Элетроциклические реакции
- •Перегруппировки
- •Нуклеофильные перегруппировки
- •Свободнорадикальные перегруппировки
- •Некоторые важнейшие перегруппировки
- •Сигматропные перегруппировки
- •Метод Мебиуса – Хюккеля
- •Наиболее важные сигматропные перегруппировки
- •Бензидиновая перегруппировка
- •Фотохимия Общие положения
- •Некоторые типы наиболее важных фотохимических реакций
- •Список рекомендуемой литературы
- •Каюков Яков Сергеевич
Электрофильное замещение
Для реакций электрофильного замещения SE наиболее характерны такие уходящие группы, которые могут существовать в состоянии с незаполненной валентной оболочкой.
Такой группой может быть протон, но его подвижность зависит от кислотности. В насыщенных алканах водород малоподвижен. Более легко замещение водорода происходит в тех положениях, где он достаточо кислый, это, например, -положение к карбонильной группе, или протон при ацетиленовой связи. Важным типом реакции SE является анионное расщепление, включающее разрыв связи углерод-углерод, при этом уходящей группой является углерод. Особенно склонны к реакциям SE металлорганические соединения.
Механизмы алифатического электрофильного замещения
Механизм алифатического SE в отличие от SN изучен недостаточно. Различают четыре типа механизмов SE: SE1, SE2 (с тыла), SE2 (с фронта), Si. Бимолекулярный механизм SE аналогичен SN2 в том смысле, что новая связь образуется одновременно с разрывом старой. Однако здесь есть существенное различие.
В SN2 нуклеофил подходит со своей электронной парой и, поскольку электронные пары взаимно отталкиваются, он может подходить только с тыла к уходящей электронной паре. В электрофильном замещении вакантная орбиталь может подходить как с тыла, притягивая на себя электронную пару, так и с фронта. Поэтому теоретически рассматривают два возможных механизма.
SE2 (с фронта)
![]()
SE2 (с тыла)
![]()
Существует третий бимолекулярный механизм SE, когда часть молекулы электрофила способствует отделению уходящей группы, образуя с ней связь. Такой механизм называют Si.
![]()
Доказательства: Механизмы SE2 и Si непросто различить. Всем им соответствует кинетика второго порядка. Si и SE2(с фронта) протекают с сохранением конфигурации. SE2(с тыла) протекает с обращением конфигурации. Подтверждением механизма SE2(с фронта) является то, что электрофильное замещение может протекать у атомов углерода в голове моста.
Мономолекулярный механизм электрофильного замещения SE1 аналогичен SN1 и включает две стадии, медленную ионизацию и быструю рекомбинацию.

Доказательства механизма SE1. Одним из доказательств служит кинетика первого порядка по субстрату. Важным является стереохимическое доказательство в реакции:

Обмен протона на дейтерий происходит с той же скоростью, что и рацемизация, и наблюдается кинетический изотопный эффект. Реакция SN1 не происходит в голове моста, а SE1 протекает легко, из чего следует, что карбанион не обязательно должен быть плоским, он может иметь пирамидальное строение.
При проведении электофильного замещения с аллильным субстратом может быть получен продукт перегруппировки:
![]()
Процесс такого типа аналогичен SN и может идти двумя путями.
Первый протекает через образование промежуточного аллильного карбаниона:

Второй путь включает электрофильное присоединение по двойной связи с промежуточным образованием карбокатиона и последующим отщеплением электрофуга:
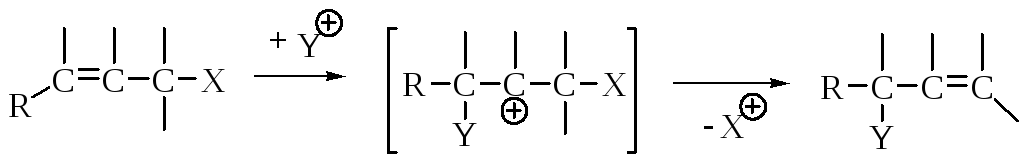
Важнейшие реакции алифатического электрофильнорго замещения
Реакции СН кислот
Если в реакциях электрофильного замещения уходящей группой является водород, отщепляющийся в виде протона, то такие субстраты называются СН-кислотами. Наиболее важные реакции этого типа идущие по механизму SE1:
-Изтопный обмен водорода
 ;
;
-Миграция двойных и тройных связей
![]()

![]()
- Сочетание с солями диазония

В суперкислой среде замещение водорода может идти по механизму SE2, через образование карбониевых ионов:
![]()
Реакции металлорганических соединений
Основные реакции металлорганических соединений - протодеметаллирование, галогендеметаллирование и переметаллирование
Протодеметаллированием называют реакцию замещения металла в металлорганическом соединении на водород под действием кислот
![]()
Галогендеметаллированием называют реакции замещения металла на галоген под действием галогенов или интергалогенов:
![]()
Переметаллированием называют реакцию обмена одного металла на другой. В качестве регента может выступать как неорганическая соль металла, так и металлорганическое соединение:
![]()
Реакции с гетеролитическим разрывом связи углерод-углерод
Ракции протекающие с расщеплением углерод-углеродной связи, называются анионным расщеплением, часто проходят по механизму SE1 с промежуточным образованием карбаниона:

Реакции анионного расщепления условно делят на две группы. К первой группе относят процессы, в которых в качнстве уходящей группы выступают карбонильные соединения. Субстратави этой реакции являются гидроксилсодержащие соединения. Наиболее важные реакции этой группы: ретроальдольная реакция, расщепление циангидринов, расщепление третичных алкоголятов. Вторая группа реакций анионного расщепления носит название ацильного расщепления, так как электрофуг отщепляется в виде карбоновой кислоты или ее производного. Субстратами в этой группе являются карбонильные соединения, а процесс начинается с нуклеофильного присоединения основания к карбонильной группе:

Наиболее важные реакции этого типа: расщепление β-кетоэфиров и β-дикетонов (кислотное расщепление под действием оснований), галоформная реакция, реакции декарбоксилирования солей карбоновых кислот.
