- •Локализованная химическая связь Атомные орбитали
- •Молекулярная орбиталь
- •Методы описания локализованной химической связи
- •Гибридизация
- •Кратные связи
- •Электронная структура молекул. Структуры Льюиса
- •Электроотрицательность
- •Дипольный момент
- •Индуктивный эффект и эффект поля
- •Характеристики связей
- •Типы химических связей
- •Делокализованная химическая связь
- •Правила резонанса
- •Типы молекул с делокализованными связями
- •Ароматичность
- •Резонансный эффект
- •Основы стереохимии Введение
- •Энантиомерия
- •Диастереомерия
- •Динамическая стереохимия
- •Прохиральность
- •Кислоты и основания
- •Теория Бренстеда
- •Кислоты и основания Льюиса
- •Карбокатионы, карбанионы, свободные радикалы, карбены и нитрены
- •Карбокатионы
- •Реакции карбокатионов
- •Влияние различных факторов на устойчивость карбокатионов
- •Карбанионы
- •Реакции карбанионов
- •Свободные радикалы
- •Устойчивость свободных радикалов
- •Карбены
- •Реакции карбенов
- •Нитрены
- •Механизмы реакций и методы их установления
- •Типы механизмов реакций по способу разрыва связей
- •Типы реакций
- •Условия протекания реакций
- •Кинетический и термодинамический контроль реакции
- •Методы установления механизмов реакций
- •Кинетические изотопные эффекты
- •Реакции нуклеофильного замещения
- •Замещение у алифатического атома углерода
- •Механизмы реакций нуклеофильного замещения у алифатического атома углерода
- •Нуклеофильное замещение у аллильного атома углерода
- •Нуклеофильное замещение у тригонального атома углерода
- •Нуклеофильное замещение в ароматических субстратах
- •Влияние различных факторов на реакционную способность в реакциях нуклеофильного замещения
- •Электрофильное замещение
- •Механизмы алифатического электрофильного замещения
- •Важнейшие реакции алифатического электрофильнорго замещения
- •Влияние различных факторов на реакционную способность в реакции se
- •Ароматическое электрофильное замещение
- •Реакционная способность и ориентация в реакциях ароматического электрофильного замещения
- •Соотношение орто- и пара-замещенных продуктов
- •Ориентация в бензольных кольцах, содержащих более одного заместителя
- •Свободнорадикальное замещение
- •Механизмы реакций свободнорадикального замещения
- •Механизмы реакций с ароматическими субстратами
- •Участие соседних групп в свободнорадикальных реакциях
- •Реакционная способность в реакциях радикального замещения
- •Реакции элиминирования
- •Механизмы - элиминирования
- •Ориентация двойной связи
- •Реакционная способность в реакциях элиминирования
- •Пиролитическое элиминирование
- •Ориентация двойной связи при пиролитическом элиминировании
- •Присоединение к кратным связям углерод–углерод
- •Электрофильное присоединение Механизмы электрофильного присоединения
- •Нуклеофильное присоединение
- •Свободнорадикальное присоединение
- •Ориентация и реакционная способность в реакциях присоединения
- •Перециклические реакции
- •Реакции циклоприсоединения
- •Элетроциклические реакции
- •Перегруппировки
- •Нуклеофильные перегруппировки
- •Свободнорадикальные перегруппировки
- •Некоторые важнейшие перегруппировки
- •Сигматропные перегруппировки
- •Метод Мебиуса – Хюккеля
- •Наиболее важные сигматропные перегруппировки
- •Бензидиновая перегруппировка
- •Фотохимия Общие положения
- •Некоторые типы наиболее важных фотохимических реакций
- •Список рекомендуемой литературы
- •Каюков Яков Сергеевич
Влияние различных факторов на устойчивость карбокатионов
1. В случае простых алкильных карбокатионов устойчивость увеличивается в ряду:

Наблюдаемый порядок можно объяснить гиперконъюгацией и эффектом поля.
2. Карбокатионный центр стабилизируется за счет сопряжения с кратной связью. Такой тип стабилизации имеют, например, катионы аллильного типа.

3. Стабилизирующее влияние оказывает фенильная группа. Например, бензильный катион довольно устойчив.
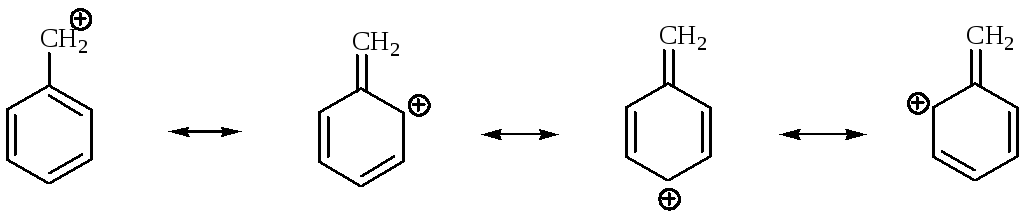
Особенно устойчивы триарилкатионы, способные существовать неограниченно долго в виде твердых солей.
4. Устойчивость повышается за счет других резонансных эффектов. Необычным стабилизирующим действием обладают циклопропановые кольца. Стабилизирующий эффект, вероятно, связан с сопряжением вакантной орбитали карбокатиона с -орбиталью циклопропанового кольца.
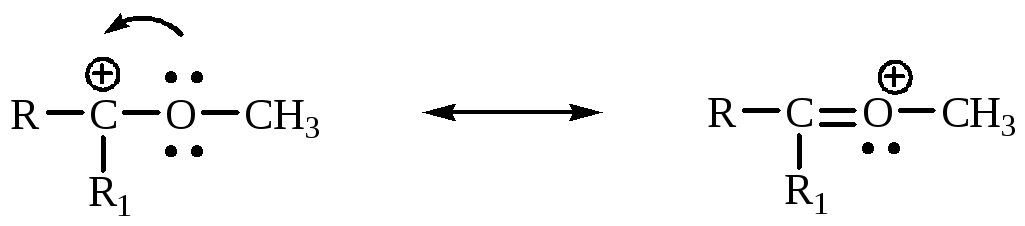
5. Наличие в соседнем положении к карбокатионному центру гетероатома, несущего электронную пару, стабилизирует катион также за счет резонанса.
6. Некоторые карбокатионы устойчивы за счет ароматичности, например, тропилиевый катион.
![]()
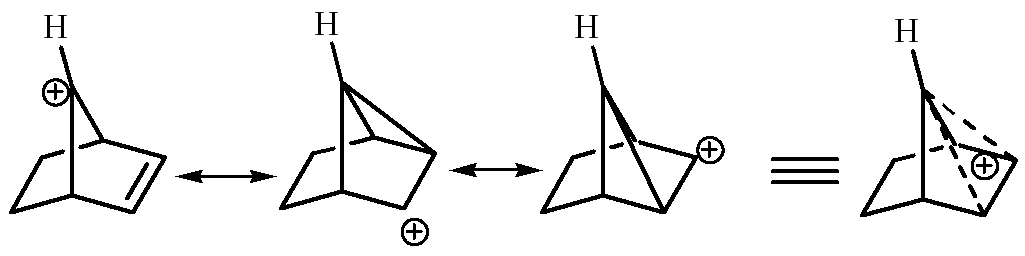
7. Некоторые катионы стабилизируются за счет взаимодействия с кратными связями, положения которых отличны от аллильного. Такие катионы называют неклассическими
Примером служит гомоаллильный катион.
Карбанионы
Методы получения карбанионов
Существует два общих способа генерации карбанионов.
1. Методы, в которых карбанион образуется, когда группа, которая была связана с атомом углерода, уходит без электронной пары. В качестве уходящей группы чаще всего выступает протон.
![]()
Известны и другие уходящие группы:
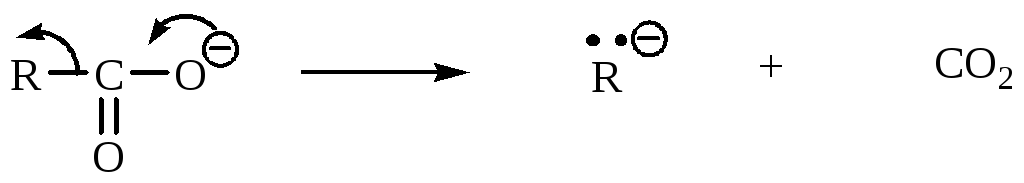
2. Методы, в которых отрицательно заряженный ион присоединяется к кратной связи.
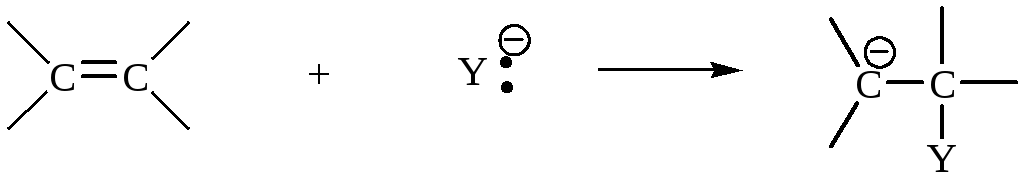
Реакции карбанионов
1. Рекомбинация с положительно заряженным ионом (реакция, обратная получению).
![]()
2. Реакции с насыщенным электрофильным атомом углерода (реакции замещения по механизму SN2).

3. Карбанионы могут присоединяться к кратным связям, образуя новый ион, который не обязательно будет карбанионом.
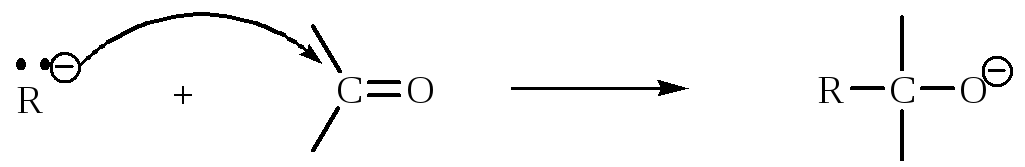
В тех случаях, когда после присоединения образуется карбанион, способный вновь присоединяться к кратной связи, и такой процесс многократно повторяется, имеет место механизм анионной полимеризации алкенов.
4. Реакции перегруппировки. В этих реакциях мигрирующая группа перемещается без электронной пары.
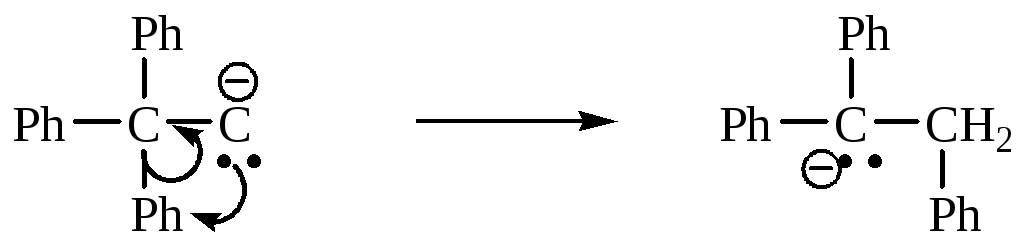
5. Карбанионы могут окисляться до ион-радикалов.
Строение и устойчивость карбанионов
Атом углерода карбанионного центра, вероятнее всего, имеет sp3-гибридизацию и пирамидальное строение. Одним из доказательств этого является то, что анионы легко образуются в вершинах угла каркасных соединений.
В ряду простых алкильных заместителей устойчивость карбанионов обратно пропорциональна устойчивости карбокатионов, что объясняется эффектом поля.
![]()
Многие карбанионы намного более устойчивы, чем алкильные анионы, за счет различных эффектов:
1. Сопряжение электронной пары с кратной связью. Этим объясняется устойчивость аллильного и бензильного анионов. Анионы, в которых карбанионный центр сопряжен с кратной связью С=О или С=N, CN еще более устойчивы.
2. Повышение s-характера неподеленной пары электронов атома углерода определяет возрастание устойчивости карбаниона.

3. Стабилизация атомами серы и фосфора. Если анионный центр находится рядом с атомом S или Р, устойчивость возрастает. Причиной, возможно, является стабилизирующее влияние d-орбиталей.
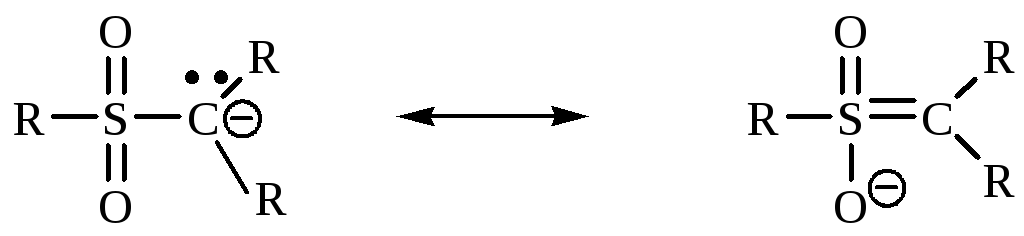
4. Эффект поля. Наиболее заметно влияние полярного эффекта в илидах.
![]()
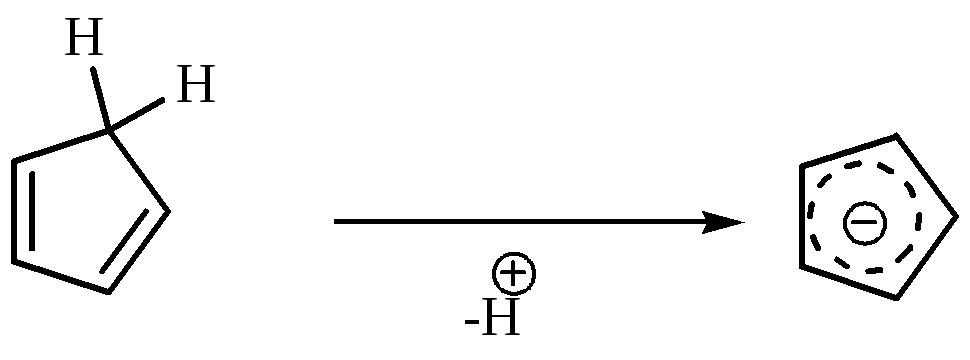
5. Ароматичность. Многие карбанионы устойчивы благодаря ароматичности, например, анион циклопентадиенила.