
- •Локализованная химическая связь Атомные орбитали
- •Молекулярная орбиталь
- •Методы описания локализованной химической связи
- •Гибридизация
- •Кратные связи
- •Электронная структура молекул. Структуры Льюиса
- •Электроотрицательность
- •Дипольный момент
- •Индуктивный эффект и эффект поля
- •Характеристики связей
- •Типы химических связей
- •Делокализованная химическая связь
- •Правила резонанса
- •Типы молекул с делокализованными связями
- •Ароматичность
- •Резонансный эффект
- •Основы стереохимии Введение
- •Энантиомерия
- •Диастереомерия
- •Динамическая стереохимия
- •Прохиральность
- •Кислоты и основания
- •Теория Бренстеда
- •Кислоты и основания Льюиса
- •Карбокатионы, карбанионы, свободные радикалы, карбены и нитрены
- •Карбокатионы
- •Реакции карбокатионов
- •Влияние различных факторов на устойчивость карбокатионов
- •Карбанионы
- •Реакции карбанионов
- •Свободные радикалы
- •Устойчивость свободных радикалов
- •Карбены
- •Реакции карбенов
- •Нитрены
- •Механизмы реакций и методы их установления
- •Типы механизмов реакций по способу разрыва связей
- •Типы реакций
- •Условия протекания реакций
- •Кинетический и термодинамический контроль реакции
- •Методы установления механизмов реакций
- •Кинетические изотопные эффекты
- •Реакции нуклеофильного замещения
- •Замещение у алифатического атома углерода
- •Механизмы реакций нуклеофильного замещения у алифатического атома углерода
- •Нуклеофильное замещение у аллильного атома углерода
- •Нуклеофильное замещение у тригонального атома углерода
- •Нуклеофильное замещение в ароматических субстратах
- •Влияние различных факторов на реакционную способность в реакциях нуклеофильного замещения
- •Электрофильное замещение
- •Механизмы алифатического электрофильного замещения
- •Важнейшие реакции алифатического электрофильнорго замещения
- •Влияние различных факторов на реакционную способность в реакции se
- •Ароматическое электрофильное замещение
- •Реакционная способность и ориентация в реакциях ароматического электрофильного замещения
- •Соотношение орто- и пара-замещенных продуктов
- •Ориентация в бензольных кольцах, содержащих более одного заместителя
- •Свободнорадикальное замещение
- •Механизмы реакций свободнорадикального замещения
- •Механизмы реакций с ароматическими субстратами
- •Участие соседних групп в свободнорадикальных реакциях
- •Реакционная способность в реакциях радикального замещения
- •Реакции элиминирования
- •Механизмы - элиминирования
- •Ориентация двойной связи
- •Реакционная способность в реакциях элиминирования
- •Пиролитическое элиминирование
- •Ориентация двойной связи при пиролитическом элиминировании
- •Присоединение к кратным связям углерод–углерод
- •Электрофильное присоединение Механизмы электрофильного присоединения
- •Нуклеофильное присоединение
- •Свободнорадикальное присоединение
- •Ориентация и реакционная способность в реакциях присоединения
- •Перециклические реакции
- •Реакции циклоприсоединения
- •Элетроциклические реакции
- •Перегруппировки
- •Нуклеофильные перегруппировки
- •Свободнорадикальные перегруппировки
- •Некоторые важнейшие перегруппировки
- •Сигматропные перегруппировки
- •Метод Мебиуса – Хюккеля
- •Наиболее важные сигматропные перегруппировки
- •Бензидиновая перегруппировка
- •Фотохимия Общие положения
- •Некоторые типы наиболее важных фотохимических реакций
- •Список рекомендуемой литературы
- •Каюков Яков Сергеевич
Реакции элиминирования
Реакции элиминирования – выброс малой молекулы из органического субстрата можно классифицировать в соответствии с относительным распоряжением атомов углерода, относительно которых происходит элиминирование:
- элиминирование
![]()
- элиминирование
![]()
- элиминирование
![]()
Механизмы - элиминирования
Различают три основных механизма гетеролитического -элиминирования.
Бимолекулярное элиминирование (Е2)
В реакциях Е2 уходящие группы отщепляются почти одновременно, при этом протон захватывается основанием. Реакция протекает в одну стадию.

Кинетические доказательства протекания реакции по механизму Е2. Поскольку реакция протекает в одну стадию, она должна описываться уравнением второго порядка, первым по субстрату и первым по основанию, что и наблюдается в эксперименте. При замене атома водорода, являющегося уходящей группой на дейтерий, наблюдается ожидаемый изотопный эффект со значением от 3 до 8.
Стереохимические доказательства протекания реакции по механизму Е2. Реакция Е2 стереоспецифична, пять атомов, участвующих в реакции, включая основание, в переходном состоянии должны лежать в одной плоскости. Это может быть достигнуто двумя путями. Группы Н и X могут лежать в транс-положении друг к другу с двугранным углом между ними 180º и в цис-положении с двугранным углом 0º. Первая конформация называется анти-перипланарной, а соответствующее элиминирование анти-элиминированием, вторая конформация называется син-перипланарной и соответствующая ей реакция – син-элиминированием.
При отсутствии определенных эффектов предпочтительнее анти-элиминирование.
Стереоспецифичность реакции Е2 показывает следующий пример:


Мезо-форма должна приводить к цис-изомеру, а (+) или (–) изомеры – к транс-изомеру. Это предположение неоднократно было подтверждено экспериментально. В молекулах, которые не могут принять конформацию с анти-перипланарным расположением уходящих групп, наблюдается син-элиминирование. В тех случаях, когда возможные уходящие группы не могут лежать в одной плоскости, элиминирование по Е2 не должно наблюдаться. Действительно, для таких соединений реакции элиминирования не идут или идут очень медленно.
Например:
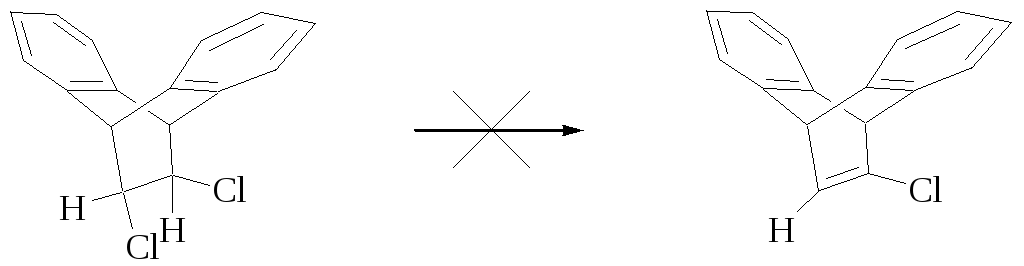
Мономолекулярный механизм (Е1)
Механизм Е1 представляет собой двухстадийный процесс, в котором лимитирующей стадией является ионизация с образованием карбокатиона, который быстро отдает протон основанию, которым часто служит растворитель.

Первая стадия реакции в точности совпадает с первой стадией SN1. Поэтому реакции Е1 и SN1 часто конкурируют друг с другом. Вторая стадия отличается тем, что при SN1 происходит присоединение нуклеофила, а при Е1 – отщепление протона.
Доказательства. Реакция подчиняется уравнению первого порядка (по отношению к субстрату). При добавлении к реакционной смеси сопряженного растворителю основания скорость реакции не увеличивается. При сравнении реакций двух соединений, отличающихся только уходящей группой, например, трет-бутилхлорида и трет-бутилдиметилсульфония, очевидно, что скорости будут различны, но если интермедиат в этих реакциях карбокатион, то он должен претерпевать одинаковые превращения и должен давать одинаковые смеси одинаковых продуктов.
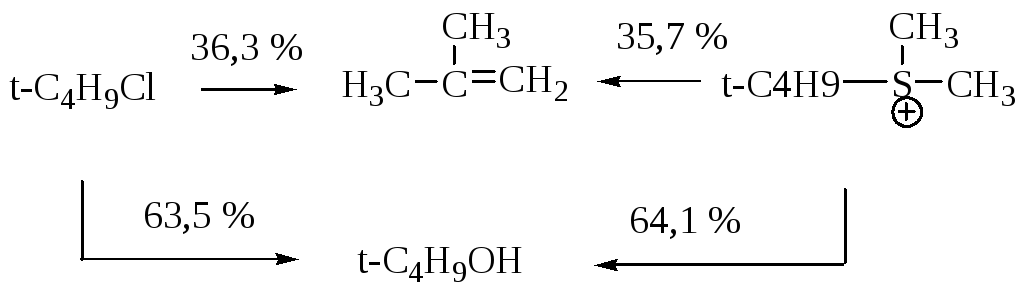
Реакция Е1 не стереоспецифична, т. к. образующийся карбокатион может свободно принимать наиболее устойчивую конфигурацию. Если в качестве интермедиата образуются карбокатионы, можно ожидать перегруппировку. Это часто наблюдается в условиях Е1.
Мономолекулярный анионный механизм (Е1сВ)
Реакция Е1сВ – двустадийный процесс. На первой стадии отщепляется протон и образуется карбанион, на второй стадии происходит отщепление уходящей группы.
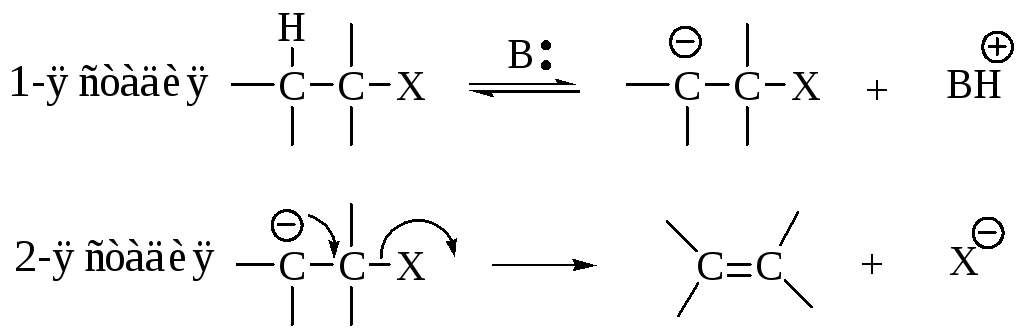
На первой стадии необходимо участие основания.
Доказательства. Первая стадия элиминирования обратима, поэтому, если использовать дейтерированное основание и остановить реакцию до ее завершения, в исходном субстрате, обнаруживается дейтерий.
![]()
![]()
Элекроноакцепторные группы стабилизируют анион и тем самым ускоряют реакцию, так разность в скоростях для субстратов с группами NO2 и COO- достигает 1011.
