
- •Локализованная химическая связь Атомные орбитали
- •Молекулярная орбиталь
- •Методы описания локализованной химической связи
- •Гибридизация
- •Кратные связи
- •Электронная структура молекул. Структуры Льюиса
- •Электроотрицательность
- •Дипольный момент
- •Индуктивный эффект и эффект поля
- •Характеристики связей
- •Типы химических связей
- •Делокализованная химическая связь
- •Правила резонанса
- •Типы молекул с делокализованными связями
- •Ароматичность
- •Резонансный эффект
- •Основы стереохимии Введение
- •Энантиомерия
- •Диастереомерия
- •Динамическая стереохимия
- •Прохиральность
- •Кислоты и основания
- •Теория Бренстеда
- •Кислоты и основания Льюиса
- •Карбокатионы, карбанионы, свободные радикалы, карбены и нитрены
- •Карбокатионы
- •Реакции карбокатионов
- •Влияние различных факторов на устойчивость карбокатионов
- •Карбанионы
- •Реакции карбанионов
- •Свободные радикалы
- •Устойчивость свободных радикалов
- •Карбены
- •Реакции карбенов
- •Нитрены
- •Механизмы реакций и методы их установления
- •Типы механизмов реакций по способу разрыва связей
- •Типы реакций
- •Условия протекания реакций
- •Кинетический и термодинамический контроль реакции
- •Методы установления механизмов реакций
- •Кинетические изотопные эффекты
- •Реакции нуклеофильного замещения
- •Замещение у алифатического атома углерода
- •Механизмы реакций нуклеофильного замещения у алифатического атома углерода
- •Нуклеофильное замещение у аллильного атома углерода
- •Нуклеофильное замещение у тригонального атома углерода
- •Нуклеофильное замещение в ароматических субстратах
- •Влияние различных факторов на реакционную способность в реакциях нуклеофильного замещения
- •Электрофильное замещение
- •Механизмы алифатического электрофильного замещения
- •Важнейшие реакции алифатического электрофильнорго замещения
- •Влияние различных факторов на реакционную способность в реакции se
- •Ароматическое электрофильное замещение
- •Реакционная способность и ориентация в реакциях ароматического электрофильного замещения
- •Соотношение орто- и пара-замещенных продуктов
- •Ориентация в бензольных кольцах, содержащих более одного заместителя
- •Свободнорадикальное замещение
- •Механизмы реакций свободнорадикального замещения
- •Механизмы реакций с ароматическими субстратами
- •Участие соседних групп в свободнорадикальных реакциях
- •Реакционная способность в реакциях радикального замещения
- •Реакции элиминирования
- •Механизмы - элиминирования
- •Ориентация двойной связи
- •Реакционная способность в реакциях элиминирования
- •Пиролитическое элиминирование
- •Ориентация двойной связи при пиролитическом элиминировании
- •Присоединение к кратным связям углерод–углерод
- •Электрофильное присоединение Механизмы электрофильного присоединения
- •Нуклеофильное присоединение
- •Свободнорадикальное присоединение
- •Ориентация и реакционная способность в реакциях присоединения
- •Перециклические реакции
- •Реакции циклоприсоединения
- •Элетроциклические реакции
- •Перегруппировки
- •Нуклеофильные перегруппировки
- •Свободнорадикальные перегруппировки
- •Некоторые важнейшие перегруппировки
- •Сигматропные перегруппировки
- •Метод Мебиуса – Хюккеля
- •Наиболее важные сигматропные перегруппировки
- •Бензидиновая перегруппировка
- •Фотохимия Общие положения
- •Некоторые типы наиболее важных фотохимических реакций
- •Список рекомендуемой литературы
- •Каюков Яков Сергеевич
Свободные радикалы
Способы получения свободных радикалов
Свободные радикалы образуются из молекул в результате гомолитического разрыва связей.
1. Термическое расщепление. При высоких температурах в газовой фазе любая органическая молекула дает свободные радикалы. При энергии связи 20-40 ккал/моль расщепление можно вызвать и в жидкой фазе. Связи с такой энергией имеют, например, азосоединения и ацилпероксиды.
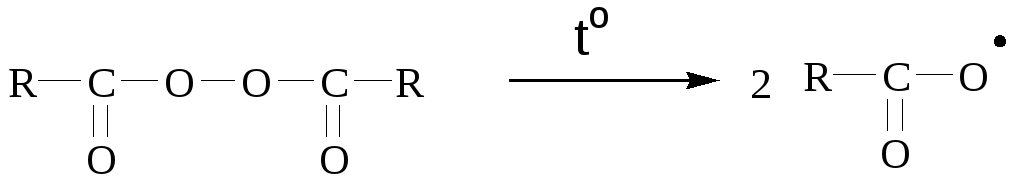
![]()
2. Фотохимическое расщепление. Энергия света с длиной волны от 600 до 300 нм составляет от 48 до 96 ккал/моль, что соответствует энергии ковалентной связи, то есть при действии света на некоторые вещества генерируются радикалы.
![]()

3. Свободные радикалы могут получаться из других свободных радикалов либо при реакции между радикалом и молекулой, либо расщеплением радикала:

Кроме того, радикалы могут быть получены в ходе реакций окисления и восстановления.
Реакции свободных радикалов
При реакциях могут образовываться либо устойчивые продукты (реакции обрыва цепи), либо другие радикалы (реакции роста цепи).
Реакции обрыва цепи:
1. Рекомбинация
![]()
2. Диспропорционирование.
![]()
Реакции роста цепи:
1. Отрыв радикалом атома или группы атомов от нейтральной молекулы
![]()
2.Присоединение радикала к кратной связи.

Образующийся при этом радикал вновь может присоединяться к алкену. Многократное повторение этой реакции - механизм радикальной полимеризации алкенов.
3. Разложение радикалов.
![]()
4. Перегруппировка радикалов.
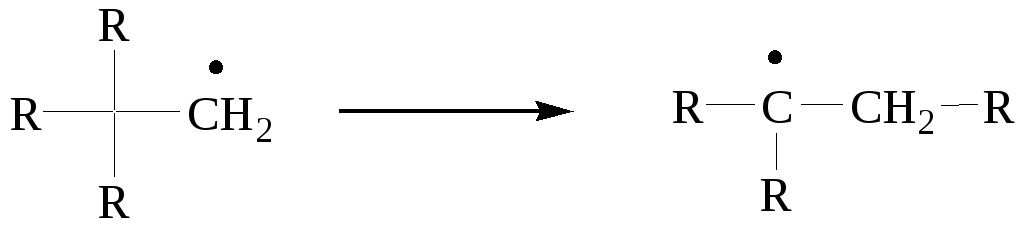
Как правило, перегруппировка направлена на образование более устойчивого радикала.
Устойчивость свободных радикалов
Как и в случае карбокатионов, порядок устойчивости свободных радикалов соответствует ряду:

Данный ряд объясняется гиперконъюгацией

Свободные радикалы, структура которых допускает возможность резонанса, более устойчивы.
Резонансом объясняется устойчивость аллильного и бензильного радикалов.
![]()

Наиболее важным фактором, влияющим на устойчивость радикалов, являются стерические затруднения радикального центра. Например, были синтезированы и изучены соединения А и В. Структура А плоская, допускает стабилизацию резонансом. Структура В не плоская, и она не стабилизирована резонансом. Тем не менее, В намного устойчивее, чем А, что можно объяснить только стерическим эффектом.

Из этого примера видно, что стерические затруднения имеют более важное значение для стабилизации радикалов, чем стабилизация резонансом.
Карбены
Способы получения карбенов
1. -Элиминирование. Отщепление двух атомов или групп от одного атома углерода. Обычно сначала отщепляется группа без электронной пары, чаще всего протон или катион металла, а затем группа с электронной парой.

Типичный пример – образование дихлоркарбена – реализуется при действии на хлороформ оснований
![]()
Другие примеры:
![]()
![]()
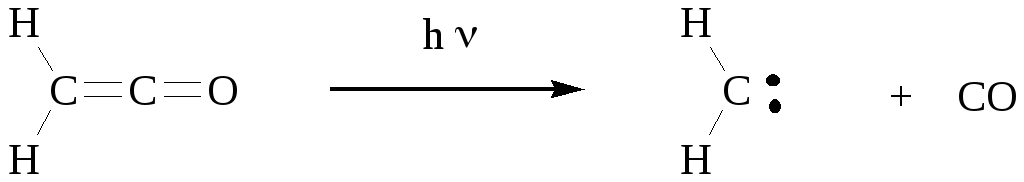
2. Распад некоторых типов двойных связей.

На таких реакциях основаны важнейшие методы получения метилена фотолизом кетена или диазометана.

Из-за высокой реакционной способности карбенов часто бывает трудно доказать, что они действительно существуют. В этих случаях используют нейтральный термин – карбеноид. Карбеноидами часто называют галогензамещенные металлоорганические соединения.
