
- •16. Средняя степень полимеризации крахмала составляет 1800. Средняя относительная молекулярная масса крахмала равна: 241
- •1. Химическая термодинамика. 304
- •2. Строение атома, химическая связь. 304
- •Введение.
- •Тема: Вводное занятие.
- •Техника выполнения лабораторных работ и техника безопасности
- •Первая помощь при ожогах и отравлениях. *
- •Фундаментальные единицы измерения.
- •Лабораторная посуда
- •1. Обозначьте на рисунках:
- •Что из перечисленного выше относится к мерной посуде?
- •Методические указания к занятию № 2.
- •Химический эквивалент.
- •Молярная масса эквивалентов вещества
- •Химическое количество эквивалентов вещества
- •Молярная концентрация эквивалентов вещества
- •Закон эквивалентов
- •1. Примеры расчета молярной концентрации эквивалента (нормальной концентрации).
- •2. Контролирующие задания
- •3. Выполнение индивидуальных заданий.
- •Методические указания к занятию № 3
- •Титриметрический анализ. Общая характеристика метода
- •Требования, предъявляемые к реакциям, которые используют в титриметрии
- •Способы титрования
- •Способы приготовления рабочих растворов
- •Правила работы с мерной посудой при проведении аналитических измерений
- •Мерные колбы
- •Пипетки
- •Бюретки
- •Проведение титрования
- •Методические указания к занятию № 4
- •Кислотно-основное титрование. Общая характеристика метода
- •Определение точки эквивалентности в кислотно-основном титровании. Кислотно-основные индикаторы
- •Титрование сильной кислоты сильным основанием:
- •Титрование слабой кислоты сильным основанием:
- •Титрование слабого основания сильной кислотой:
- •Подбор индикаторов при кислотно-основном титровании
- •Кривые титрования многоосновных (полипротонных) кислот, многокислотных оснований и их солей
- •Применение кислотно-основного титрования
- •Расчет: вычисляют средний объем (V) кислоты, пошедшей на титрование с точностью до сотых мл
- •Методические указания к занятию № 5
- •Редоксиметрия. Общая характеристика и классификация методов
- •Кривые титрования в редоксиметрии
- •Способы определения точки эквивалентности
- •Перманганатометрия
- •Иодометрия
- •Расчет: вычисляют средний объем (V) kMnO4,, пошедший на титрование с точностью до сотых
- •Тесты к теме: Закон эквивалентов. Титриметрия.
- •Учение о растворах. Методические указания к занятию № 6
- •1. Задачи для самостоятельного решения
- •Методические указания к занятию № 7.
- •1. Задачи для самостоятельного решения
- •Тесты к теме: Растворы. Электролитическая диссоциация. Буферные растворы.
- •Методические указания к занятию № 8.
- •Лабораторная работа № 2: Прочность и разрушение комплексных ионов.
- •Тесты к теме: Комплексные соединения.
- •Химическая кинетика и катализ. Методические указания к занятию № 9.
- •1. Задачи для самостоятельного решения
- •Тесты к теме: Скорость химических реакций.
- •Методические указания к занятию № 10.
- •Тесты к теме: Катализ.
- •Электрохимия. Методические указания к занятию № 11.
- •Методические указания к занятию № 12.
- •Тесты к теме: Электрохимия. Электропроводимость растворов.
- •Поверхностные явления. Методические указания к занятию № 13.
- •Методические указания к занятию № 14.
- •Тесты к теме: Поверхностные явления. Адсорбция.
- •Физическая химия дисперсных систем. Методические указания к занятию № 15.
- •Методические указания к занятию № 16.
- •Тесты к теме: Дисперсные системы. Коллоидные растворы.
- •Методические указания к занятию № 17.
- •Тесты к теме: Растворы биополимеров.
- •Химия биогенных элементов. Методические указания к занятию № 18.
- •Общая характеристика биогенных элементов
- •Общая характеристика групп элементов Общая характеристика неметаллов
- •Общая характеристика элементов viiа группы Нахождение в природе
- •Строение атомов галогенов, их физические и химические свойства
- •Биологическая роль элементов viiа группы
- •Общая характеристика элементов viа группы Нахождение в природе
- •Строение атомов, химические и физические свойства халькогенов
- •Биологическая роль элементов viа группы
- •Общая характеристика элементов va группы Нахождение в природе
- •Строение атомов, физические и химические свойства пниктогенов
- •Биологическая роль элементов vа группы
- •Общая харатеристика элементов ivа группы Нахождение в природе
- •Физические и химические свойства элементов iva группы
- •Биологическая роль элементов ivа группы
- •Общая характеристика металлов
- •Общая характеристика элементов iiia группы Нахождение в природе
- •Строение атомов, физические и химические свойства элементов iiia группы
- •Биологическая роль элементов iiia группы
- •Общая характеристика элементов iiа группы Нахождение в природе
- •Общая характеристика элементов iiа группы на основании строения их атомов и положения в таблице д.И. Менделеева
- •Биологическая роль элементов iiа группы
- •Общая харатеристика элементов iа группы Нахождение в природе
- •Общая характеристика щелочных металлов на основании строения их атомов и положения в таблице д.И. Менделеева
- •Физические свойства простых веществ
- •Биологическая роль элементов iа группы
- •Общая харатеристика d-элементов
- •Качественные реакции на важнейшие биогенные элементы
- •1. Химическая термодинамика.
- •2. Строение атома, химическая связь.
- •Химическая термодинамика.
- •Вопросы для подготовки к экзамену по общей химии для лечебного и педиатрического факультетов.
- •Вопросы для подготовки к экзамену по общей химии для медико-психологического факультета.
Кривые титрования в редоксиметрии
При оксидиметрическом титровании вследствие изменения концентраций участвующих в реакции веществ происходит непрерывное изменение окислительно-восстановительного потенциала системы (Е) подобно тому, как при кислотно-основном титровании всё время изменяется рН раствора. В связи с этим кривые титрования в редоксиметрии строят в координатах – величина редокс-потенциала как функция объёма добавленного титранта (рис. 41). Причём значения точек для построения такой кривой титрования можно измерить экспериментально с помощью потенциометрии или рассчитать теоретически по уравнению Нернста.
Как следует из рисунка 41, сперва редокс-потенциал системы при добавлении рабочего раствора изменяется медленно и незначительно, но в области точки эквивалентности при переходе от раствора недотитрованного на 0,1% к перетитрованному на 0,1%, потенциал изменяется резко и скачкообразно. Причём чем больше разность стандартных потенциалов титранта и исследуемого раствора, тем больше скачок титрования.
Для оксидиметрического титрования можно использовать такие окислительно-восстановительные пары, у которых разность их стандартных редокс-потенциалов (∆Е = Е0(окислителя) – Е0(восстановителя)) не меньше 0,4В.
В противном случае отсутствует резкий скачок потенциала вблизи точки эквивалентности.
На величину скачка титрования будут оказывать влияние и все те факторы, от которых зависят значения электродных потенциалов окислителя и восстановителя. Так, например, если в реакции, протекающей при титровании, принимают участие протоны или гидроксильные ионы, то ход кривой титрования станет определяться и значением рН системы.
В то же время, исходные концентрации титруемого вещества и титранта не будут оказывать влияния на вид кривой титрования.
Наличие резкого скачка на кривой титрования позволяет определить точку эквивалентности непосредственно с помощью потенциометрических измерений или использовать для этих целей определённые окислительно-восстановительные (редокс) индикаторы, окраска которых изменяется в зависимости от величины потенциала системы.
Способы определения точки эквивалентности
В редоксиметрии точку эквивалентности можно определить с помощью различных инструментальных методов (например, потенциометрически) либо визуально.
Визуальное обнаружение конечной точки титрования может быть проведено по изменению окраски одного из участников протекающей реакции, либо с помощью индикаторов. Например, в перманганатометрии критерием достижения точки эквивалентности обычно служит появление неисчезающей розовой окраски вследствие добавления к бесцветному титруемому раствору одной лишней капли ярко-малинового раствора KМnO4.
Индикаторы, используемые для определения точки эквивалентности, могут быть специфическими либо окислительно-восстановительными.
Специфические индикаторы реагируют на изменение концентрации одного из участников химической реакции, протекающей при титровании, образуя с ним нестойкое яркоокрашенное соединение.
Оно легко может разрушаться при добавлении второго реагента. Например, в иодометрии для этих целей используют раствор крахмала, образующий с I2 соединение ярко-синего цвета. По исчезновении (в результате расходования I2) или возникновении (при добавлении лишней капли раствора I2) синей окраски судят о достижении точки эквивалентности.
Окислительно-восстановительными, или редокс-индикаторами, называются вещества, которые изменяют свою окраску в зависимости от величины окислительно-восстановительного потенциала системы.
Под действием окислителя или восстановителя в структуре молекулы редокс-индикатора происходят изменения, вызывающие возникновение новой окраски. Таким образом, в растворе редокс-индикатора существует равновесие между его окисленной и восстановленной формами, имеющими разную окраску, которое сдвигается при изменении потенциала системы:
Indox + ne- ↔IndRed
где Indox – окисленная, а IndRed – восстановленная формы индикатора; n – число электронов, принимающих участие при переходе молекулы индикатора из одной формы в другую.
Потенциал такой индикаторной системы может быть рассчитан по уравнению Нернста:
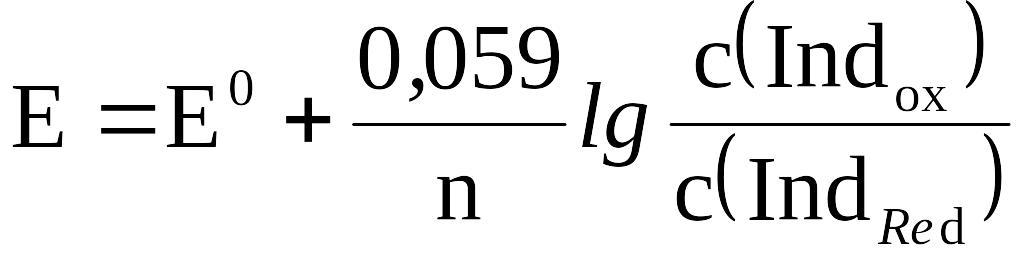
где Е0 – стандартный электродный потенциал, возникающий в системе, когда молярные концентрации окисленной (с(Indox)) и восстановленной (с(IndRed)) форм индикатора будут равны друг другу.
Как и в случае индикаторов других типов, изменение окраски редокс-индикаторов происходит в некотором интервале изменения величины их электродного потенциала. Можно показать, что крайние значения этого интервала определяются соотношением:
![]()
Редокс-индикатор можно использовать в окислительно-восстановительном титровании, если его интервал перехода лежит внутри скачка редокс-потенциала системы на кривой титрования.
Редокс-индикаторы могут быть двухцветными (каждая из его форм имеет свою специфическую окраску) и одноцветными (табл. 22). В первом случае в точке эквивалентности мы наблюдаем переход одной окраски раствора в другую. Во втором случае – исчезновение или возникновение окраски титруемого раствора.
Таблица 22. Некоторые окислительно-восстановительные индикаторы
Индикатор |
Е0, В |
Окраска |
|
Окисленная форма |
Восстановленная форма |
||
Нейтральный красный |
+0,240 |
красная |
нет |
Метиловый синий |
+0,532 |
синяя |
нет |
Дифениламин |
+0,76 |
фиолетовая |
нет |
Эриоглауцин А |
+0,99 |
оранжевая |
жёлтая |
Ферроин |
+1,06 |
бледно-голубая |
красная |
5-Нитроферроин |
+1,25 |
бледно-голубая |
красная |
Редокс-индикаторы бывают обратимыми и необратимыми. Первые могут изменять свою окраску в растворе в зависимости от величины электродного потенциала системы неограниченное число раз. Вторые изменяют свою окраску необратимо, например, при окислении разрушаются с образованием бесцветных продуктов, как индиго под действием гипохлоритов или нафтоловый сине-чёрный под действием ионов BrO3-.
