
- •Все вещества состоят из атомов или молекул
- •Атомы и молекулы веществ находятся в состоянии беспорядочного движения
- •Между атомами и молекулами вещества действуют как силы притяжения, так и силы отталкивания.
- •2. Давление
- •3. Уравнение состояния идеального газа
- •4. Законы идеальных газов
- •Изотермический процесс
- •Изобарический процесс
- •Изохорический процесс
- •Закон Авогадро
- •Закон Дальтона
- •5. Барометрическая формула
- •З акон Больцмана
- •6. Распределение молекул по скоростям
- •7. Функция распределения
- •9. Формула Максвелла
- •10. Средняя арифметическая, средняя квадратичная и наивероятнейшая скорости молекул
- •11. Кинетическая теория теплоты Внутренняя энергия идеального газа
- •12. Первое начало термодинамики
- •§5. Макроскопическая работа
- •13. Различные приложения I начала термодинамики. Теплоёмкость
- •15, 16 Классическая теория теплоёмкости и её недостатки
- •19. Адиабатический процесс. Уравнение Пуассона
- •20. Работа при адиабатическом изменении объёма газа
- •21. Политропический процесс
- •22. Столкновение молекул и явления переноса
- •§2. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- •§3. Рассеяние молекулярного пучка в газе
- •23. Явление переноса в газах. Уравнение переноса
- •24. Диффузия
- •25. Теплопроводность газов
- •26. Вязкость газов (внутреннее трение)
- •28. Неидеальные газы. Уравнение Ван-дер-Ваальса. Отклонение свойств газов от идеальности
- •29. Фаза и фазовые равновесия
- •30. Уравнение Ван-Дер-Ваальса
- •31. Изотермы Ван-дер-Ваальса
- •32. Критическая температура и критическое состояние
- •33. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- •34. Равновесные состояния
- •Обратимые и необратимые процессы
- •35. Необратимость и вероятность
- •37. Внутренняя энергия
- •38. Цикл Карно
- •39. Коэффициент полезного действия в цикле Карно
- •. Холодильная машина
- •40. Свободная энергия
- •41. Энтропия
- •42. Некоторые термодинамические соотношения
- •44 Закон возрастания энтропии. Второе начало термодинамики
- •Увеличение энтропии при теплопередаче
- •45. Энтропия и вероятность
- •46 Энтропия и беспорядок
- •47. Третье начало термодинамики
- •§9. Сжижение газов
- •48. Эффект Джоуля-Томсона
- •50. Строение жидкостей
- •51. Поверхностное натяжение
- •52. Условия равновесия на границе двух сред. Краевой угол
- •53. Силы, возникающие на кривой поверхности жидкости
- •54. Капиллярные явления
- •55. Упругость насыщенного пара над кривой поверхностью жидкости
- •56. Условия равновесия фаз химически однородного вещества
- •§3. Уравнение Клапейрона
З акон Больцмана
Формула (3.37) является барометрической формулой, которая относиться к случаю, когда газ находиться над действием силы тяжести. Величины mgh в (3.37) представляет потенциальную энергию молекулы на высоте h. Можно поэтому сказать, что формула (3.35) даёт число частиц n, энергия которых U=mgh, если число частиц с энергией, равной нулю, равно n0. Очевидно, поведение газа существенно не измениться, если вместо силы тяжести на него будет действовать какая – либо другая сила, а выражение для энергии будет иметь другой вид.
Если газ находиться в каком-нибудь силовом поле, так что частица обладает потенциальной энергией U, то число частиц с такой энергией определится формулой
![]() .
(3.38)
.
(3.38)
Формула (3.38) называется формулой Больцмана. Она позволяет определить долю частиц, которые в условиях теплового равновесия обладают энергией U.
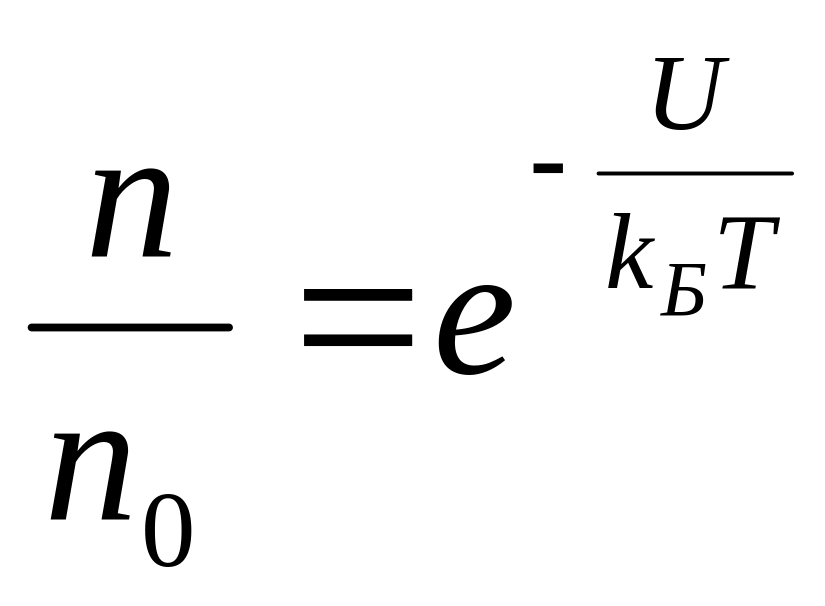
Из
формулы (3.38) видно, что доля
![]() частиц
с данной энергией U
кроме величины этой энергии, зависит
только от температуры.
частиц
с данной энергией U
кроме величины этой энергии, зависит
только от температуры.
При данной температуре, доля молекул обладающих той и иной энергией U, зависит от значения U и быстро уменьшается с ростом U. Это означает доля молекул, обладающих большой энергией всегда очень мала.
6. Распределение молекул по скоростям
Благодаря
хаотичному движению, столкновениям
между собой молекулы обладают разными
скоростями. Об этом свидетельствует и
барометрическая формула. Если бы все
молекулы имели одинаковые скорости,
распределение частиц по высоте было бы
совершенно иным. В действительности,
предположим, что все молекулы находятся
у поверхности земли и имеют одинаковые
скорости с вертикальной составляющей
![]() .
Эти молекулы поднялись бы на высоту
.
Эти молекулы поднялись бы на высоту
![]() ,
определяемую выражением
,
определяемую выражением
![]() ,
,
т.е. до высоты
![]() ,
,
после чего они вернулись бы к Земле с первоначальной кинетической энергией. При таких условиях атмосфера имела бы на высоте резкую границу, за пределами которой ее не было бы. Опыт же показывает, что атмосфера резкой границы не имеет, ее плотность убывает с высотой в соответствии с барометрической формулой и простирается, поэтому практически бесконечно. Предположение о равенстве скоростей всех молекул противоречит, таким образом, опыту.
Следовательно,
молекулы газа имеют различные скорости,
так что среди них имеются как очень
быстрые, так и очень медленные. Несмотря
на полную хаотичность молекулярных
движений, несмотря на случайный характер
столкновений и вызываемых ими изменений
скоростей молекул, их распределение по
скоростям оказывается не случайным, не
произвольным, и вполне определенным.
Необходимо получить закон распределения
молекул по скоростям. Прежде чем
приступить к выводу закона распределения
молекул по скоростям, необходимо
выяснить, что значит распределение
молекул по скоростям. С первого взгляда
определить распределение молекул по
скоростям означает, как будто бы,
определить число молекул, обладающих
той или иной заданной скоростью. Однако
в такой постановке вопрос не имеет
смысла, так как число молекул, имеющих
точно заданную скорость, равна нулю,
поскольку число различных скоростей
бесконечно много, а число молекул
конечно. Поэтому число молекул, приходящих
на долю каждого произвольно заданного
значения скорости, равно нулю. Вследствие
этого вопрос о распределении молекул
по скоростям должен быть сформулирован
следующим образом: сколько
молекул
![]() из общего числа
из общего числа
![]() имеют
скорости
имеют
скорости
![]() в
интервале от
в
интервале от
![]() до
до
![]() .
.
