
- •Все вещества состоят из атомов или молекул
- •Атомы и молекулы веществ находятся в состоянии беспорядочного движения
- •Между атомами и молекулами вещества действуют как силы притяжения, так и силы отталкивания.
- •2. Давление
- •3. Уравнение состояния идеального газа
- •4. Законы идеальных газов
- •Изотермический процесс
- •Изобарический процесс
- •Изохорический процесс
- •Закон Авогадро
- •Закон Дальтона
- •5. Барометрическая формула
- •З акон Больцмана
- •6. Распределение молекул по скоростям
- •7. Функция распределения
- •9. Формула Максвелла
- •10. Средняя арифметическая, средняя квадратичная и наивероятнейшая скорости молекул
- •11. Кинетическая теория теплоты Внутренняя энергия идеального газа
- •12. Первое начало термодинамики
- •§5. Макроскопическая работа
- •13. Различные приложения I начала термодинамики. Теплоёмкость
- •15, 16 Классическая теория теплоёмкости и её недостатки
- •19. Адиабатический процесс. Уравнение Пуассона
- •20. Работа при адиабатическом изменении объёма газа
- •21. Политропический процесс
- •22. Столкновение молекул и явления переноса
- •§2. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- •§3. Рассеяние молекулярного пучка в газе
- •23. Явление переноса в газах. Уравнение переноса
- •24. Диффузия
- •25. Теплопроводность газов
- •26. Вязкость газов (внутреннее трение)
- •28. Неидеальные газы. Уравнение Ван-дер-Ваальса. Отклонение свойств газов от идеальности
- •29. Фаза и фазовые равновесия
- •30. Уравнение Ван-Дер-Ваальса
- •31. Изотермы Ван-дер-Ваальса
- •32. Критическая температура и критическое состояние
- •33. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- •34. Равновесные состояния
- •Обратимые и необратимые процессы
- •35. Необратимость и вероятность
- •37. Внутренняя энергия
- •38. Цикл Карно
- •39. Коэффициент полезного действия в цикле Карно
- •. Холодильная машина
- •40. Свободная энергия
- •41. Энтропия
- •42. Некоторые термодинамические соотношения
- •44 Закон возрастания энтропии. Второе начало термодинамики
- •Увеличение энтропии при теплопередаче
- •45. Энтропия и вероятность
- •46 Энтропия и беспорядок
- •47. Третье начало термодинамики
- •§9. Сжижение газов
- •48. Эффект Джоуля-Томсона
- •50. Строение жидкостей
- •51. Поверхностное натяжение
- •52. Условия равновесия на границе двух сред. Краевой угол
- •53. Силы, возникающие на кривой поверхности жидкости
- •54. Капиллярные явления
- •55. Упругость насыщенного пара над кривой поверхностью жидкости
- •56. Условия равновесия фаз химически однородного вещества
- •§3. Уравнение Клапейрона
19. Адиабатический процесс. Уравнение Пуассона
Процесс, происходящий без подвода и отвода тепла, называется адиабатическим. Применим I закон термодинамики для определения связи между параметрами, определяющими состояние идеального газа, когда газ совершает адиабатический процесс.
Полагая в (1.13) dQ=0, dU=CvdT, получим
CvdT=-PdV (1.23)
К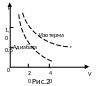 ак
следует из формулы (1.23) при адиабатическом
расширении dV>0,
dT<0,
что значит
температура тела понижается. Наоборот,
при сжатии dV<0,
dT>0
температура тела повышается. Это связано
с тем, что адиабатически расширяющийся
газ совершает работу за счёт собственной
внутренней энергии, поэтому его
температура понижается. Для получения
уравнения адиабатического процесса, в
переменных давление P
и объём V,
необходимо в уравнении (1.23) исключить
температуру T.
Это можно сделать, воспользовавшись
уравнением состояния
ак
следует из формулы (1.23) при адиабатическом
расширении dV>0,
dT<0,
что значит
температура тела понижается. Наоборот,
при сжатии dV<0,
dT>0
температура тела повышается. Это связано
с тем, что адиабатически расширяющийся
газ совершает работу за счёт собственной
внутренней энергии, поэтому его
температура понижается. Для получения
уравнения адиабатического процесса, в
переменных давление P
и объём V,
необходимо в уравнении (1.23) исключить
температуру T.
Это можно сделать, воспользовавшись
уравнением состояния
![]() ,
,
дифференцирование которого даёт
PdV+ VdP=RdT
Откуда
![]() (1.24)
(1.24)
Подставляя это значение dT в (1.23) получим
![]() .
.
После замены R равным ему значением Cp-Cv=R и приведения к общему знаменателю имеем
CVVdP+CpPdV=0.
Обозначим отношение теплоёмкостей
![]()
тогда последнее уравнение принимает вид
![]() .
.
Проинтегрируем это выражение в предположении, что - постоянная величина:
![]() .
.
После интегрирования получим
lnР+lnV=const,
или
![]() =const,
(1.25)
=const,
(1.25)
которое даёт искомое соотношение между давлением и объёмом идеального газа при адиабатическом процессе изменения объёма.
Уравнение (1.25)
называется уравнением Пуассона или
уравнением адиабаты,
![]() - показатель
адиабаты.
- показатель
адиабаты.
Из уравнения Пуассона видно, что в отличие от изотермического процесса, при адиабатическом процессе давление газа меняется обратно не первой степени объёма, а V, причём больше единицы, так как Cp>Cv.
Так как >1, то кривая P=f(V) при адиабатическом процессе, называемая адиабатой, круче изотермы. Более крутое падение давления с увеличением объёма при адиабатном процессе объясняется тем, что при адиабатном расширении идеального газа его давление уменьшается не только за счёт увеличения объёма, но и вследствие происходящего при этом понижения температуры газа.
Нетрудно найти связь другими термодинамическими параметрами газа при адиабатическом процессе. Если мы хотим найти связи между V и T при адиабатическом процессе, то необходимо в уравнении Пуассона (1.25) исключить P, воспользуясь уравнением состояния. Поставив в (1.25)
![]()
получаем
![]() ,
,
или
![]() .
(1.26)
.
(1.26)
Здесь мы учли, что const/R также является постоянной величиной. Если в уравнение (1.25) вместо V поставим его значение
![]() ,
,
то получим
![]() .
.
После преобразования
![]() .
.
Возвысив обе части последнего равенства в степень 1/, получаем
![]() =const
(1.27)
=const
(1.27)
Уравнение (1.27) представляет уравнение адиабатического процесса в переменных P и T.
