
- •Все вещества состоят из атомов или молекул
- •Атомы и молекулы веществ находятся в состоянии беспорядочного движения
- •Между атомами и молекулами вещества действуют как силы притяжения, так и силы отталкивания.
- •2. Давление
- •3. Уравнение состояния идеального газа
- •4. Законы идеальных газов
- •Изотермический процесс
- •Изобарический процесс
- •Изохорический процесс
- •Закон Авогадро
- •Закон Дальтона
- •5. Барометрическая формула
- •З акон Больцмана
- •6. Распределение молекул по скоростям
- •7. Функция распределения
- •9. Формула Максвелла
- •10. Средняя арифметическая, средняя квадратичная и наивероятнейшая скорости молекул
- •11. Кинетическая теория теплоты Внутренняя энергия идеального газа
- •12. Первое начало термодинамики
- •§5. Макроскопическая работа
- •13. Различные приложения I начала термодинамики. Теплоёмкость
- •15, 16 Классическая теория теплоёмкости и её недостатки
- •19. Адиабатический процесс. Уравнение Пуассона
- •20. Работа при адиабатическом изменении объёма газа
- •21. Политропический процесс
- •22. Столкновение молекул и явления переноса
- •§2. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- •§3. Рассеяние молекулярного пучка в газе
- •23. Явление переноса в газах. Уравнение переноса
- •24. Диффузия
- •25. Теплопроводность газов
- •26. Вязкость газов (внутреннее трение)
- •28. Неидеальные газы. Уравнение Ван-дер-Ваальса. Отклонение свойств газов от идеальности
- •29. Фаза и фазовые равновесия
- •30. Уравнение Ван-Дер-Ваальса
- •31. Изотермы Ван-дер-Ваальса
- •32. Критическая температура и критическое состояние
- •33. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- •34. Равновесные состояния
- •Обратимые и необратимые процессы
- •35. Необратимость и вероятность
- •37. Внутренняя энергия
- •38. Цикл Карно
- •39. Коэффициент полезного действия в цикле Карно
- •. Холодильная машина
- •40. Свободная энергия
- •41. Энтропия
- •42. Некоторые термодинамические соотношения
- •44 Закон возрастания энтропии. Второе начало термодинамики
- •Увеличение энтропии при теплопередаче
- •45. Энтропия и вероятность
- •46 Энтропия и беспорядок
- •47. Третье начало термодинамики
- •§9. Сжижение газов
- •48. Эффект Джоуля-Томсона
- •50. Строение жидкостей
- •51. Поверхностное натяжение
- •52. Условия равновесия на границе двух сред. Краевой угол
- •53. Силы, возникающие на кривой поверхности жидкости
- •54. Капиллярные явления
- •55. Упругость насыщенного пара над кривой поверхностью жидкости
- •56. Условия равновесия фаз химически однородного вещества
- •§3. Уравнение Клапейрона
50. Строение жидкостей
Жидкое состояние, занимая промежуточное положение между газом и кристаллами, сочетает в себе некоторые черты обоих этих состояний. В частности, для жидкостей, как и для кристаллических тел, характерно наличие определенного объема, а вместе с тем, жидкость, подобно газу, принимает форму того сосуда, в котором она находится. Известно, что для кристаллического состояния характерно упорядоченное расположение частиц, в газах, наоборот, царит полный хаос. В жидкостях, как показывают рентгенографические исследования, расположение частиц является также промежуточным. В расположении частиц жидкости наблюдается так называемый ближний порядок. Это означает, что по отношению к любой частице расположение ближайших к ней соседей является упорядоченным. Однако по мере удаления от данной частицы расположение по отношению к ней других частиц становится все менее упорядоченным и довольно быстро порядок в расположении частиц полностью исчезает. В кристаллах имеет место дальний порядок - упорядоченное расположение частиц по отношению к любой частице наблюдается в пределах всего объема.
Из-за отсутствия дальнего порядка жидкости (за исключением жидких кристаллов) не обнаруживают анизотропии, характерной для кристаллов с их правильным расположением частиц.
В жидкостях с удлиненными молекулами наблюдается одинаковая ориентация молекул в пределах значительного объема, чем обуславливается анизотропия оптических и некоторых других свойств. Такие жидкости получили название жидких кристаллов. У них упорядочена только ориентация молекул, взаимное же расположение молекул, как и в обычных жидкостях, дальнего порядка не обнаруживают. Из-за того, что в жидкости отсутствует дальний порядок, а молекулы жидкости испытывают значительные силы межмолекулярного взаимодействия, его теория гораздо менее развита, чем теория кристаллического, и, особенно, газообразного состояний.
Значительная заслуга в разработке ряда проблем теории жидкого состояния принадлежит ученому Я.И.Френкелю. Согласно Френкелю, тепловое движение в жидкостях имеет следующий характер. Каждая молекула в течение некоторого времени колеблется около определенного положения равновесия. Время от времени молекула меняет место равновесия, скачком перемещаясь в новое положение, отстоящее от предыдущего на расстоянии порядка размеров молекул. Таким образом, молекулы лишь медленно перемещаются внутри жидкости, пребывая часть времени около определенных мест. Время колебания молекул в этих местах, или так называемое время оседлой жизни зависит от температуры жидкости, резко убывая при повышении температуры. В связи с этим при повышении температуры сильно возрастает подвижность молекул, что, в свою очередь влечет за собой уменьшение вязкости жидкости.
51. Поверхностное натяжение
Поверхность жидкости, соприкасающейся с другой средой (собственным паром, какой-либо другой жидкостью или твердым телом) находится в особых условиях по сравнению с остальной массой жидкости. Возникают эти особые условия потому, что молекулы пограничного слоя жидкости в отличие от молекул в ее глубине окружены молекулами той же жидкости не со всех сторон. Часть соседей поверхностных молекул - это частицы второй среды, с которой жидкость граничит. Эта среда может отличаться от жидкости, как природой, так и плотностью частиц. Имея же разных соседей, молекулы поверхностного слоя и взаимодействуют с ними различным способом. Поэтому силы, действующие на каждую молекулу в этом слое, оказываются неуравновешенными, существует некоторая равнодействующая сила, направленная либо в сторону объема жидкости, либо в сторону объема граничной с ней среды. Вследствие этого перемещение молекулы из поверхностного слоя в глубь жидкости или вглубь среды, с которой она граничит, сопровождается совершением работы. Равнодействующая всех сил, действующих на молекулы внутри жидкости равно нулю, поэтому их перемещение не сопровождается работой. Величина и знак работы совершаемой при перемещении молекул поверхностного слоя зависит от соотношения между силами взаимодействия молекул этого слоя со "своими" же молекулами и с молекулами второй среды. В случае, когда жидкость граничит со своим собственным паром, сила, испытываемая молекулами поверхностного слоя, направлена внутрь жидкости. Это связано с тем, что плотность молекул в жидкости намного больше, чем в насыщенном паре над жидкостью, соответственно, сила притяжения молекулами поверхностного слоя со стороны молекул жидкости больше, чем со стороны молекул пара.
Молекулы поверхностного слоя, перемещаясь во внутрь жидкости, совершают положительную работу. Наоборот, переход молекул из объема жидкости к поверхности сопровождается отрицательной работой, т.е. требует затраты внешней работы. Если поверхность жидкости увеличивается, это значит, что некоторое количество молекул из объема жидкости переходит на поверхность. Для этого надо затратить внешнюю работу. Таким образом, увеличение поверхности жидкости сопровождается отрицательной работой. Наоборот, при сокращении поверхности совершается положительная работа. Если при постоянной температуре обратимым путем изменить поверхность жидкости на бесконечно малую величину , то необходимая для этого работа равна
![]() .
.
Знак
"минус" показывает, что при увеличении
поверхности
![]() совершается
отрицательная работа. Коэффициент
называется коэффициентом поверхностного
натяжения.
совершается
отрицательная работа. Коэффициент
называется коэффициентом поверхностного
натяжения.
Из
сказанного выше следует, что молекулы
поверхностного слоя жидкости обладают
избыточной по сравнению с молекулами,
находящимися в объеме жидкости,
потенциальной энергией
![]() ,
которая измеряется работой, которую
могут совершить молекулы поверхности,
перемещаясь внутрь жидкости под действием
сил притяжения со стороны молекул в
объеме жидкости.
,
которая измеряется работой, которую
могут совершить молекулы поверхности,
перемещаясь внутрь жидкости под действием
сил притяжения со стороны молекул в
объеме жидкости.
Поскольку
энергия
обязана
своим происхождением наличию поверхности
жидкости, то она должна быть пропорциональна
площади
![]() поверхности жидкости
поверхности жидкости
![]() .
(6.1)
.
(6.1)
Т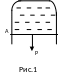 огда
изменение поверхности
повлечет
за собой изменение потенциальной
энергии
огда
изменение поверхности
повлечет
за собой изменение потенциальной
энергии
![]() ,
которая сопровождается работой
,
которая сопровождается работой
![]() .
Если изменение поверхности
происходит
при постоянной температуре, то совершаемая
работа равна изменению свободной энергии
поверхности
.
Если изменение поверхности
происходит
при постоянной температуре, то совершаемая
работа равна изменению свободной энергии
поверхности
![]() .
(6.2)
.
(6.2)
Т
В
Рассмотрим
пример. Если проволочную рамку, одна из
сторон которой подвижна (см. рис.1)
опустить в мыльный раствор, то вся она
затянется пленкой жидкости. Силы
поверхностного натяжения принуждают
пленку сокращаться, и подвижная
перекладина АВ
вслед за пленкой перемещается
вверх. Чтобы сохранить ее в равновесии
к перекладине нужно приложить силу Р
в виде груза. Таким образом, сила
поверхностного натяжения, действующая
в пленке, перпендикулярна к линии АВ,
которая в данном случае и является
линией раздела. Такие же силы действуют
на другие стороны рамки. Но здесь они
уравновешиваются силами притяжения
жидкости к веществу жесткой рамки.
Описанный опыт может быть использован
для определения численного значения
коэффициента поверхностного натяжения
жидкости. Действительно, поверхностная
сила
![]() ,
с учетом того, что пленка имеет две
поверхности, равно при равновесии весу
груза Р,
т.е.
,
с учетом того, что пленка имеет две
поверхности, равно при равновесии весу
груза Р,
т.е.
![]()
или
![]() .
.
Если
под действием этой силы перекладина,
увлекаемая пленкой, переместилась на
расстояние
![]() из
положения АВ,
то работа, совершенная силой равна
из
положения АВ,
то работа, совершенная силой равна
![]() .
Эта работа как видно из (6.2) равно
уменьшению свободной энергии пленки,
которая равна:
.
Эта работа как видно из (6.2) равно
уменьшению свободной энергии пленки,
которая равна:
![]() .
.
В
данном случае
![]() ,
где
,
где
![]() -
длина рамки. Отсюда
-
длина рамки. Отсюда
![]() .
.
Отсюда
![]() .
(6.3)
.
(6.3)
Из (6.3) следует, что коэффициент поверхностного натяжения может быть определен как величина, равная силе, действующей по касательной к поверхности жидкости, приходящейся на единицу длины линии раздела.
