
- •Все вещества состоят из атомов или молекул
- •Атомы и молекулы веществ находятся в состоянии беспорядочного движения
- •Между атомами и молекулами вещества действуют как силы притяжения, так и силы отталкивания.
- •2. Давление
- •3. Уравнение состояния идеального газа
- •4. Законы идеальных газов
- •Изотермический процесс
- •Изобарический процесс
- •Изохорический процесс
- •Закон Авогадро
- •Закон Дальтона
- •5. Барометрическая формула
- •З акон Больцмана
- •6. Распределение молекул по скоростям
- •7. Функция распределения
- •9. Формула Максвелла
- •10. Средняя арифметическая, средняя квадратичная и наивероятнейшая скорости молекул
- •11. Кинетическая теория теплоты Внутренняя энергия идеального газа
- •12. Первое начало термодинамики
- •§5. Макроскопическая работа
- •13. Различные приложения I начала термодинамики. Теплоёмкость
- •15, 16 Классическая теория теплоёмкости и её недостатки
- •19. Адиабатический процесс. Уравнение Пуассона
- •20. Работа при адиабатическом изменении объёма газа
- •21. Политропический процесс
- •22. Столкновение молекул и явления переноса
- •§2. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- •§3. Рассеяние молекулярного пучка в газе
- •23. Явление переноса в газах. Уравнение переноса
- •24. Диффузия
- •25. Теплопроводность газов
- •26. Вязкость газов (внутреннее трение)
- •28. Неидеальные газы. Уравнение Ван-дер-Ваальса. Отклонение свойств газов от идеальности
- •29. Фаза и фазовые равновесия
- •30. Уравнение Ван-Дер-Ваальса
- •31. Изотермы Ван-дер-Ваальса
- •32. Критическая температура и критическое состояние
- •33. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- •34. Равновесные состояния
- •Обратимые и необратимые процессы
- •35. Необратимость и вероятность
- •37. Внутренняя энергия
- •38. Цикл Карно
- •39. Коэффициент полезного действия в цикле Карно
- •. Холодильная машина
- •40. Свободная энергия
- •41. Энтропия
- •42. Некоторые термодинамические соотношения
- •44 Закон возрастания энтропии. Второе начало термодинамики
- •Увеличение энтропии при теплопередаче
- •45. Энтропия и вероятность
- •46 Энтропия и беспорядок
- •47. Третье начало термодинамики
- •§9. Сжижение газов
- •48. Эффект Джоуля-Томсона
- •50. Строение жидкостей
- •51. Поверхностное натяжение
- •52. Условия равновесия на границе двух сред. Краевой угол
- •53. Силы, возникающие на кривой поверхности жидкости
- •54. Капиллярные явления
- •55. Упругость насыщенного пара над кривой поверхностью жидкости
- •56. Условия равновесия фаз химически однородного вещества
- •§3. Уравнение Клапейрона
55. Упругость насыщенного пара над кривой поверхностью жидкости
Испарение жидкости происходит с ее поверхности. Поэтому изменение свойств поверхностного слоя должно изменить условия равновесия между жидкостью и паром над ней. В частности, на условиях равновесия, а значит и на упругости насыщенного пара должна сказаться кривизна поверхности жидкости. Это значит, упругость насыщенного пара над кривой поверхностью должна отличаться от упругости его над плоской поверхностью. Вычислим, насколько упругость насыщенного пара над кривой и плоской поверхностями отличаются друг от друга.
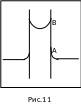
Представим себе замкнутый сосуд с жидкостью, в которую частично погружена капиллярная трубка К, полностью смачиваемая жидкостью (рис.11).
Под действием капиллярных сил жидкость в трубке поднимается на высоту , определяемую формулой
![]() .
(6.18)
.
(6.18)
Упругость пара в точке. В, т.е. над вогнутой поверхностью можно определить, пользуясь барометрической формулой
![]() .
(6.19)
.
(6.19)
Поставив в (6.19) значение из (6.18), получим:
![]() (6.20)
(6.20)
или
![]() .
(6.21)
.
(6.21)
Разложив в (6.20) экспоненту в ряд Тейлора и, ограничиваясь первыми двумя членами разложения, имеем:
![]() .
(6.22)
.
(6.22)
Если учесть, что насыщенный пар подчиняется уравнению состояния идеального газа
![]() ,
,
где
![]() -
плотность насыщенного пара, уравнение
(6.22) можно переписать в виде:
-
плотность насыщенного пара, уравнение
(6.22) можно переписать в виде:
![]() .
(6.23)
.
(6.23)
Таким
образом, упругость насыщенного пара
над вогнутой поверхностью меньше, чем
над плоской на величину
![]() .
Очевидно, что точно таким же образом
можно показать, что над выпуклой
поверхностью упругость насыщенного
пара больше, чем под плоской на ту же
величину
.
Очевидно, что точно таким же образом
можно показать, что над выпуклой
поверхностью упругость насыщенного
пара больше, чем под плоской на ту же
величину
![]() .
.
56. Условия равновесия фаз химически однородного вещества
Условие равновесия
фаз можно получить из теорем термодинамики.
Как уже говорилось, при равновесии
системы температура и давление всех
фаз одинаковые. Если их поддержать
постоянными, то термодинамический
потенциал системы может только убывать.
При равновесии оно принимает минимальное
значение. Этим положением мы и воспользуемся
для вывода условия равновесия фаз. Пусть
![]() -
масса первой фазы,
-
масса первой фазы,
![]() -
масса второй фазы. Обозначим через
-
масса второй фазы. Обозначим через
![]() и
и
![]() удельные
термодинамические потенциалы вещества
в этих фазах. Термодинамический потенциал
всей системы представится в виде
удельные
термодинамические потенциалы вещества
в этих фазах. Термодинамический потенциал
всей системы представится в виде
![]() .
Пусть Р
и Т
системы поддерживаются постоянными.
Тогда при фазовых превращениях величины
и
не будут
изменяться, так как они являются
однозначными функциями только Р
и Т.
Не будет изменяться и полная масса
вещества
.
Пусть Р
и Т
системы поддерживаются постоянными.
Тогда при фазовых превращениях величины
и
не будут
изменяться, так как они являются
однозначными функциями только Р
и Т.
Не будет изменяться и полная масса
вещества
![]() .
Могут изменяться только
.
Могут изменяться только
![]() .
Эти изменения должны происходить в
таком направлении, что термодинамический
потенциал принял наименьшее значение,
возможное в рассматриваемых условиях.
Если
.
Эти изменения должны происходить в
таком направлении, что термодинамический
потенциал принял наименьшее значение,
возможное в рассматриваемых условиях.
Если
![]() ,
то всякое превращение фазы 1 в фазу 2
сопровождается уменьшением
,
то всякое превращение фазы 1 в фазу 2
сопровождается уменьшением
![]() .
Это превращение и будет происходить,
пока вся фаза 1 не перейдет в более
устойчивую фазу 2. Тогда система станет
однофазной, и ее термодинамический
потенциал достигнет минимального
значения
.
Это превращение и будет происходить,
пока вся фаза 1 не перейдет в более
устойчивую фазу 2. Тогда система станет
однофазной, и ее термодинамический
потенциал достигнет минимального
значения
![]() .
Если
.
Если
![]() ,
то фаза 2, в конце концов, превратится в
фазу 1. Только при условии
,
то фаза 2, в конце концов, превратится в
фазу 1. Только при условии
![]() (9.1)
(9.1)
фазы будут находиться в равновесии друг с другом.
Таким образом, условием равновесия фаз является равенство их удельных термодинамических потенциалов.
