
- •Все вещества состоят из атомов или молекул
- •Атомы и молекулы веществ находятся в состоянии беспорядочного движения
- •Между атомами и молекулами вещества действуют как силы притяжения, так и силы отталкивания.
- •2. Давление
- •3. Уравнение состояния идеального газа
- •4. Законы идеальных газов
- •Изотермический процесс
- •Изобарический процесс
- •Изохорический процесс
- •Закон Авогадро
- •Закон Дальтона
- •5. Барометрическая формула
- •З акон Больцмана
- •6. Распределение молекул по скоростям
- •7. Функция распределения
- •9. Формула Максвелла
- •10. Средняя арифметическая, средняя квадратичная и наивероятнейшая скорости молекул
- •11. Кинетическая теория теплоты Внутренняя энергия идеального газа
- •12. Первое начало термодинамики
- •§5. Макроскопическая работа
- •13. Различные приложения I начала термодинамики. Теплоёмкость
- •15, 16 Классическая теория теплоёмкости и её недостатки
- •19. Адиабатический процесс. Уравнение Пуассона
- •20. Работа при адиабатическом изменении объёма газа
- •21. Политропический процесс
- •22. Столкновение молекул и явления переноса
- •§2. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- •§3. Рассеяние молекулярного пучка в газе
- •23. Явление переноса в газах. Уравнение переноса
- •24. Диффузия
- •25. Теплопроводность газов
- •26. Вязкость газов (внутреннее трение)
- •28. Неидеальные газы. Уравнение Ван-дер-Ваальса. Отклонение свойств газов от идеальности
- •29. Фаза и фазовые равновесия
- •30. Уравнение Ван-Дер-Ваальса
- •31. Изотермы Ван-дер-Ваальса
- •32. Критическая температура и критическое состояние
- •33. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- •34. Равновесные состояния
- •Обратимые и необратимые процессы
- •35. Необратимость и вероятность
- •37. Внутренняя энергия
- •38. Цикл Карно
- •39. Коэффициент полезного действия в цикле Карно
- •. Холодильная машина
- •40. Свободная энергия
- •41. Энтропия
- •42. Некоторые термодинамические соотношения
- •44 Закон возрастания энтропии. Второе начало термодинамики
- •Увеличение энтропии при теплопередаче
- •45. Энтропия и вероятность
- •46 Энтропия и беспорядок
- •47. Третье начало термодинамики
- •§9. Сжижение газов
- •48. Эффект Джоуля-Томсона
- •50. Строение жидкостей
- •51. Поверхностное натяжение
- •52. Условия равновесия на границе двух сред. Краевой угол
- •53. Силы, возникающие на кривой поверхности жидкости
- •54. Капиллярные явления
- •55. Упругость насыщенного пара над кривой поверхностью жидкости
- •56. Условия равновесия фаз химически однородного вещества
- •§3. Уравнение Клапейрона
20. Работа при адиабатическом изменении объёма газа
Для получения выражения работы, совершаемой газом при адиабатном расширении, воспользуемся общим выражением работы
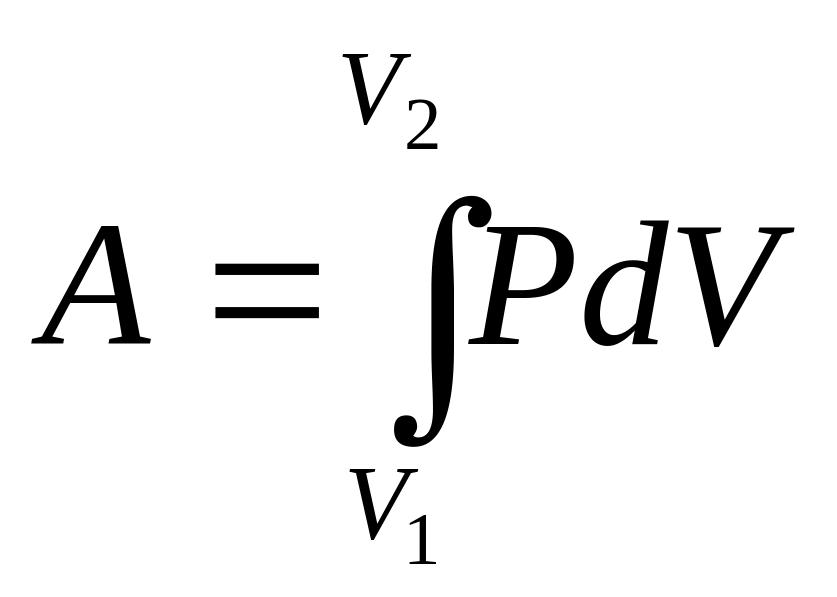 .
.
Связь между давлением газа P и объёмом V определяется уравнением адиабаты(1.25), которые можно написать в таком виде
![]() ,
,
где P1, V1 – соответственные начальные значения давления и объёма. Отсюда
![]() .
.
Подставив это значение P в формулу для работы, получим
 .
.
В свою очередь
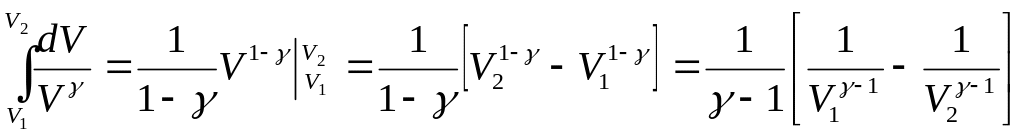 .
.
Тогда выражение для работы A принимает вид
 .
.
Поскольку P1V1=RT1, окончательно имеем
 .
(1.28)
.
(1.28)
Так как крутизна адиабаты намного больше крутизны изотермы, при одинаковых начальных условиях в результате изотермического расширения АВ газ совершает больше работы, чем при адиабатическом расширении AГ.
Э
Г
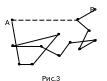 то
следует из рисунка. Работа при адиабатном
расширении газа зависит от значения
показателя адиабаты .
Легко показать, что при 1
формула (1.28) переходит в (1.11). Поскольку
при адиабатическом процессе
то
следует из рисунка. Работа при адиабатном
расширении газа зависит от значения
показателя адиабаты .
Легко показать, что при 1
формула (1.28) переходит в (1.11). Поскольку
при адиабатическом процессе
![]() ,
можем
записать, что
,
можем
записать, что
![]() .
.
21. Политропический процесс
Все процессы, происходящие при постоянном значении теплоёмкости, называются политропическими. В частности, к политропическому процессу относится адиабатический, изотермический, изохорический и изобарический процессы. При политропическом процессе
Q=CdT,
где C - теплоёмкость данного процесса.
Из формулы
![]() следует, что
при адиабатическом процессе C=0,
поскольку дQ=0.
Наоборот, при изотермическом процессе
dT=0,
отсюда C=.
следует, что
при адиабатическом процессе C=0,
поскольку дQ=0.
Наоборот, при изотермическом процессе
dT=0,
отсюда C=.
Нетрудно найти уравнение политропы, т.е. связи между объёмом V и давлением P для идеального газа при данном процессе.
Первое начало термодинамики в случае политропического процесса имеет вид
![]() или
или
![]() .
.
Подставим вместо dT его значение из (1.21) и, заменив R его значением равным CP-CV, получим
![]() .
.
Обозначив
![]() ,
,
где n- показатель политропы, получим
![]() .
.
Решив это дифференциальное уравнение, имеем уравнение политропы в виде
![]() (1.29)
(1.29)
При n= уравнение (1.29) переходит в уравнение адиабатического процесса.
При n=1 (С=) – в уравнение изотермы.
При n=0 (С=CP) – в уравнение изобары.
При n=![]() (С=Cv)
– в уравнение изохоры.
(С=Cv)
– в уравнение изохоры.
Выражение для работы по изменению объёма газа при политропическом процессе аналогично уравнению (1.28) в котором нужно заменить на n.
22. Столкновение молекул и явления переноса
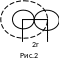 Столкновение
между молекулами играют очень важную
роль во всех процессах, происходящих в
газах. В частности, столкновения молекул
играют важную роль в механизме установления
равновесия газа. Столкновения молекул
являются результатом их взаимодействия.
В общем случае взаимодействия молекул
могут приводить к самым различным
результатам. Молекулы могут отклоняться
от своего прямолинейного движения
(рассеяние), они могут распадаться на
атомы. Мы будем интересоваться только
рассеянием молекул. При рассмотрении
столкновения между молекулами, мы их
будем уподоблять упругим шарикам. В
действительности молекулы являются
сложными системами заряженных частиц,
ядер и электронов, между которыми
действуют силы притяжения и отталкивания,
сложным образом зависящие от расстояния
между молекулами. Во многих случаях
рассеяния для количественной
характеристики процесса вводят понятие
эффективной площади сечения или сечения
рассеяния.
Столкновение
между молекулами играют очень важную
роль во всех процессах, происходящих в
газах. В частности, столкновения молекул
играют важную роль в механизме установления
равновесия газа. Столкновения молекул
являются результатом их взаимодействия.
В общем случае взаимодействия молекул
могут приводить к самым различным
результатам. Молекулы могут отклоняться
от своего прямолинейного движения
(рассеяние), они могут распадаться на
атомы. Мы будем интересоваться только
рассеянием молекул. При рассмотрении
столкновения между молекулами, мы их
будем уподоблять упругим шарикам. В
действительности молекулы являются
сложными системами заряженных частиц,
ядер и электронов, между которыми
действуют силы притяжения и отталкивания,
сложным образом зависящие от расстояния
между молекулами. Во многих случаях
рассеяния для количественной
характеристики процесса вводят понятие
эффективной площади сечения или сечения
рассеяния.
П усть
частица В движется прямолинейно. Положим,
что для того, чтобы произошел тот
или иной из интересующихся нас процессов
при взаимодействии этой частицы с другой
частицей А, эта частица должна пролететь
не дальше, чем расстояние r
(рис.1). Если провести вокруг частицы А
круг радиусом r,
плоскость которого перпендикулярна
направлению движения частицы В,
то произойдет рассеяние частицы В, если
она пройдет через этот круг. Площадь
этого круга
усть
частица В движется прямолинейно. Положим,
что для того, чтобы произошел тот
или иной из интересующихся нас процессов
при взаимодействии этой частицы с другой
частицей А, эта частица должна пролететь
не дальше, чем расстояние r
(рис.1). Если провести вокруг частицы А
круг радиусом r,
плоскость которого перпендикулярна
направлению движения частицы В,
то произойдет рассеяние частицы В, если
она пройдет через этот круг. Площадь
этого круга
![]() и носит название сечения рассеяния
данного процесса.
и носит название сечения рассеяния
данного процесса.
Если
рассмотреть столкновение молекул, как
столкновение твердых шариков радиусом
r,
то сечение рассеяния будет
![]() ,
поскольку рассеяние произойдет только
при непосредственном соприкосновении
молекул (рис.2). В этом случае эффективное
поперечное сечение молекул
,
поскольку рассеяние произойдет только
при непосредственном соприкосновении
молекул (рис.2). В этом случае эффективное
поперечное сечение молекул
![]() в
4 раза больше площади поперечного сечения
молекулы.
в
4 раза больше площади поперечного сечения
молекулы.
