
- •Все вещества состоят из атомов или молекул
- •Атомы и молекулы веществ находятся в состоянии беспорядочного движения
- •Между атомами и молекулами вещества действуют как силы притяжения, так и силы отталкивания.
- •2. Давление
- •3. Уравнение состояния идеального газа
- •4. Законы идеальных газов
- •Изотермический процесс
- •Изобарический процесс
- •Изохорический процесс
- •Закон Авогадро
- •Закон Дальтона
- •5. Барометрическая формула
- •З акон Больцмана
- •6. Распределение молекул по скоростям
- •7. Функция распределения
- •9. Формула Максвелла
- •10. Средняя арифметическая, средняя квадратичная и наивероятнейшая скорости молекул
- •11. Кинетическая теория теплоты Внутренняя энергия идеального газа
- •12. Первое начало термодинамики
- •§5. Макроскопическая работа
- •13. Различные приложения I начала термодинамики. Теплоёмкость
- •15, 16 Классическая теория теплоёмкости и её недостатки
- •19. Адиабатический процесс. Уравнение Пуассона
- •20. Работа при адиабатическом изменении объёма газа
- •21. Политропический процесс
- •22. Столкновение молекул и явления переноса
- •§2. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- •§3. Рассеяние молекулярного пучка в газе
- •23. Явление переноса в газах. Уравнение переноса
- •24. Диффузия
- •25. Теплопроводность газов
- •26. Вязкость газов (внутреннее трение)
- •28. Неидеальные газы. Уравнение Ван-дер-Ваальса. Отклонение свойств газов от идеальности
- •29. Фаза и фазовые равновесия
- •30. Уравнение Ван-Дер-Ваальса
- •31. Изотермы Ван-дер-Ваальса
- •32. Критическая температура и критическое состояние
- •33. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- •34. Равновесные состояния
- •Обратимые и необратимые процессы
- •35. Необратимость и вероятность
- •37. Внутренняя энергия
- •38. Цикл Карно
- •39. Коэффициент полезного действия в цикле Карно
- •. Холодильная машина
- •40. Свободная энергия
- •41. Энтропия
- •42. Некоторые термодинамические соотношения
- •44 Закон возрастания энтропии. Второе начало термодинамики
- •Увеличение энтропии при теплопередаче
- •45. Энтропия и вероятность
- •46 Энтропия и беспорядок
- •47. Третье начало термодинамики
- •§9. Сжижение газов
- •48. Эффект Джоуля-Томсона
- •50. Строение жидкостей
- •51. Поверхностное натяжение
- •52. Условия равновесия на границе двух сред. Краевой угол
- •53. Силы, возникающие на кривой поверхности жидкости
- •54. Капиллярные явления
- •55. Упругость насыщенного пара над кривой поверхностью жидкости
- •56. Условия равновесия фаз химически однородного вещества
- •§3. Уравнение Клапейрона
§3. Рассеяние молекулярного пучка в газе
Со столкновением молекул в газе связано ослабление молекулярного пучка при прохождении через газ.
Пусть некоторое число молекул, обладающих определенной скоростью, величина и направление которой одинакова для всех молекул, проходит через газ. Из-за столкновений с молекулами, часть молекул пучка изменит направление своего движения, и будет выбывать из пучка. По мере продвижения через газ число таких молекул, покинувших пучок, будет возрастать, а число частиц в пучке будет постепенно уменьшаться.
Пусть
пучок движется в газе вдоль оси Х
и в начале его пути при Х=0
число частиц в пучке равно
![]() .
После прохождения отрезка пути
.
После прохождения отрезка пути
![]() ,
число частиц в пучке уменьшится на
некоторую величину
и
станет равным
.
Отношение числа, выбывших из пучка
частиц к числу, оставшихся равно
отношению пройденного пучком пути к
длине свободного пробега
,
так как чем больше это отношение, т.е.
чем больше длин свободного пробега
умещаются в длине
,
тем больше шансов у каждой молекулы
быть отклоненной при столкновении.
Поэтому
,
число частиц в пучке уменьшится на
некоторую величину
и
станет равным
.
Отношение числа, выбывших из пучка
частиц к числу, оставшихся равно
отношению пройденного пучком пути к
длине свободного пробега
,
так как чем больше это отношение, т.е.
чем больше длин свободного пробега
умещаются в длине
,
тем больше шансов у каждой молекулы
быть отклоненной при столкновении.
Поэтому
![]() .
Знак минус указывает, что частиц в пучке
уменьшается. Интегрируя обе части этого
выражения, получим:
.
Знак минус указывает, что частиц в пучке
уменьшается. Интегрируя обе части этого
выражения, получим:
![]() ,
,
где
![]() -
постоянная интегрирования. Ее можно
определить из условия, что при х=0
-
постоянная интегрирования. Ее можно
определить из условия, что при х=0
![]() .
Поэтому
.
Поэтому
![]() .
.
Отсюда
![]() ,
или
,
или
![]() ,
тогда
,
тогда
![]() .
.
Эта формула показывает, что с ростом толщины слоя число частиц в молекулярном пучке уменьшается по экспоненциальному закону.
23. Явление переноса в газах. Уравнение переноса
 Хаотичное
движение газовых молекул ведет к
непрерывному перемешиванию газа. С этим
связано ряд важных явлений, происходящих
в газах. Например, если в разных частях
сосуда с газом плотность газа
Хаотичное
движение газовых молекул ведет к
непрерывному перемешиванию газа. С этим
связано ряд важных явлений, происходящих
в газах. Например, если в разных частях
сосуда с газом плотность газа
![]() различная, то с течением времени она
выравнивается. Точно также два различных
газа, находящихся в соприкосновении
перемешиваются между собой. Эти явление
называются диффузией.
различная, то с течением времени она
выравнивается. Точно также два различных
газа, находящихся в соприкосновении
перемешиваются между собой. Эти явление
называются диффузией.
В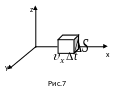 объеме газа, части которого имели
первоначально различные температуры,
происходит постепенное выравнивание
температуры, за счет переноса молекулами
своей энергии
объеме газа, части которого имели
первоначально различные температуры,
происходит постепенное выравнивание
температуры, за счет переноса молекулами
своей энергии
![]() и
обмена энергиями с другими молекулами
при перемешивании. Это явление называется
теплопроводностью. Рассмотрим еще одно
явление. Пусть газ течет вдоль
горизонтальной поверхности
АВ. Ближайший
к поверхности слой имеет меньшую скорость
благодаря трению о поверхность. Скорости
разных слоев газа показаны на рисунке
6. Между слоями газа возникает сила
трения, обусловленная переносом
молекулами из слоя в слой количества
движения
и
обмена энергиями с другими молекулами
при перемешивании. Это явление называется
теплопроводностью. Рассмотрим еще одно
явление. Пусть газ течет вдоль
горизонтальной поверхности
АВ. Ближайший
к поверхности слой имеет меньшую скорость
благодаря трению о поверхность. Скорости
разных слоев газа показаны на рисунке
6. Между слоями газа возникает сила
трения, обусловленная переносом
молекулами из слоя в слой количества
движения
![]() .
Это явление называется внутренним
трением или вязкостью. Благодаря
внутреннему трению газ движется вблизи
поверхности параллельными слоями,
скорости которых убывают в направлении
перпендикулярном к поверхности АВ.
Все перечисленные явления обусловлены
одной причиной - переносом молекулами
газа своих физических характеристик:
массы (диффузия), энергии (теплопроводность),
количество движения (явление внутреннего
трения). Поэтому механизм всех этих
явлений является одинаковым, и все они
объединены под общим названием - явление
переноса.
.
Это явление называется внутренним
трением или вязкостью. Благодаря
внутреннему трению газ движется вблизи
поверхности параллельными слоями,
скорости которых убывают в направлении
перпендикулярном к поверхности АВ.
Все перечисленные явления обусловлены
одной причиной - переносом молекулами
газа своих физических характеристик:
массы (диффузия), энергии (теплопроводность),
количество движения (явление внутреннего
трения). Поэтому механизм всех этих
явлений является одинаковым, и все они
объединены под общим названием - явление
переноса.
Исходя
из молекулярно-кинетической теории,
выведем общее для всех явлений переноса
уравнение переноса. В пространство, где
находится газ с концентрацией![]() ,
введем декартовую систему координат
(рис.7).
,
введем декартовую систему координат
(рис.7).
Перпендикулярно
оси Х
поместим поверхность площадью
![]() .
Определим количество молекул,
проходящих через эту поверхность за
время
.
Определим количество молекул,
проходящих через эту поверхность за
время
![]() .
.
Рис.7![]() через
пройдут
через
пройдут
![]() часть
всех молекул, находящихся внутри
параллелепипеда с основанием
и
высотой
часть
всех молекул, находящихся внутри
параллелепипеда с основанием
и
высотой
![]() .
Число таких молекул будет равно
.
Число таких молекул будет равно
![]() .
.
Эти
молекулы переносят через площадку
значения своих характеристик
![]() (масса,
энергия, количество движения). Тогда
количество физических характеристик,
перенесенных молекулами в одном
направлении через
(масса,
энергия, количество движения). Тогда
количество физических характеристик,
перенесенных молекулами в одном
направлении через
![]() за
время
определится
выражением:
за
время
определится
выражением:
![]() .
.
Такое же количество физической характеристики будет перенесено и в обратном направлении, т.е. поток физической характеристики через будет равным нулю.
П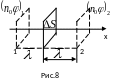 редположим,
что рассматриваемый газ неоднороден
по своим свойствам, т.е.
различно
в разных местах объема, а сами молекулы
имеют неодинаковые значения
.
Тогда
редположим,
что рассматриваемый газ неоднороден
по своим свойствам, т.е.
различно
в разных местах объема, а сами молекулы
имеют неодинаковые значения
.
Тогда
![]() будет
также различным в разных местах объема
газа. Пусть
будет
также различным в разных местах объема
газа. Пусть
![]() убывает
в положительном направлении оси Х.
убывает
в положительном направлении оси Х.
Выберем
две площади, находящиеся на одинаковых
расстояниях от площади
,
равных длине свободного пробега
(Рис.8).
Тогда
![]() будет
связано переносом физической характеристики
по направлению оси Х.
будет
связано переносом физической характеристики
по направлению оси Х.
Такой
же поток физической характеристики
![]() в
направлении оси Х
будет и через площадь
,
так как эти площади находятся на
расстоянии длины свободного пробега,
и в этом промежутке обмен значениями
и
изменение
не
происходит, поскольку молекулы не
испытывают столкновения. Также рассуждая,
можно предположить, что через площадь
в
обратном направлении оси Х,
будет поток физической характеристики
в
направлении оси Х
будет и через площадь
,
так как эти площади находятся на
расстоянии длины свободного пробега,
и в этом промежутке обмен значениями
и
изменение
не
происходит, поскольку молекулы не
испытывают столкновения. Также рассуждая,
можно предположить, что через площадь
в
обратном направлении оси Х,
будет поток физической характеристики
![]() ,
причем
>
.
Тогда результирующий поток физической
характеристики через
будет
равным:
,
причем
>
.
Тогда результирующий поток физической
характеристики через
будет
равным:
![]() .
.
Разделив
и умножив правую часть полученного
выражения на
![]() ,
перепишем в виде:
,
перепишем в виде:
![]() .
.
Поскольку
![]() представляет
изменение
на
единицу длины, мы можем переписать
выражение для
представляет
изменение
на
единицу длины, мы можем переписать
выражение для
![]() в
виде:
в
виде:
![]() .
(4.3)
.
(4.3)
Полученное
выражение представляет уравнение
переноса. Знак (-) обусловлен тем, что
перенос физической величины происходит
в направлении противоположном
![]() ,
определяет
направление максимального роста
.
,
определяет
направление максимального роста
.
