
- •Модуль № 3. Молекулярна біологія. Біохімія гормонів і фізіологічних функцій. Тематичний план практичних занять з модуля 3
- •Завдання для самостійної роботи студентів (срс)
- •Модуль № 3. Молекулярна біологія. Біохімія гормонів і фізіологічних функцій. Змістовий модуль 12. Основи молекулярної біології.
- •Теоретичні питання
- •Практична робота
- •Дослід 2. Кількісне визначення сечової кислоти в сечі.
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •1. У сечі місячної дитини виявлено підвищений вміст оротової кислоти. Дитина погано набирає вагу. Які речовини потрібно використати для нормалізації метаболізму?
- •Індивідуальна самостійна робота студентів
- •Література
- •Змістовий модуль 13. Основи молекулярної генетики.
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Індивідуальна самостійна робота студентів
- •Література
- •Змістовий модуль 14. Молекулярні механізми дії гормонів білкової природи на клітини-мішені. Регуляція метаболізму.
- •Тема 3. Дослідження молекулярно-клітинних механізмів дії гормонів білкової природи на клітини-мішені.
- •Теоретичні питання
- •Практична робота і. Якісні реакції на інсулін.
- •Іі. Якісні та кількісні реакції на адреналін.
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Змістовий модуль 15. Молекулярні механізми дії стероїдних і тиреоїдних гормонів, їх участь у регуляції метаболізму.
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •А. Кортизолу
- •А Тироксин і трийодтиронін
- •Приклади тестів “Крок-1”
- •Глутамату
- •Індивідуальна самостійна робота студентів
- •Література
- •Змістовий модуль 16. Біохімія харчування людини. Вітаміни як компоненти харчування. Тема № 5. Дослідження біохімічного складу та функцій слини.
- •Теоретичні питання
- •Практична робота
- •Питання контролю виконання практичної роботи
- •Приклади тестів “Крок – 1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Дослід № 3 Бензидинова проба на кров.
- •Контроль виконання лабораторної роботи
- •B. Дегідрогеназа
- •Реакцію Уффельмана
- •Приклади тестів “Крок – 1”
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література Основна:
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література Основна:
- •Змістовий модуль 17. Біохімія та патобіохімія крові.
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •5. Як за вмістом залишкового азоту крові та загального азоту сечі диференціювати ретенційну і продукційну азотемії? Приклади тестів „Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок – 1”
- •Індивідуальна самостійна робота студентів
- •Література Основна:
- •Змістовий модуль 18. Функціональна та клінічна біохімія органів і тканин.
- •Конкретні завдання.
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Дослід 2. Кількісне визначення кальцію комплексонометричним методом.
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок – 1”
- •Література Основна:
- •Теоретичні питання
- •Практична робота Дослід 1. Виявлення білка у тканинах зуба.
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •C. Тиреокальцитоніну
- •Література:
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •D. Посилений розпад м’язових білків
- •Література
- •Перелік теоретичних питань до підсумкового модульного контролю № 3
- •Перелік практичних навичок до підсумкового модульного контролю № 3
Теоретичні питання
Гормони: загальна характеристика; роль гормонів та інших біорегуляторів у системі міжклітинної інтеграції функцій організму людини.
Класифікація гормонів та біорегуляторів; відповідність структури та механізмів дії гормонів.
Реакція клітин-мішеней на дію гормонів. Мембранні (іонотропні, метаботропні) та цитозольні рецептори.
Біохімічні системи внутрішньоклітинної передачі гормональних сигналів: G-білки, вторинні посередники (цАМФ, Ca2+/кальмодулін, ІФ3, ДАГ, протеїнкінази С, А), їх роль.
Гормони гіпоталамуса – ліберини та статини. Функціональний зв'язок між гіпоталамусом і гіпофізом.
Гормони передньої частки гіпофіза: соматотропін (СТГ), пролактин. Патологічні процеси, пов’язані з порушенням функції цих гормонів.
Гормони задньої частки гіпофіза. Вазопресин та окситоцин: будова, біологічні функції.
Гормони підшлункової залози. Інсулін – будова, біосинтез та секреція; вплив на обмін вуглеводів, ліпідів, амінокислот та білків. Рістстимулівні ефекти інсуліну.
Глюкагон. Хімічна природа та біологічна дія гормону.
Катехоламіни (адреналін, норадреналін, дофамін): будова, біосинтез, біологічні ефекти, біохімічні механізми дії.
Практична робота і. Якісні реакції на інсулін.
Дослід 1. Біуретова реакція.
Принцип методу. За хімічною природою інсулін – простий білок, який у лужному середовищі реагує з купруму сульфатом, при цьому утворюються сполуки, забарвлені у фіолетовий колір.
Матеріальне забезпечення: 10 % розчин NaOH, СuSO4, інсулін.
Хід роботи. До 10 крапель інсуліну додають 5 крапель 10 % розчину NaOH і краплю розчину CuSO4. Рідина забарвлюється у фіолетовий колір.
Зробити висновок.
Дослід 2. Реакція Фоля.
Принцип методу. Сірковмісні амінокислоти, особливо цистеїн і цистин, при кип’ятінні з лугом втрачають сірку, яка відщеплюється у вигляді сірководню. Сірководень, взаємодіючи з лугом, утворює сульфіди, які можна виявити при додаванні плюмбуму ацетату (реактиву Фоля). Сульфіди утворюють з ним коричневий або чорний осад плюмбуму сульфіду.
Матеріальне забезпечення: реактив Фоля, інсулін.
Хід роботи. До 5 крапель інсуліну додають 5 крапель реактиву Фоля і кип’ятять. Через 1 – 2 хвилини після відстоювання утворюється бурий або чорний осад сульфіду свинцю.
Зробити висновок.
Іі. Якісні та кількісні реакції на адреналін.
Дослід 3. Реакція з хлорним залізом.
Принцип методу. Адреналін легко окиснюється на повітрі з утворенням адренохрому, який дає смарагдово-зелене забарвлення із феруму хлоридом.
Матеріальне забезпечення: хлорне залізо, аміак, адреналін.
Хід роботи. До 3 крапель розчину адреналіну додають 1 краплю розчину хлорного заліза. Рідина забарвлюється в смарагдово-зелений колір. Якщо додати аміак, спостерігається зміна забарвлення на червоне, а потім – коричневе.
Зробити висновок.
Дослід 4. Кількісне визначення адреналіну (за Фоліним).
Принцип методу. Метод ґрунтується на колориметричному визначенні інтенсивності забарвлення, яке утворюється при взаємодії адреналіну з реактивом Фоліна.
Матеріальне забезпечення: досліджуваний розчин адреналіну, 10 % розчин вуглекислого натрію, реактив Фоліна, стандартний розчин адреналіну.
Хід роботи. У суху пробірку вносять 1 мл досліджуваного розчину адреналіну і до нього додають 4 мл 10 % р-ну NaHCO3 і 0,5 мл реактиву Фоліна. Вміст пробірки струшують. Через 5 хв інтенсивність отриманого синього забарвлення вимірюють на калориметрі з червоним світофільтром проти контрольної проби, яка містить замість розчину адреналіну 1 мл дистильованої води, 4 мл 10 % NaHCO3 і 0,5 мл реактиву Фоліна. Знаючи оптичну густину досліджуваного розчину, за калібрувальним графіком знаходимо концентрацію адреналіну в грамах на літр.
Побудова калібрувального графіка. У мірну колбу об’ємом 25 мл додають 1 мл адреналіну і доводять до мітки водою. 1 мл такого розчину містить 0,04 мг адреналіну. Основний розчин розводять в 2 і 4 рази та отримують відповідно розчини з концентрацією адреналіну 0,02 і 0,01 г/л. В три пробірки додають по 1 мл розчину адреналіну (0,01, 0,02 і 0,04 г/л), а в четверту пробірку – 1 мл дист. води і виконують хід роботи. Отримавши відповідні оптичні густини кожної концентрації, будують калібрувальний графік. На осі абсцис відкладають значення концентрації стандартних розчинів адреналіну, на осі ординат – оптичну густину відповідно до цих концентрацій.
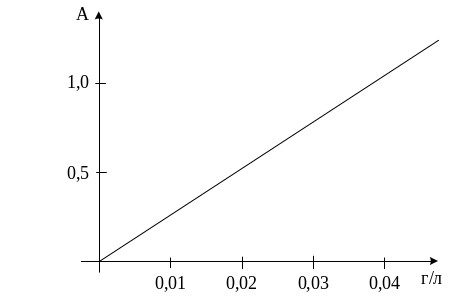
Зробити висновок.
Клініко-діагностичне значення. Вивчення метаболізму гормонів і медіаторів має велике значення для діагностики ендокринних розладів, а також оцінки функціонального стану організму при багатьох інших формах патології, які пов’язані з порушенням центральної, вегетативної нервової систем, серця, печінки, нирок і інших паренхіматозних органів.
Будь-які порушення в системі гіпоталамус-гіпофіз-кора надниркових залоз безпосередньо приводять до зміни продукції гормонів надниркових залоз. За умов норми концентрація адреналіну в плазмі крові становить 112 – 658 пг/мл; норадреналіну — менше 10 пг/мл. Підвищується екскреція адреналіну при артеріальній гіпертензії, феохромоцитомі, в гострий період інфаркту міокарда, нападах стенокардії, інфекційних захворюваннях. Знижений вміст адреналіну спостерігають при колагенозах, гострих лейкозах, ураженні гіпоталамуса, міастенії, синдромі Іценка-Кушінга тощо. Паління, фізичне навантаження, емоційний стрес викликають екскрецію катехоламінів із сечею. Збільшення екскреції катехоламінів спостерігають при гепатитних цирозах печінки, загостренні виразкової хвороби шлунка і 12-палої кишки. Порушення екскреції спостерігають в патогенезі уремії.
