
- •Химический состав и строение молекулы воды.
- •Водородные взаимодействия.
- •Агрегатные состояния воды.
- •Аномалии воды.
- •Химические свойства воды.
- •Свойства растворов
- •6. Физико-химические свойства растворов неэлектролитов и электролитов.
- •7. Свойства растворов слабых электролитов.
- •Ионные равновесия
- •8. Растворимость веществ в воде.
- •10. Диссоциация воды.
- •11. Ионное произведение воды
- •12. Буферные растворы и их свойства
- •13. Гидролиз солей
- •14. Количественные характеристики гидролиза
- •15. Понятие о системах, фазах, компонентах.
- •16. Диаграмма состояния воды
- •17. Окислители и восстановители
- •18. Типы окислительно-восстановительных реакций
- •19. Окислительно-восстановительные потенциалы
- •20. Окислительно-восстановительные свойства воды
- •Классификация дисперсных систем.
- •Методы получения дисперсных систем.
- •Строение коллоидной частицы.
- •Свойства коллоидных систем.
- •Электрокинетические явления.
- •26.Причины устойчивости коллоидных систем
- •27. Разрушение дисперсных систем
- •28. Поверхностное натяжение
- •29. Поверхностно активные вещества
- •Поверхностные явления
- •30. Адсорбция равновесия
- •34 Особенности химического состава природных вод
- •36. Понятие об обобщённых оценочных показателях качества воды.
- •37. Химические показатели качества воды
- •40. Отстаивание.
- •41. Осаждение
- •42. Фильтрование воды
- •43. Флотация и электрофлотация
- •44. Коагуляция
- •45. Зависимость выбора оптимальных условий обработки различными коагулянтами от качества воды
- •46. Электрокоагуляция, эффективность использования
- •47. Флокулянты (анионо- и катионоактивные) их природа, свойства и методы действия, выбор оптимальной дозы.
- •48. Хлорирование: хлорирующие реагенты; механизм обеззараживающего действия, хлороёмкость воды в отсутствии и присутствии солевого аммиака.
- •56. Жесткость воды
- •57. Единицы измерения жесткости
- •58. Методы реагентного умягчения воды, их эффективность, контроль процессов реагентного умягчения.
- •59. Умягчения воды методом ионного обмена
- •60. Иониты (катиониты и аниониты), их природа, строение, свойства.
- •61. Термический метод умягчения воды.
- •62. Импфирование (подкисление)
- •63. Опреснение воды
- •64. Электрохимический метод.
- •66. Методы удаления из воды соединений железа и марганца
- •67.Удаление кремниевой кислоты
- •68.Обесфторирование и фторирование воды.
- •69. Не нашли этот вопрос
- •70. Углекислота и ее формы.
- •71. Вычисление содержания агрессивной углекислоты с помощью таблицы
- •72. Индекс насыщения воды карбонатом кальция
- •73. Особенности химического состава бытовых и производственных сточных вод
- •75Отстаивание, удаление масел и нефти
- •76.Коагулирование сточных вод.77.Выбор и подготовка коагулянтов.
- •78) Флотация сточных вод.
- •79) Сорбция.
- •80) Сорбция – область использования, факторы, влияющие на выбор сорбентов.
- •81) Экстракция, требования, предъявляемые к экстрагентам, экстракция в противотоке.
- •82.Эвапорация и аэрация.
- •83. Области использования аэрации и эвапорации, контроль процессов.
- •85. Нейтрализация сточных вод
- •84. Радиационнаяочистка сточных вод от органических загрязнений.
- •87.Химич очистка сточных вод
- •86.Дезинфекция сточных вод
- •88.Химическое окисление под давлением
- •89.Кристаллизация.
34 Особенности химического состава природных вод
При формировании состава природных вод происходит взаимодействие с окружающей средой (почва, атмосфера, горные породы), при этом протекают следующие процессы: растворение соединений, химическое взаимодействие с водой и водными растворами, биохимические реакции, калоидно – химические взаимодействия.
Действие каждого процесса в свою очередь определяются следующими условиями: температура, давление, геологические особенности
Природные воды квалифицируют:
-по происхождению различают: атмосферные воды (осадочные), подземные воды (ключевые и колодезные), и поверхностные воды (речные, озерные, морские, болотные).
-по классификации Вернадского выделено 485 видов вод с учетом солесодержания, преобладающего иона или группы ионов, соотношение между группами наличие специфических компонентов.
-по солесодержанию: пресные воды до 1 г/кг; солоноватые 0т1 до 25 г/кг; соленые больше 50 г/кг; с морской соленостью от 25 до 50 г/кг
- по согласно классификации О.А. Алекин природные воды
по преобладающему аниону делятся на 3 класса:
1) карбонатный или гидрокарбонатный (С);
2) сульфатный (S);
3) хлорные(Cl);
по преобладающему катиону классы делятся на группы:
1) кальциевая (Са);
2)магниевая(Mg);
3)натриевые(Na);
группы делятся на типы в которых указывается соотношение между ионами (мг-экв)
I гидрокарбонат анионов HCO-3>Ca2++Mg2+- воды с небольшим солесодержанием с преобладающими Na и Ca
II HCO-3+SO42-< Ca2++Mg2+ или Cl-> Na+ воды океанов и морей и сильно минерализованных подземных источников
IV кислые воды содержащие HCO-3=0
Состав воды записывают формулой соответствующего класса
ССа,…г/кг II, общая жесткость мг-экв/л – относится к гидрокарбонатному классу, группы кальция, тип II
Если содержание другого иона металла отличается от преобладающего не более чем на 5 ммоль-экв то формулу записываем два символа элементов
ССа,MgII
36. Понятие об обобщённых оценочных показателях качества воды.
В зависимости от требований к воде, предъявляемых различными потребителями, ее классифицируют по целевым назначениям:
Питьевая вода и идущая для пищевой и бродильной промышленности должна быть безвредна для здоровья человека, иметь хорошие органолептические показатели и пригодна для хозяйственно-бытовых процессов. Если вода фторируется, то содержание фтора должно быть в пределах 70—80% от приведенных норм. Содержание серебра не должно превышать 0,05 мг/л.
При обнаружении в воде нескольких токсических веществ (за исключением фторидов, нитратов и радиоактивных веществ) сумма концентраций, выраженная в долях от максимально допустимых концентраций каждого вещества не должна превышать 1.
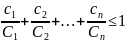
где с — обнаруженные концентрации каждого компонента, мг/л; С — максимально допустимые, мг/л.
В сахарном производстве должны отсутствовать легко разлагающиеся органические вещества во избежание брожения, содержание солей должно быть минимальным.
В пивоваренном производстве недопустимо CaSO4, т.к. препятствует брожению дрожжей.
Охлаждающая вода. В качестве охлаждающей используется необработанная природная вода. Она должна обладать: а) возможно более низкой температурой; б) возможно меньшей временной жесткостью; в) возможно меньшим содержанием взвешенных веществ, особенно органического происхождения; г) незначительной постоянной жесткостью воды. Она не должна оказывать разрушающего действия на аппаратуру.
Вода для паросилового хозяйства должна обладать: меньшей общей жесткостью; возможно меньшим содержанием кремниевой кислоты; не должно быть веществ, способствующих образованию стойкой пены (масла, смолистые и органические вещества); должны отсутствовать растворенные газы и свободные кислоты; допустимое количество масел в воде для питания котлов среднего давления не более 2 мг/л, для котлов высокого давления—до 1 мг/л; содержание кислорода для котлов низкого давления не более 3 мг/л, а для котлов среднего и высокого давлений – кислород не допускается.
Вода, идущая для технических целей. Зависит от конкретного производства. В фотопромышленности, текстильной и бумажной промышленности требуется отсутствие в воде железа, марганца, кремниевой кислоты, ограничивают содержание хлоридов.
В производстве искусственного волокна используется вода с низкой окисляемостью, низкой жесткостью; ограничивается и содержание железа.
Для крахмального производства недопустимо содержание листьев, водорослей крахмал будет желтым. Также недопустимо наличие железа.
Поливные воды. Недопустимо большое содержание солей, особенно солей Na и хлоридов.
