
- •Химический состав и строение молекулы воды.
- •Водородные взаимодействия.
- •Агрегатные состояния воды.
- •Аномалии воды.
- •Химические свойства воды.
- •Свойства растворов
- •6. Физико-химические свойства растворов неэлектролитов и электролитов.
- •7. Свойства растворов слабых электролитов.
- •Ионные равновесия
- •8. Растворимость веществ в воде.
- •10. Диссоциация воды.
- •11. Ионное произведение воды
- •12. Буферные растворы и их свойства
- •13. Гидролиз солей
- •14. Количественные характеристики гидролиза
- •15. Понятие о системах, фазах, компонентах.
- •16. Диаграмма состояния воды
- •17. Окислители и восстановители
- •18. Типы окислительно-восстановительных реакций
- •19. Окислительно-восстановительные потенциалы
- •20. Окислительно-восстановительные свойства воды
- •Классификация дисперсных систем.
- •Методы получения дисперсных систем.
- •Строение коллоидной частицы.
- •Свойства коллоидных систем.
- •Электрокинетические явления.
- •26.Причины устойчивости коллоидных систем
- •27. Разрушение дисперсных систем
- •28. Поверхностное натяжение
- •29. Поверхностно активные вещества
- •Поверхностные явления
- •30. Адсорбция равновесия
- •34 Особенности химического состава природных вод
- •36. Понятие об обобщённых оценочных показателях качества воды.
- •37. Химические показатели качества воды
- •40. Отстаивание.
- •41. Осаждение
- •42. Фильтрование воды
- •43. Флотация и электрофлотация
- •44. Коагуляция
- •45. Зависимость выбора оптимальных условий обработки различными коагулянтами от качества воды
- •46. Электрокоагуляция, эффективность использования
- •47. Флокулянты (анионо- и катионоактивные) их природа, свойства и методы действия, выбор оптимальной дозы.
- •48. Хлорирование: хлорирующие реагенты; механизм обеззараживающего действия, хлороёмкость воды в отсутствии и присутствии солевого аммиака.
- •56. Жесткость воды
- •57. Единицы измерения жесткости
- •58. Методы реагентного умягчения воды, их эффективность, контроль процессов реагентного умягчения.
- •59. Умягчения воды методом ионного обмена
- •60. Иониты (катиониты и аниониты), их природа, строение, свойства.
- •61. Термический метод умягчения воды.
- •62. Импфирование (подкисление)
- •63. Опреснение воды
- •64. Электрохимический метод.
- •66. Методы удаления из воды соединений железа и марганца
- •67.Удаление кремниевой кислоты
- •68.Обесфторирование и фторирование воды.
- •69. Не нашли этот вопрос
- •70. Углекислота и ее формы.
- •71. Вычисление содержания агрессивной углекислоты с помощью таблицы
- •72. Индекс насыщения воды карбонатом кальция
- •73. Особенности химического состава бытовых и производственных сточных вод
- •75Отстаивание, удаление масел и нефти
- •76.Коагулирование сточных вод.77.Выбор и подготовка коагулянтов.
- •78) Флотация сточных вод.
- •79) Сорбция.
- •80) Сорбция – область использования, факторы, влияющие на выбор сорбентов.
- •81) Экстракция, требования, предъявляемые к экстрагентам, экстракция в противотоке.
- •82.Эвапорация и аэрация.
- •83. Области использования аэрации и эвапорации, контроль процессов.
- •85. Нейтрализация сточных вод
- •84. Радиационнаяочистка сточных вод от органических загрязнений.
- •87.Химич очистка сточных вод
- •86.Дезинфекция сточных вод
- •88.Химическое окисление под давлением
- •89.Кристаллизация.
44. Коагуляция
Коагуляция - объединение частиц дисперсной фазы в агрегаты вследствие сцепления (адгезии) частиц при их соударениях. Коллоидные примеси возникают в результате алюмо-кремниевых кислот и солей, являющимися основным компонентом глины. Коллоидные частицы образуются отрицательно заряженными ионами (имеют отриц.заряд). При уменьшении pH устойчивость коллоидов снижается и наоборот. Если вода очень жесткая, то коллоидные частицы могут иметь положительный заряд.
Метод обработки воды, направленный на удаление в-в, находящихся в коллоидном состоянии, с помощью хим.реагентов, называется коагулированием. Применяющиеся при этом хим.в-ва называются коагулянтами. Метод применяется для осветления и обесцвечивания воды. При коагулировании наряду с коллоидными примесями удаляются грубодисперсные в-ва, а также бактерии и вирусы.
В качестве коагулянтов чаще всего используют соли алюминия и железа: сульфат алюминия Al2(SO4)3·18H2O, алюминат натрия NaAlO2, сульфат железа (II) FeSO4·7H2O (железный купорос), хлорид железа (III) FeCl3·6H2O.
В воде эти соли подвергаются ступенчатому гидролизу по схеме:
Me3+
+ H2O
![]() Me(OH)2+
Me(OH)2+
Me(OH)2+ + H2O Me(OH)2+ + H+
Me(OH)2+ + H2O Me(OH)3 + H+
Me3+ + 3H2O Me(OH)3 + 3H+
Полнота процесса гидролиза коагулянта достигается только при условии связывания образующихся ионов водорода. Степень гидролиза повышается при разбавлении растворов и повышении температуры.
Наибольшее распространение при коагуляции получил сернокислый алюминий, однако его применение ограничивается величиной рН обрабатываемой воды 6,5—7,5.
Коагулирование включает 3 стадии:
образование коллоидного р-ра гидроксида металла в результате полного гидролиза коагулянта;
коагуляция образовавшегося золя коагулянта под действием анионов воды и его взаимодействие с коллоидными и грубодисперсными молекулами;
процесс хлопьеобразования, завершающийся осаждением.
Основным фактором скорости коагулирования явл.стадия хлопьеобразования. Чем быстрее растут хлопья, тем быстрее идет осаждение, тем выше степень осветления воды.
На процесс коагуляции влияет t воды ( при уменьшении t устойчивость коллоидов увеличивается), pH и солевой состав.
45. Зависимость выбора оптимальных условий обработки различными коагулянтами от качества воды
Под оптимальной дозой коагулянта понимается та минимально возможная в данных условиях доза, дающая наибольшее снижение мутности.
Оптимальная доза определяется на основании результатов пробного коагулирования воды, которое служит не только для определения дозы коагулянта и флокулянта, но и для выбора наиболее перспективных видов реагентов. Доза коагулянта должна быть такой, чтобы при данных условиях было обеспечено образование относительно крупных хлопьев. Эта доза может быть найдена лабораторным путем.
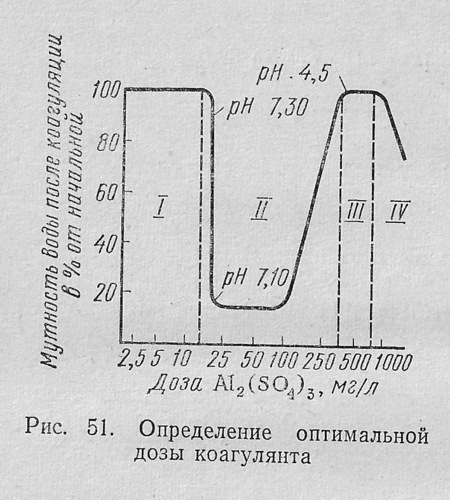
Помимо выявления необходимой дозы коагулянта опыты по пробному коагулированию устанавливают: 1) скорость образования хлопьев; 2) кинетику выпадения осадка; 3) кинетику уплотнения осадка. В процессе пробного коагулирования учитываются факторы, влияющие на процесс коагуляции: температура, pH раствора, интенсивность перемешивания и солевой состав воды.
Оптимальная доза коагулянта:
1)для
мутных вод: Дк=3,5
2)для
цветных вод: Дк=4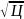
где Дк – доза коагулянта, М – мутность воды, мг/л, Ц – цветность воды.
