
- •Повторення основних питань курсу хімія
- •Валентність атомів деяких елементів у сполуках
- •Класифікація неорганічних сполук Оксиди
- •Класифікація
- •Добування
- •Хімічні властивості
- •Хімічні властивості
- •Кислоти
- •За числом атомів водню, які можуть заміщуватися на метал:
- •Добування
- •Хімічні властивості
- •Класифікація
- •Середні солі Добування
- •Хімічні властивості
- •Окисно-відновні реакції
- •Неметали та їх сполуки
- •Взаємодія неметалів з металами:
- •2. Взаємодія неметалів із неметалами.
- •Добування кисню:
- •Властивості кисню й озону
- •Сульфур
- •Алотропні видозміни Карбону
- •Вуглець
- •Нітроген
- •Сполуки неметалічних елементів ізГідрогеном
- •Хлороводень і хлороводнева кислота
- •Амоніак
- •Солі амонію
- •Виділення амоніаку – характерна ознак для розпізнавання солей амонію.
- •Розв’язування розрахункових задач на надлишок та вихід продукту.
- •1.Розвязування задач на визначення масової частки, об’єму та кількості речовини.
- •Самостійна робота:
- •Розв’язування задач на надлишок
- •Розв’язування задач на вихід продукту реакції
- •Оксиди неметалічних елементів. Оксиди Сульфуру
- •Оксиди Нітрогену
- •Хімічні властивості.
- •Оксиди Фосфору
- •Оксиди Карбону
- •Оксиди силіцію
- •Сульфатна кислота
- •Розбавлена сульфатна кислота
- •Концентрована сульфатна кислота
- •Добування і застосування сульфатної кислоти
- •Сульфати
- •Нітратна та ортофосфатна кислота
- •Мінеральні добрива
- •Карбонатна і силікатна кислота
- •Кристалічні гратки металів
- •Загальні фізичні властивості металів
- •Хімічні властивості металів.
- •Фізичні властивості лужних металів
- •Хімічні властивості лужних металів
- •Добування лужних металів
- •Оксиди лужних металів
- •Застосування оксидів лужних металів.
- •Гідроксиди лужних металів
- •Лужно-земельні метали
- •Кальцій
- •Кальцій оксид
- •Кальцій гідроксид
- •Алюміній
- •Алюміній оксид
- •Алюміній гідроксид
- •Солі Алюмінію
- •Оксиди і гідроксиди Феруму
- •Сполуки Феруму(ііі).
- •Органічна хімія
- •Отримання алкенів
- •Отримання алкінів
- •Отримання і хімічні властивості ароматичних вуглеводнів
- •Розв'язування задач на виведення молекулярної формули речовини.
- •Оксигеновмісні органічні сполуки
- •Альдегіди і карбонові кислоти
- •Естери і жири
- •Отримання і хімічні властивості жирів
- •Вуглеводи
- •Глюкоза
- •Сахароза
- •Крохмаль і целюлоза
- •Характеристики амінів
- •Амінокислоти
- •Реакції амінокислот
- •Загальні правила роботи і техніка безпеки в хімічній лабораторії
Алюміній
*охарактеризуйте алюміній за місеросташуванням в ПС,напишіть електронну конфігурацію його атома
У збудженому стані атом Алюмінію може утворювати три ковалентні зв’язки або віддавати три валентні електрони, виявляючи ступінь окиснення +3. Отже, в окисно-відновних реакціях Алюміній поводить себе як відновник.
У природі Алюміній дуже поширений,найпоширеніший метал на Землі-складає 8% земної кори, трапляється тільки у вигляді алюмосилікатів. Це різні глини, слюда, польовий шпат, каолін тощо. Основною алюмінієвою рудою є
![]()
Фізичні властивості.
Алюміній – сріблясто-білий метал, ковкий,легко витягається в дріт,доволі легкоплавкий tпл = 660oC, і дуже легкий r = 2,7 г/см3. Має високу електричну і теплову провідність, дуже пластичний. За кімнатної температури не змінюється на повітрі,тому що вкритий тонкою оксидною плівкою,яка має сильну захисн дію.
Хімічні властивості.
Алюміній – активний метал. Його поверхня вкрита тонкою, щільною і дуже міцною оксидною плівкою Al2O3, яка захищає його від подальшого окиснення і зумовлює високу корозійну стійкість:
4Al + 3O2 = 2Al2O3
1)якщо зняти оксидну плівку, алюміній енергійно реагує з водою:
![]()
2) за стандартних умов взаємодіє з хлором і бромом:

3) під час нагрівання – з багатьма неметалами:

4)за стандартних умов алюміній реагує з хлоридною і розбавленою сульфатною кислотою:
*напишіть рівняння реакції
Концентровані сульфатна й нітратна кислоти пасивують алюміній: під дією цих кислот збільшується товщина оксидної плівки на металі, і він не взаємодіє з ними.
5) взаємодіє з лугами завдяки легкості розчинення в них оксидної плівки:

6)Алюміній – добрий відновник багатьох оксидів металів:
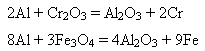
|
|
Спосіб відновлення оксидів металів алюмінієм називають алюмінотермією (різновид металотермії).
Добування і застосування алюмінію.
Спочатку з бокситу добувають глинозем, а потім електролізом розчину алюміній оксиду у розплавленому криоліті Na3[AlF6] добувають металічний алюміній.
Алюміній за використанням у промисловості посідає друге місце після заліза. Основна маса його йде на виготовлення сплавів – дюраль, або дюралюміній. Це сплав алюмінію з міддю і невеликими кількостями магнію, мангану та інших компонентів. Використовується як конструктивний матеріал в авіа- і машинобудуванні, як розкисник (вилучає надлишковий кисень) під час виплавляння сталі, для добування кальцію, барію, мангану, хрому алюмінотермічним способом, для виготовлення фольги у виробництві конденсаторів, у радіотехніці та для упакування шоколаду, чаю, інших продуктів і виготовлення алюмінієвого дроту, “срібної” фарби. Зі сплавів алюмінію роблять різні предмети побуту.
Алюміній оксид
Алюміній оксид (глинозем) Al2O3- біла тугоплавка (tпл=2044oC), нерозчинна у воді речовина.
Хімічний зв’язокAl – Oковалентний полярний, близький за полярністю до зв’язку О – Н. Тому алюміній оксид може виявляти як основні, так і кислотні властивості залежно від кислотно-основних властивостей речовини, з якою реагує. З кислотами він взаємодіє як основний оксид, а з основами (лугами) – як кислотний.
1) свіжодобутий алюміній оксид розчиняється в кислотах і лугах:

2)Під час сплавляння з лугами також утворюються алюмінати:


Добувають алюміній оксид у лабораторних умовах:
спалюючи метал:
*напишіть рівняння реакції
прожарюючи алюміній гідроксид:
*напишіть рівняння реакції
У природі існують модифікації алюміній оксиду у вигляді мінералу корунду, якому властива дуже висока твердість, і глинозему.
Застосування.
Забарвлені прозорі кристали корунду – коштовні камені:
- рубін – червоного кольору,
-сапфір – синього кольору.
Вони використовуються у ювелірній справі. Рубіни (штучно добуті) використовують як опорні камені у точних механізмах і як робочі тіла лазерів.
-Непрозорі кристали корунду – наждак. З нього виробляють шліфувальні круги, бруски для полірування металів. З глинозему як тугоплавкого матеріалу виготовляють тиглі, цеглу для скловарних печей тощо.
