
- •Повторення основних питань курсу хімія
- •Валентність атомів деяких елементів у сполуках
- •Класифікація неорганічних сполук Оксиди
- •Класифікація
- •Добування
- •Хімічні властивості
- •Хімічні властивості
- •Кислоти
- •За числом атомів водню, які можуть заміщуватися на метал:
- •Добування
- •Хімічні властивості
- •Класифікація
- •Середні солі Добування
- •Хімічні властивості
- •Окисно-відновні реакції
- •Неметали та їх сполуки
- •Взаємодія неметалів з металами:
- •2. Взаємодія неметалів із неметалами.
- •Добування кисню:
- •Властивості кисню й озону
- •Сульфур
- •Алотропні видозміни Карбону
- •Вуглець
- •Нітроген
- •Сполуки неметалічних елементів ізГідрогеном
- •Хлороводень і хлороводнева кислота
- •Амоніак
- •Солі амонію
- •Виділення амоніаку – характерна ознак для розпізнавання солей амонію.
- •Розв’язування розрахункових задач на надлишок та вихід продукту.
- •1.Розвязування задач на визначення масової частки, об’єму та кількості речовини.
- •Самостійна робота:
- •Розв’язування задач на надлишок
- •Розв’язування задач на вихід продукту реакції
- •Оксиди неметалічних елементів. Оксиди Сульфуру
- •Оксиди Нітрогену
- •Хімічні властивості.
- •Оксиди Фосфору
- •Оксиди Карбону
- •Оксиди силіцію
- •Сульфатна кислота
- •Розбавлена сульфатна кислота
- •Концентрована сульфатна кислота
- •Добування і застосування сульфатної кислоти
- •Сульфати
- •Нітратна та ортофосфатна кислота
- •Мінеральні добрива
- •Карбонатна і силікатна кислота
- •Кристалічні гратки металів
- •Загальні фізичні властивості металів
- •Хімічні властивості металів.
- •Фізичні властивості лужних металів
- •Хімічні властивості лужних металів
- •Добування лужних металів
- •Оксиди лужних металів
- •Застосування оксидів лужних металів.
- •Гідроксиди лужних металів
- •Лужно-земельні метали
- •Кальцій
- •Кальцій оксид
- •Кальцій гідроксид
- •Алюміній
- •Алюміній оксид
- •Алюміній гідроксид
- •Солі Алюмінію
- •Оксиди і гідроксиди Феруму
- •Сполуки Феруму(ііі).
- •Органічна хімія
- •Отримання алкенів
- •Отримання алкінів
- •Отримання і хімічні властивості ароматичних вуглеводнів
- •Розв'язування задач на виведення молекулярної формули речовини.
- •Оксигеновмісні органічні сполуки
- •Альдегіди і карбонові кислоти
- •Естери і жири
- •Отримання і хімічні властивості жирів
- •Вуглеводи
- •Глюкоза
- •Сахароза
- •Крохмаль і целюлоза
- •Характеристики амінів
- •Амінокислоти
- •Реакції амінокислот
- •Загальні правила роботи і техніка безпеки в хімічній лабораторії
Кристалічні гратки металів
У вузлах кристалічних граток металів містяться атоми та позитивно заряджені йони. Між ними постійно рухаються електрони. За рахунок електростатичного притягання між йонами та електронами забезпечується певна стабільність кристалічних граток металів.
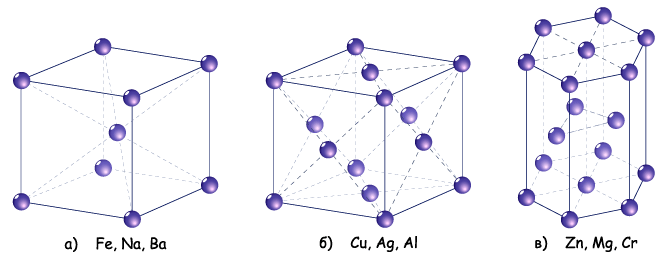
Основні типи кристалічних граток металів: а – кубічна об’ємноцентрована; б – кубічна гранецентрована; в – гексагональна.
Загальні фізичні властивості металів
Для металів характерні:
-металічний блиск внаслідок розсіювання світла електронами. Найкраще відбивають світло індій In та срібло Ag;
-кристалічна будова, крім ртуті Hg та францію Fr;
-сріблясто-білий колір(Ag, Al, Ni) або сріблясто-сірий (Fe, Pb), за винятком золота Au та міді Cu.
-За забарвленням метали умовно поділяють на чорні й кольорові. До чорних металів найчастіше відносять залізо та його сплави (чавун, сталь). Усі інші – називають кольоровими.
-теплова й електрична провідність, що зумовлена постійним рухом електронів у кристалі. За стандартних умов найвищу електричну провідність має срібло Ag, на другому місці – мідь Cu, далі золото Au і алюміній Al.
-твердість металів порівнюють із твердістю алмазу. Найтвердішими з металів є хром Cr і вольфрам W. Найм’якішими – є лужні метали, натрій Na і калій K легко ріжуться ножем;
-пластичність металів, їхня здатність необоротно деформуватися під дією механічних навантажень пояснюється можливістю переміщення (ковзання) одних шарів йонів металів відносно інших завдяки наявності “електронного газу”. Пластична деформація пояснюється розривом деяких міжатомних зв’язків і утворенням нових. Найпластичнішим металом є золото Au, а стибій Sb – дуже крихкий метал;
-розчинність. Усі метали не розчинні у воді, але розчиняються один в одному у розплавах
|
|
Твердий розчин одного металу в іншому називають сплавом. |
-густина. За густиною метали поділяють на легкіρ< 5 г/см3 і важкі ρ> 5 г/см3
Типові легкі метали – літій Li, натрій Na, магній Mg, алюміній Al. До важких металів належить цинк Zn, залізо Fe, мідь Cu, свинець Pb, ртуть Hg, золото Au. Найважчим з металів є осмій Os.
-температура плавлення найвища у вольфраму 3380o C, найнижча – у ртуті -30o C
За температурою плавлення метали поділяються на легкоплавкі tпл< 1000o C - натрій, магній, алюміній і тугоплавкі tпл> 1000o C - мідь, залізо, хром, титан, молібден.
Хімічні властивості металів.
Хімічна активність металів визначається здатністю їх атомів віддавати валентні електрони, тобто окиснюватись і перетворюватись на катіони (позитивно заряджені йони).
Чим легше метали віддають електрони, тим вони хімічно активніші, тим вони є сильнішими відновниками
За активністю метали розташовано у певний ряд (ряд Бекетова, витискувальний ряд, ряд активності, електрохімічний ряд металів):
![]()
![]()
зменшення хімічної активності
кожний метал цього ряду може витіснити з водного розчину сполуки будь-який з металічних елементів, що стоїть праворуч від нього, і може бути витіснений будь-яким з металів, що стоять ліворуч;
усі метали, що стоять ліворуч від водню, можуть витісняти Гідроген з кислот, а ті, що стоять праворуч, - не можуть;
чим лівіше стоїть у ряду метал, тим він сильніший відновник і тим важче відновити його.
1)взаємодіють з неметалами:
*Напишіть рівняння реакції взаємодії калію і сірки,магнію і кисню,алюмінію і брому.Вкажіть тип звязку у сполуках.Складіть схему електронногобалансу,визначте окисник і відновник
2)взаємодіють з водою:
Лужні й лужноземельні метали взаємодіють з водою за стандартних умов з утворенням лугів:
*напишіть рівнянян реакції взаємодіїкалію,кальцію,барію,натрію з водою
Менш активні метали реагують з водою при нагріванні:

3)взаємодіють з кислотами:
*Напишітьяк будуть взаємодіяти калій,кальцій,алюміній,залізо з хлоридною,фосфатною,карбонатною та концентрованими нітратною та сульфатною кислотами.Складіть схему електронного балансу.
4)взаємодіють з солями:
Реакція відбувається тільки у водному розчині: активніші метали витісняють менш активні:

5)взаємодіють з оксидами:
Активні метали відновлюють менш активні з оксидів під час нагрівання – металотермія:

6)взаємодіють з лугами:
Метали, яким відповідають амфотерні гідроксиди, реагують з лугами:

*Напишіть можливі рівняння реакцій
А)Al+ Fe2CO3=Е)Mg+CrPO4
Б) K+ NaCl=Г) Сu+CaSO4=
Д)Mn+Cu(NO3)2Є)Cu+FeCl3
Ж)Be+KOHВ)Mg+AgNO3
Загальна характеристика лужних та лужно-земельних металів
Елементи І групи періодичної системи називаються лужними металами.
Серед лужних металів найважливіше практичне значення мають елементи Натрій і Калій.
*Напишіть будову атомів Натрію і Калію,охарактеризуйте їх як хімічні елементи
|
|
Поширення лужних металів у природі
Лужні метали в природі у вільному стані не трапляються, тільки у вигляді сполук
Поширення лужних металів у природі
|
||||||||||||||||||||||||||||||||||||||||||||
