
- •Глава 13. Химия крови Кровь состоит из плазмы и форменных элементов.
- •Ведущая функция крови – транспортная
- •Белки – преобладающие компоненты плазмы
- •Патопротеинемия – любое отклонение от нормального соотношения белков в плазме крови
- •Уровень белков в плазме определяет распределение воды между кровью и тканями
- •Синтез белков плазмы – яркий пример механизма синтеза секретируемых белков.
- •Каждый белок плазмы характеризуется временем полураспада в кровообращении.
- •Содержание некоторых белков в плазме увеличивается во время острого воспаления.
- •Для классификации белков плазмы можно использовать разные подходы
- •Альбумин - главный белок плазмы человека
- •Глобулины - наиболее гетерогенная группа белков плазмы
- •Фракция α1-глобулинов
- •Недостаточность α1-антитрипсина ведет к эмфиземе легких
- •Фракция α2-глобулинов
- •Транспортный белок с ферментативной активностью – церулоплазмин
- •Фракция β-глобулинов
- •Иммуноглобулины – ведущие молекулы в механизмах защиты организма
- •Все иммуноглобулины состоят как минимум из двух легких и двух тяжелых цепей
- •Различают два типа легких цепей – λ и κ
- •Двух идентичных вариабельных областей не бывает
- •Функции, свойственные классу иммуноглобулина, определяют константные области молекул
- •Вместе с иммуноглобулинами на защиту организма может выступать система комплемента
- •Рис 13.5. Пути активирования системы комплемента Компоненты системы комплемента имеют специфические названия
- •Белки классического пути активирования комплемента
- •Лектиновый путь подобен классическому пути за исключением первой реакции
- •У альтернативного пути свой набор белков
- •В регуляции работы системы комплемента принимают участие специфические ингибиторы
- •Растворимые активные компоненты комплемента обладают широким спектром действия
- •Белки системы гемостаза
- •Сужение сосудов - первый этап гемостаза
- •Сосудисто-тромбоцитарный гемостаз – механизм остановки кровотечения при повреждении капилляров
- •Рис 13.6. Формы неактивных и активных тромбоцитов
- •Эндотелиоциты поддерживают кровь в жидком состоянии и участвуют в свертывании
- •Ингибиторы циклооксигеназной системы - эффективные антитромботические препараты
- •Классическая теория свертывание предложена п. Моравитцем и а Шмидтом.
- •Коагуляционный гемостаз состоит из трех фаз коагуляции и посткоагуляционной фазы
- •В зависимости от механизма первой фазы различают внутреннюю и внешнюю системы гемостаза
- •Фактор Ха – конечный продукт внутренней и внешней систем коагуляционного гемостаза
- •Вторая коагуляционная фаза – образованиие тромбина
- •Тромбин катализирует превращение фибриногена в фибрин в третью фазу коагуляции
- •Факторы свертывания крови происходят, по-видимому, из общего предшественника
- •Структурное подобие между белками дополняется общей зависимостью их функционального состояния от витамина к
- •Антитромботические механизмы предупреждают генерализацию свертывания крови в сосудах
- •Искусственные антикоагулянты могут быть прямого и непрямого действия
- •Гепарин, эдта и цитрат тормозят свертывание in vitro
- •Фибринолиз - важнейшая антисвертывающая система
- •Активаторы плазминогена выделены из тканей и биологических жидкостей
- •Ингибиторы фибринолиза - неотъемлемый компонент фибринолитической системы
- •Лабораторные тесты позволяют оценить состояние системы гемостаза у человека
- •Недостаточность факторов, тормозящих свертывание, обусловливает возникновение тромбозов
- •Кислотно-щелочное состояние
- •Концентрацию протонов необходимо поддерживать на постоянном уровне
- •Со2 – конечный продукт метаболизма и составляющая буферных систем организма
- •Цистеин и метионин важнейшие источники протонов
- •Буферные системы внеклеточного и внутриклеточного пространств.
- •Бикарбонатная буферная система является открытой системой
- •Гемоглобин является самым важным небикарбонатным буфером
- •Регуляция концентрации протонов
- •Легкие участвуют в регуляции бикарбонатной буферной системы
- •Синтез мочевины - один из путей регуляции кислотно-щелочного состояния
- •Почки участвуют в регуляции кщс путем выделения протонов
- •В моче также существует открытая буферная система
- •Ацидозы и алкалозы – это нарушения кислотно-щелочного состояния
- •РН-метры и газовые анализаторы позволяют поставить диагноз нарушения кщс
- •Самые частые нарушения кщс в медицинской практике – метаболические ацидозы
Синтез мочевины - один из путей регуляции кислотно-щелочного состояния
В условиях азотистого равновесия около 90 г белков подвергаются распаду, результатом которого является образование ионов бикарбоната (около 60 г или 1 моль/сут) и аммиака, которые используются в основном печенью в механизме синтеза мочевины (рис.13.20). При этом из моля HCO3- и моля NH4+ образуется 1 моль мочевины, т.е. удаления бикарбоната и аммиака сопряжены друг с другом. Если количество бикарбоната снижается, то снижается и образование мочевины, а выделение ионов аммония переключается на альтернативные пути.
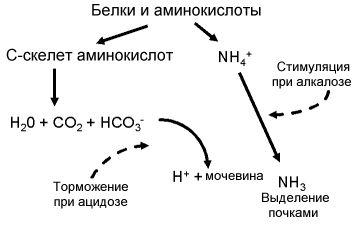
Рис.13.20. Обмен белков и КЩС
Примером такого состояния может служить ацидоз, при котором наблюдается снижение синтеза мочевины и ионы аммония, связываясь с глутаминовой кислотой в составе глутамина, покидают гепатоциты. Глутамин транспортируется к почкам, и используются как источник ионов аммония, выделяемых с мочой. Наоборот, при алкалозе происходит активное потребление бикарбоната циклом мочевинообразования, а необходимый в эквимолярных количествах NH4+ образуется путем повышения активности глутаминазы из глутамина, который в этом случае потребляется печенью.
Почки участвуют в регуляции кщс путем выделения протонов
Хотя почки изменяют концентрацию протонов значительно медленнее, чем другие органы, однако удаление протонов с мочой позволяет регенерировать буферные анионы. Канальцы почек в состоянии повысить концентрацию водородных ионов в 1000 раз: от 40 нмоль/л (концентрация в крови и первичной моче) до 40 ммоль/л (концентрация в конечной моче при рН 4,4). Эти 0,04 ммоль/л лишь незначительная часть ежедневной продукции протонов, которая у взрослого человека составляет от 40 до 80 ммоль за сутки. Если бы это количество протонов (в среднем 60 ммоль) распределить в 1,5 л мочи (40 ммоль/л мочи), то рН мочи было бы 1,4. Однако обычно рН мочи не опускается ниже 4,4 (в норме 4,4-8,0). То, что ежедневно произведенное количество протонов, тем не менее, может выделяться, объясняется присутствием буферных растворов в моче.
При секреции протонов в мочу (Рис.13.21) диоксид углерода, который образуется в реакциях обмена в клетках канальцев или извлекается из крови, под влиянием фермента карбангидразы II превращается в углекислоту. Последняя диссоциирует на ионы бикарбоната и протоны. В то время как протоны диффундируют в мочу, бикарбонаты переходят во внеклеточное пространство вместе с ионами натрия для поддержания электронейтральности. Как уже упоминалось, выделяемые протоны в моче связываются буферными растворами.
В моче также существует открытая буферная система
Такой буферной системой в моче является фосфатная. Она образована одно- и двузамещенными солями фосфорной кислоты. Концентрация компонентов данной буферной системы в гломерулярном фильтрате такая же, как и в плазме (1 ммоль/л). При значении рН гломерулярного фильтрата равном 7.4, 80 % фосфатов этой системы представлено

Рис.13.21. Схема образования протонов клетками канальцев почек. Выделение протона сопровождается переходом в кровь иона бикарбоната
двузамещенной и 20 % однозамещенной формами ионов фосфорной кислоты (отношение 4:1). Благодаря благоприятному положению значения рK равному 6,80 (рН=рК±1 для нелетучих буферных систем) эта система превосходно соответствует условиям поддержания рН в моче. Уже при рН 4.5 почти весь двузамещенный фосфат превращается, принимая протон (НРО4- + Н+ → Н2РО4-) в двузамещенный. Таким способом около 50 % протонов, попадающих в мочу, могут быть связаны.
При титровании мочи щелочью (0,1 N NаОН) связанные этой буферной системой протоны можно определить количественно. Данная величина обозначается как титруемая кислотность мочи, которая у здорового человека составляет 10 – 40 ммоль /24 ч.
Титруемая кислотность сильно повышается при нагрузках кислотой. Емкость этой нелетучей буферной системы при нагрузках относительно мала, так как уровень фосфатов в моче во многом определяется их потреблением с пищей.
Система ионы аммония/аммиак. Клетки эпителия канальцев обладают еще одной возможностью связывать протоны – они синтезируют аммиак. Так как концентрация аммиака во внеклеточном пространстве и, следовательно, в гломерулярном фильтрате чрезвычайно низкая (аммиак обезвреживается в печени) клетки эпителия получают аммиак, главным образом, из глутамина, который образуется в различных тканях (мышцы, мозг, печень) и рассматривается как транспортная форма аммиака в крови. Эпителиальные клетки дистальных и проксимальных канальцев, а также собирательных трубочек содержат высокоактивную глутаминазу, катализирующую гидролиз глутамина и высвобождение аммиака. Последний секретируется в просвет канальцев и действует там как акцептор протонов (NH3 +H+ → NH4+).
Образующийся ион аммония, обладающий высоким зарядом, не проходит через мембраны и остается в моче. Выделение аммония составляет у здорового 30 – 50 ммоль/сут. В то время как фосфатная буферная система быстро реагирует на нагрузку кислотой, повышение выделения аммония происходит постепенно, в течение нескольких дней.
Таблица 13.8. Выделение протонов почками у человека
|
|
Выделение протонов (ммоль/24 ч) |
Отношение аммиак/ титруемая кислотность |
|
У здорового Протоны, связанные с аммиаком Титруемая кислотность
У больных диабетом с кетоацидозом Протоны, связанные с аммиаком Титруемая кислотность
У больных с хроническим воспалением почек (нефрит) Протоны, связанные с аммиаком Титруемая кислотность |
30–50
10–30
300–500
75–250
0,5 – 1,5
2,0 – 20 |
1 – 2,5
1 – 2,5
0,2 – 1,5 |
Однако возможности аммиачной буферной системы намного выше, чем у фосфатной (титруемая кислотность). Выделение протонов при помощи данной буферной системы может достигать до 500 ммоль/сут. Аммиак очень удобный компонент буферной системы, поскольку подобно диоксиду углерода является конечным продуктом обмена азота и его количество не ограничено. При помощи реакций аминирования (глутаматдегидрогеназа и глутаминсинтетаза) аммиак частично может усваиваться ( подобно СО2 в реакциях карбоксилирования), однако животные клетки не обладают способностью полной фиксации этого конечного продукта. При нагрузках кислотой ( например, при продолжительном голодании, что сопровождается образованием кетоновых тел) азота больше выделяется в форме аммиака чем в форме мочевины.
Таблица 13.9. Характеристика СО2/НСО3 и NH4+/NH3 буферных систем
|
Показатели |
СО2/НСО3 |
NH4+/NH3 |
|
рК Один из партнеров Тип системы Отношение ион/газ при рН 7.4 Конечный продукт Растворимость в воде Место действия
Противостоит
|
6,10 Летучий Открытая
20:1 С-обмена Хорошая Внеклеточное пространство Щелочи |
9,40 Летучий Открытая
100:1 N-обмена Очень хорошая Моча
Кислоте |
Значение рК аммиачной буферной системы равно 9,4, что, как указывалось выше, относительно неблагоприятно для значений рН гломерулярного фильтрата. Такая буферная система в закрытых условиях плохо справлялась бы с функцией поддержания рН. Однако учитывая то, что аммиак постоянно выделяется клетками канальцев, этот буфер можно рассматривать как открытую систему подобно таковой для бикарбонатной буферной системы. Так как соотношение ион аммония / аммиак очень высокое ( 100:1 при рН 7.4) через мочу могут выделяться большие количества протонов без значительных изменений рН. Такая система соответствует описанной выше бикарбонатной системе, которая представляет открытую систему с соотношением анион /газ 20:1 и неблагоприятным для рН крови значением рК равном 6.1.
