
- •Глава 13. Химия крови Кровь состоит из плазмы и форменных элементов.
- •Ведущая функция крови – транспортная
- •Белки – преобладающие компоненты плазмы
- •Патопротеинемия – любое отклонение от нормального соотношения белков в плазме крови
- •Уровень белков в плазме определяет распределение воды между кровью и тканями
- •Синтез белков плазмы – яркий пример механизма синтеза секретируемых белков.
- •Каждый белок плазмы характеризуется временем полураспада в кровообращении.
- •Содержание некоторых белков в плазме увеличивается во время острого воспаления.
- •Для классификации белков плазмы можно использовать разные подходы
- •Альбумин - главный белок плазмы человека
- •Глобулины - наиболее гетерогенная группа белков плазмы
- •Фракция α1-глобулинов
- •Недостаточность α1-антитрипсина ведет к эмфиземе легких
- •Фракция α2-глобулинов
- •Транспортный белок с ферментативной активностью – церулоплазмин
- •Фракция β-глобулинов
- •Иммуноглобулины – ведущие молекулы в механизмах защиты организма
- •Все иммуноглобулины состоят как минимум из двух легких и двух тяжелых цепей
- •Различают два типа легких цепей – λ и κ
- •Двух идентичных вариабельных областей не бывает
- •Функции, свойственные классу иммуноглобулина, определяют константные области молекул
- •Вместе с иммуноглобулинами на защиту организма может выступать система комплемента
- •Рис 13.5. Пути активирования системы комплемента Компоненты системы комплемента имеют специфические названия
- •Белки классического пути активирования комплемента
- •Лектиновый путь подобен классическому пути за исключением первой реакции
- •У альтернативного пути свой набор белков
- •В регуляции работы системы комплемента принимают участие специфические ингибиторы
- •Растворимые активные компоненты комплемента обладают широким спектром действия
- •Белки системы гемостаза
- •Сужение сосудов - первый этап гемостаза
- •Сосудисто-тромбоцитарный гемостаз – механизм остановки кровотечения при повреждении капилляров
- •Рис 13.6. Формы неактивных и активных тромбоцитов
- •Эндотелиоциты поддерживают кровь в жидком состоянии и участвуют в свертывании
- •Ингибиторы циклооксигеназной системы - эффективные антитромботические препараты
- •Классическая теория свертывание предложена п. Моравитцем и а Шмидтом.
- •Коагуляционный гемостаз состоит из трех фаз коагуляции и посткоагуляционной фазы
- •В зависимости от механизма первой фазы различают внутреннюю и внешнюю системы гемостаза
- •Фактор Ха – конечный продукт внутренней и внешней систем коагуляционного гемостаза
- •Вторая коагуляционная фаза – образованиие тромбина
- •Тромбин катализирует превращение фибриногена в фибрин в третью фазу коагуляции
- •Факторы свертывания крови происходят, по-видимому, из общего предшественника
- •Структурное подобие между белками дополняется общей зависимостью их функционального состояния от витамина к
- •Антитромботические механизмы предупреждают генерализацию свертывания крови в сосудах
- •Искусственные антикоагулянты могут быть прямого и непрямого действия
- •Гепарин, эдта и цитрат тормозят свертывание in vitro
- •Фибринолиз - важнейшая антисвертывающая система
- •Активаторы плазминогена выделены из тканей и биологических жидкостей
- •Ингибиторы фибринолиза - неотъемлемый компонент фибринолитической системы
- •Лабораторные тесты позволяют оценить состояние системы гемостаза у человека
- •Недостаточность факторов, тормозящих свертывание, обусловливает возникновение тромбозов
- •Кислотно-щелочное состояние
- •Концентрацию протонов необходимо поддерживать на постоянном уровне
- •Со2 – конечный продукт метаболизма и составляющая буферных систем организма
- •Цистеин и метионин важнейшие источники протонов
- •Буферные системы внеклеточного и внутриклеточного пространств.
- •Бикарбонатная буферная система является открытой системой
- •Гемоглобин является самым важным небикарбонатным буфером
- •Регуляция концентрации протонов
- •Легкие участвуют в регуляции бикарбонатной буферной системы
- •Синтез мочевины - один из путей регуляции кислотно-щелочного состояния
- •Почки участвуют в регуляции кщс путем выделения протонов
- •В моче также существует открытая буферная система
- •Ацидозы и алкалозы – это нарушения кислотно-щелочного состояния
- •РН-метры и газовые анализаторы позволяют поставить диагноз нарушения кщс
- •Самые частые нарушения кщс в медицинской практике – метаболические ацидозы
Антитромботические механизмы предупреждают генерализацию свертывания крови в сосудах
Описанные выше механизмы свертывания по своему принципу организации напоминают систему водяного каскада, что обеспечивает выполнение ими важной функции – усиления (амплификации) сигнала: ферменты более высокого уровня этого каскада множат (с множителем равным 8) число молекул нижнего уровня, что подчеркивает повышение значимости концентрации факторов свертывания более низкого уровня этого каскада для достижения цели – образования сгустка крови. Однако такое усиление могло бы привести к непрерывному ускорению однажды начавшегося свертывания крови и вызвать превращение всего наличного фибриногена в фибрин. Особенностью данного каскада является возможность обратной регуляции на каждом уровне каскада, которая обеспечивает поддержку баланса между про- и антикоагулянтами. Система факторов коагуляции контролируется системой антикоагулянтов (рис.13.12).
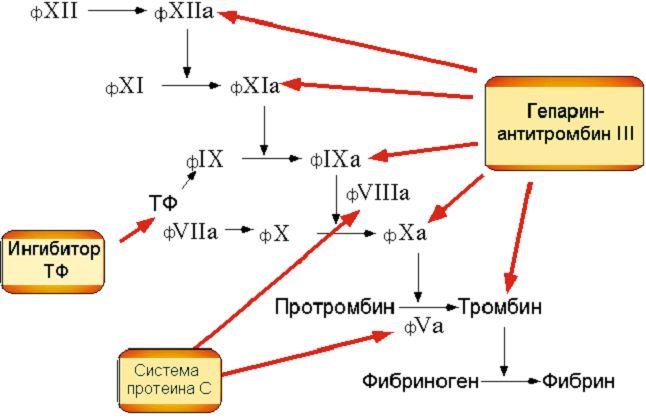
Рис.13.12. Место действия ингибиторов системы гемостаза
Антикоагулянты действуют по различным механизмам: препятствуют активированию факторов свертывания крови, нейтрализуют и ингибируют активные факторы коагуляции, блокируют реакции между факторами свертывания; блокируют активацию тромбоцитов, их активные формы и (или) тромбоцитарные факторы (в частности, Р3 и Р4) на стадиях протромбиназо- и тромбинообразования, а также препятствуют полимеризации фибрин-мономеров. Практически каждому из участников процесса фибринообразования противостоят специфические ингибиторы. По механизму образования в организме все естественные (физиологические) антикоагулянты разделяют на первичные и вторичные. Первичные антикоагулянты постоянно синтезируются в организме и с постоянной скоростью выделяются в кровоток. Они взаимодействуют с активными факторами коагуляции, нейтрализуя их, и не действуют на неактивные формы этих факторов. Вторичные антикоагулянты образуются из факторов свертывания и других белков в процессе свертывания крови, фибринолиза и активации других протеолитических систем.
Из множества физиологических антикоагулянтов наиболее хорошо известными являются:
антитромбин III (гепариновый кофактор) – гликопротеин с молекулярной массой 56 – 65 кДа. Содержание в сыворотке – 290 мг/л. Ингибирует различные протеолитические ферменты серинового типа, но наиболее активно действует на факторы IIa, Ха и XIa. В присутствии гепарина ингибирующая активность повышается почти в 100 раз. Терапевтический эффект гепарина зависит от антитромбина III: при снижении содержания последнего падает эффективность вводимого гепарина. Уровень антитромбина III снижается при 6олезнях печени, диссеминированном внутрисосудистом свертывании, опухолях, остром лейкозе и других заболеваниях. Врожденная недостаточность антитромбина III характеризуется усилением свертывания, предрасположенностью к тромбофлебитам, тромбоэмболии. Гепарин образует комплексы с антитромбином III в соотношении 1: 1. Механизм ингибирующего действия подобен действию α1-ингибитора протеаз. Тромбин образует комплекс с ингибитором, причем его диссоциация сопровождается образованием двух цепей антитромбина, соединенных между собой дисульфидными мостиками, что указывает на протеолитическое расщепление антитромбина тромбином. Подобный эффект обнаруживается и при взаимодействии антитромбина III с факторами IXа и Ха. Увеличение ингибирующих свойств антитромбина III под влиянием гепарина связывают с действием последнего на конформацию антитромбина III;
a2-макроглобулин, на долю которого приходится около 3,5 % антитромбинового потенциала крови;
Протеин С (назван так потому, что при хроматографии на ионобенной колонке выходил в третьей фракции (первые А и В). Это сериновая протеаза, состоящая из двух полипептидных цепей с мол. массой 41 и 21 кДа, синтезируется в форме неактивного профермента в печени. Подобно другим факторам свертывания имеет 10 витамин К-зависимых карбокислированных остатков Глу. При лечении антагонистами витамина К активность этого белка снижается. Протеин С активируется свободным тромбином, но этот процесс протекает медленно и не имеет физиологического значения. Значительно быстрее он активируется с участием тромбомодулина – белка на поверхности тромбоцитов, являющегося рецептором тромбина. Связанный с тромбомодулином тромбин очень быстро активирует протеин С. Для оптимального протекания этого процесса необходимо участие кофактора – протеина S (по названию города Сиэттла, где его впервые открыли);
Протеин S – тоже витамин К-зависимый белок, синтезируемый в печени. В крови циркулирует в свободной форме или как комплекс с С4b-связывающим белком (ингибитором системы комплемента) или как комплекс с протеин S-связывающим белком. Комплекс из активного белка С и белка S инактивирует активные факторы Vа и VIIIа и действует при этом как антикоагулянт. Одновременно этот комплекс инактивирует ингибитор тканевого активатора плазминогена, косвенно выполняя роль стимулятора фибринолиза.
В физиологических условиях содержание антикоагулянтов достаточно для сдерживания процессов гемокоагуляции на уровне, необходимом для предотвращения потери крови из сосудов при неизбежных микротравмах, связанных с обязательными механическими движениями (дыхание, перемещение и т.д.). При усиленном тромбинообразовании компенсаторно растет и уровень антикоагулянтов. Патологическое повышение активности ингибиторов затрудняет свертывание крови и может сопровождаться развитием геморрагии. Снижение активности антикоагулянтов, наоборот, повышает свертываемость крови и способствует образованию тромбов. Дефицит АТ-III и протеина С или его кофакторов, является наиболее частой причиной тромбофилий.
