
- •Глава 13. Химия крови Кровь состоит из плазмы и форменных элементов.
- •Ведущая функция крови – транспортная
- •Белки – преобладающие компоненты плазмы
- •Патопротеинемия – любое отклонение от нормального соотношения белков в плазме крови
- •Уровень белков в плазме определяет распределение воды между кровью и тканями
- •Синтез белков плазмы – яркий пример механизма синтеза секретируемых белков.
- •Каждый белок плазмы характеризуется временем полураспада в кровообращении.
- •Содержание некоторых белков в плазме увеличивается во время острого воспаления.
- •Для классификации белков плазмы можно использовать разные подходы
- •Альбумин - главный белок плазмы человека
- •Глобулины - наиболее гетерогенная группа белков плазмы
- •Фракция α1-глобулинов
- •Недостаточность α1-антитрипсина ведет к эмфиземе легких
- •Фракция α2-глобулинов
- •Транспортный белок с ферментативной активностью – церулоплазмин
- •Фракция β-глобулинов
- •Иммуноглобулины – ведущие молекулы в механизмах защиты организма
- •Все иммуноглобулины состоят как минимум из двух легких и двух тяжелых цепей
- •Различают два типа легких цепей – λ и κ
- •Двух идентичных вариабельных областей не бывает
- •Функции, свойственные классу иммуноглобулина, определяют константные области молекул
- •Вместе с иммуноглобулинами на защиту организма может выступать система комплемента
- •Рис 13.5. Пути активирования системы комплемента Компоненты системы комплемента имеют специфические названия
- •Белки классического пути активирования комплемента
- •Лектиновый путь подобен классическому пути за исключением первой реакции
- •У альтернативного пути свой набор белков
- •В регуляции работы системы комплемента принимают участие специфические ингибиторы
- •Растворимые активные компоненты комплемента обладают широким спектром действия
- •Белки системы гемостаза
- •Сужение сосудов - первый этап гемостаза
- •Сосудисто-тромбоцитарный гемостаз – механизм остановки кровотечения при повреждении капилляров
- •Рис 13.6. Формы неактивных и активных тромбоцитов
- •Эндотелиоциты поддерживают кровь в жидком состоянии и участвуют в свертывании
- •Ингибиторы циклооксигеназной системы - эффективные антитромботические препараты
- •Классическая теория свертывание предложена п. Моравитцем и а Шмидтом.
- •Коагуляционный гемостаз состоит из трех фаз коагуляции и посткоагуляционной фазы
- •В зависимости от механизма первой фазы различают внутреннюю и внешнюю системы гемостаза
- •Фактор Ха – конечный продукт внутренней и внешней систем коагуляционного гемостаза
- •Вторая коагуляционная фаза – образованиие тромбина
- •Тромбин катализирует превращение фибриногена в фибрин в третью фазу коагуляции
- •Факторы свертывания крови происходят, по-видимому, из общего предшественника
- •Структурное подобие между белками дополняется общей зависимостью их функционального состояния от витамина к
- •Антитромботические механизмы предупреждают генерализацию свертывания крови в сосудах
- •Искусственные антикоагулянты могут быть прямого и непрямого действия
- •Гепарин, эдта и цитрат тормозят свертывание in vitro
- •Фибринолиз - важнейшая антисвертывающая система
- •Активаторы плазминогена выделены из тканей и биологических жидкостей
- •Ингибиторы фибринолиза - неотъемлемый компонент фибринолитической системы
- •Лабораторные тесты позволяют оценить состояние системы гемостаза у человека
- •Недостаточность факторов, тормозящих свертывание, обусловливает возникновение тромбозов
- •Кислотно-щелочное состояние
- •Концентрацию протонов необходимо поддерживать на постоянном уровне
- •Со2 – конечный продукт метаболизма и составляющая буферных систем организма
- •Цистеин и метионин важнейшие источники протонов
- •Буферные системы внеклеточного и внутриклеточного пространств.
- •Бикарбонатная буферная система является открытой системой
- •Гемоглобин является самым важным небикарбонатным буфером
- •Регуляция концентрации протонов
- •Легкие участвуют в регуляции бикарбонатной буферной системы
- •Синтез мочевины - один из путей регуляции кислотно-щелочного состояния
- •Почки участвуют в регуляции кщс путем выделения протонов
- •В моче также существует открытая буферная система
- •Ацидозы и алкалозы – это нарушения кислотно-щелочного состояния
- •РН-метры и газовые анализаторы позволяют поставить диагноз нарушения кщс
- •Самые частые нарушения кщс в медицинской практике – метаболические ацидозы
Ингибиторы фибринолиза - неотъемлемый компонент фибринолитической системы
Как и в системе коагуляции, конечный эффект определяется взаимоотношениями между активаторами и ингибиторами фибринолиза. На каждом его этапе действуют специфические ингибиторы. Различают ингибиторы плазмина и ингибиторы активаторов плазминогена. Нередко один и тот же ингибитор способен инактивировать и активатор плазминогена и плазмин.
Ингибиторы плазмина –антиплазмины. Известно, по меньшей мере, шесть антиплазминов α2-антиплазмин, α2-макроглобулин, α2-антитрисин, антитромбин III, С1-инактиватор, интер-α2-антитрипсин.
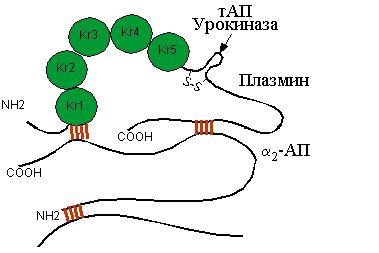
Рис.13.16.Схема взаимодействия a2-АП и плазмина
Важнейшим физиологическим ингибитором плазмина является α2-антиплазмин (α2-АП) – гликопротеин (мол. масса 67 кДа), синтезирующийся в гепатоцитах. Хотя на α2-АП приходится всего 2,2 % общей антиплазминовой активности плазмы, он является наиболее мощным и быстродействующим ингибитором плазмина.
α2-АП, имеющий богатые лизинами домены, необратимо ингибирует плазмин. связываясь с кринглами последнего. В циркулирующей крови свободного плазмина нет, так как α2-АП связывает и инактивирует даже его следовые количества, быстро прекращая фибринолиз за пределами сгустков фибрина. Поэтому фибриноген, более предпочтительный субстрат для свободного плазмина, сохраняется в крови интактным. В случае внутривенного введения активаторов плазминогена в больших дозах при лечении тромбозов возможности α2-АП по ингибированию образующегося плазмина могут быть превышены и в циркулирующей крови появляется свободный плазмин, что вызывает фибриногенолиз и, следовательно, кровотечение, часто сопровождающее лечение активаторами плазминогена. α2-АП способен также связывать трипсин, калликреин, фактор Ха, урокиназу, тАПГ и, следовательно, вмешиваться в процесс как на ранних, так и на поздних этапах фибринолиза, а также тормозить процесс свертывания крови.
Другой функционально важный ингибитор плазмина α2-макроглобулин (α2-МГ), в отличие от α2-АП реагирует с плазмином относительно медленно, но его связывающая емкость довольно высокая, и он используется для инактивации плазмина при появлении последнего в больших количествах и исчерпании запасов α2-АП . α2 МГ ингибирует не только свободный, но и связанный с фибрином плазмин. Вызывая частичный протеолиз плазмина, не затрагивающий активного центра, он сохраняет большую часть фибринолитической активности плазмина, но тормозит фибриногенолитическую активность. α2-МГ может связываться с внутренней поверхностью эндотелиального слоя кровеносных сосудов, что позволяет говорить о важной роли этого белка в регуляции протеолиза на стенке кровеносных сосудов.
α1Антитрипсин, антитромбин III и его комплекс с гепарином, как и другие ингибиторы, играют ограниченную роль в качестве ингибиторов плазмина. Их значение возрастает только тогда, когда концентрации α2-антиплазмина и α2-макроглобулина понижаются .
Ингибиторы активаторов плазминогена (антиактиваторы). Неспособность тканевого активатора плазминогена вызвать активацию плазминогена в жидкой фазе обусловлена и большим избытком антиактиваторов, с которым он образует комплекс. Это ингибирование активаторов плазминогена обратимо и для диссоциации комплекса активатор–антиактиватор необходима твердая фаза в виде фибринового сгустка.
Выделяют четыре типа естественных тканевых ингибиторов активаторов плазминогена (ПАИ).
Ингибитор I типа (ПАИ-1) найден в эндотелии, плазме, тромбоцитах и гепатоцитах. На его долю приходится 60 % антиактиваторной активности.
Ингибитор II типа (ПАИ-2), получивший название плацентарного, синтезируется не только в плаценте, но и макрофагами и моноцитами; он чрезвычайно быстро связывает активатор плазминогена урокиназного типа, но не способен нейтрализовать проурокиназу.
Ингибитор III типа (ПАИ-З) обнаружен в плазме.
Ингибитор IV типа (ПАИ-4), или никсинпротеаза, синтезируется фибробластами и напоминает ингибитор трипсиноподобных протеаз. Повышенное образование антиактиваторов плазминогена может быть причиной снижения фибринолитической активности крови.
NB! Фибринолиз можно затормозить при помощи лекарственных препаратов
Для нормализации повышенной активности системы фибринолиза (например, при лейкозах, операциях на богатых активаторами фибринолиза органах, таких, как матка, предстательная железа или легкие) можно использовать искусственные ингибиторы фибринолиза. Наиболее широко используются такие лекарственные препараты как эпсилон-аминокапроновая кислота (ЭАКК) и амбен (блокируют активный центр активатора плазминогена и препятствуют образованию плазмина); трасилол, контрикал, гордокс (непосредственно ингибируют плазмин).
В условиях нормы активаторная и ингибиторная функции фибринолитической системы находятся в динамическом равновесии. Локальное или системное снижение фибринолитической активности приводит к тромбозам. С другой стороны, чрезмерное повышение фибринолитической активности может сопровождаться кровотечениями.
