
- •ВВЕДЕНИЕ
- •1. ОСНОВНЫЕ ПОНЯТИЯ ХИМИИ
- •1.1. Химическая реакция
- •1.2. Классификация веществ
- •1.3. Количественные расчеты в химии
- •2. СТРОЕНИЕ АТОМА
- •2.1. Развитие представлений о строении атома
- •2.1.1. Теория строения атома Бора
- •2.1.2. Особенности описания микрочастиц
- •2.2. Основные понятия волновой механики
- •2.2.1. Волновое уравнение
- •2.2.2. Решение уравнения Шрёдингера для простейших случаев
- •2.3.1. Основное состояние атома водорода
- •2.3.2. Радиальное распределение электронной плотности. Электронная орбиталь
- •2.3.3. Возбужденные состояния атома водорода
- •2.3.4. Многоэлектронные атомы
- •2.4. Периодический закон и таблица элементов
- •2.4.1. Электронные конфигурации многоэлектронных атомов
- •2.4.2. Связь периодического закона со строением атома
- •2.4.3. Физико-химические характеристики атома
- •Контрольные вопросы
- •3. ХИМИЧЕСКАЯ СВЯЗЬ
- •3.1. Основные характеристики и классификация моделей химической связи
- •3.1.1. Основные параметры химической связи
- •3.1.2. Типы химической связи
- •3.2. Ковалентная химическая связь
- •3.2.1. Метод валентных связей
- •3.2.3. Геометрия простейших молекул. Гибридизация АО
- •3.2.4. Донорно-акцепторный механизм образования ковалентной связи
- •3.2.5. Метод молекулярных орбиталей
- •3.2.6. Полярность связи и дипольный момент молекулы
- •Контрольные вопросы
- •4. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ВЕЩЕСТВАХ
- •4.1. Межмолекулярные взаимодействия
- •4.1.2. Водородная связь
- •4.2. Химическая связь в твердом теле
- •4.2.1. Основные понятия о строении кристаллов
- •4.2.3. Ковалентные (атомные) кристаллы
- •4.2.4. Ионные кристаллы. Ионный тип химической связи
- •4.2.5. Химическая связь в металлах
- •4.2.6. Зонная модель кристаллического тела
- •4.2.7. Металлы, полупроводники и диэлектрики
- •4.2.8. Кристаллические материалы
- •4.2.9. Аморфные твердые тела
- •4.3. Химическая связь в жидкостях
- •Контрольные вопросы
- •5. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
- •5.1. Основные понятия и определения
- •5.1.1. Термодинамическая система
- •5.1.2. Термодинамический процесс
- •5.2. Тепловые эффекты физико-химических процессов
- •5.2.1. Внутренняя энергия
- •5.2.2. Первое начало термодинамики
- •5.2.3. Тепловой эффект химической реакции
- •5.2.4. Термохимические расчеты
- •5.3. Направление и пределы протекания химического процесса
- •5.3.1. Второе начало термодинамики
- •5.3.2. Энтропия
- •5.3.3. Направление химического процесса
- •5.3.4. Химический потенциал
- •Контрольные вопросы
- •6. КИНЕТИКА ХИМИЧЕСКИХ РЕАКЦИЙ
- •6.1. Механизм химической реакции
- •6.1.1. Частицы, участвующие в химической реакции
- •6.1.2. Классификация химических реакций
- •6.2. Элементарная химическая реакция
- •6.2.1. Скорость химической реакции
- •6.2.2. Зависимость скорости химической реакции от концентрации реагирующих веществ
- •6.2.3. Константа скорости химической реакции
- •6.3. Формальная кинетика гомогенных реакций
- •6.3.1. Кинетические уравнения реакций
- •6.3.2. Зависимость скорости реакции от температуры
- •6.3.3. Определение кинетических параметров реакции
- •6.4. Цепной механизм химической реакции
- •6.5. Индуцированные реакции
- •6.5.1. Фотохимические реакции
- •6.5.2. Радиационно–химические процессы
- •6.6. Макрокинетика
- •6.6.1. Гетерогенные реакции
- •6.6.2. Горение и взрыв
- •6.7. Катализ
- •6.7.1. Гомогенный катализ
- •6.7.2. Гетерогенный катализ
- •Контрольные вопросы
- •7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- •7.1. Термодинамическое условие химического равновесия
- •7.2. Кинетическое условие химического равновесия
- •7.3. Расчет равновесного состава газовой смеси
- •7.4. Равновесия в растворах
- •7.4.1. Растворы
- •7.4.2. Электролитическая диссоциация
- •7.4.3. Ионное произведение воды. Водородный показатель
- •7.4.4. Растворы кислот и оснований
- •7.4.5. Буферные растворы
- •7.4.6. Гидролиз солей
- •7.4.7. Обменные реакции с образованием осадка
- •7.5. Фазовые равновесия
- •7.5.1. Диаграмма состояния однокомпонентной системы
- •7.5.2. Диаграмма состояния двухкомпонентной системы
- •7.5.3. Кипение и кристаллизация растворов
- •7.5.4. Электролиты
- •Контрольные вопросы
- •8. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- •8.1. Основные понятия и определения
- •8.2. Электродные процессы
- •8.2.1. Скачок потенциала на границе «металл–электролит»
- •8.2.2. Уравнение Нернста
- •8.2.3. Электроды
- •8.3. Неравновесные электрохимические системы
- •8.3.1. Гальванический элемент
- •8.3.2. Окислительно-восстановительные реакции в водных растворах
- •8.3.3. Электролиз
- •8.4. Кинетика электрохимических процессов
- •8.4.1. Скорость электрохимических процессов
- •8.4.2. Поляризация электродов
- •8.5. Практическое использование электрохимических процессов
- •8.5.1. Химические источники тока
- •8.5.2. Применение электролиза
- •Контрольные вопросы
- •9. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- •9.1. Коррозионные процессы
- •9.2. Химическая коррозия
- •9.2.1. Высокотемпературная газовая коррозия
- •9.2.2. Кинетика роста оксидных пленок
- •9.2.3. Факторы, влияющие на скорость газовой коррозии
- •9.3. Электрохимическая коррозия
- •9.3.1. Анодные и катодные реакции
- •9.3.2. Термодинамические условия электрохимической коррозии металлов
- •9.3.3. Факторы, влияющие на скорость электрохимической коррозии
- •9.4. Коррозионные среды и влияние дополнительных факторов
- •9.4.1. Коррозионно-механическое разрушение металлов
- •9.4.2. Водородная коррозия
- •9.4.3. Радиационная коррозия
- •Контрольные вопросы
- •Библиографический список

динат (траектории движения), а можем говорить лишь о вероятности нахождения ее в какой-либо части пространства.
Вероятностный характер механики микрочастиц следует также из опытов по дифракции электронов. Если пропускать не поток, а последовательно по одному электрону, то каждый из них попадет в какое-то определенное место экрана и дифракционной картины не будет. В какое конкретное место попадет следующий электрон, мы не знаем, но знаем, где вероятность его появления максимальна (кольцо) и где минимальна (между кольцами) (см. рис. 2.2). И только большое число электронов, пропущенных последовательно друг за другом, создадут на экране дифракционную картину.
2.2. Основные понятия волновой механики
2.2.1. Волновое уравнение
Уравнение, которое будет описывать движение электрона, должно удовлетворять следующим требованиям: отражать волновой характер движения электрона и содержать характеристики электрона как частицы.
Для описания волновых свойств электрона можно использовать известное из математики и физики дифференциальное уравнение
второго порядка (уравнение волнового процесса):
∂∂2xΨ2 +∂∂2yΨ2 +∂∂2zΨ2 =v12 ∂∂2tΨ2 ,
где v – скорость распространения волны; Ψ(x,y,z,t) – пси-функция – волновая функция, которая зависит от координат и времени и может быть представлена в виде синуса, косинуса, экспоненты или любой другой функции, являющейся решением дифференциального уравнения волнового процесса.
Для простоты написания левую часть уравнения представляют
обычно в операторной форме: |
|
∂2Ψ |
|
||||||||||
|
|
|
|
|
|
|
∂2Ψ |
+ |
∂2Ψ |
+ |
= 2Ψ, |
||
|
|
|
|
|
|
|
∂x2 |
∂y2 |
∂z2 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|||
|
∂2 |
∂2 |
∂2 |
|
|
|
|
|
|
||||
где |
|
+ |
|
+ |
|
= 2 – |
оператор |
Лапласа (читается «набла |
|||||
∂x2 |
∂y2 |
∂z2 |
|||||||||||
два»), тогда волновое уравнение приобретает вид
32

2Ψ= v12 ∂∂2tΨ2 .
Чаще всего интерес представляют стационарные процессы (стоячие волны). Описывающее их уравнение содержит функцию, не зависящую от времени. Для стоячей волны
2Ψ(x,y,z) + (4π2ν2/v2) Ψ(x,y,z) = 0.
Поскольку частота волнового процесса (ν) равна скорости распространения волны (v), деленной на длину волны: ν = v/λ и, соот-
ветственно, ν/v = 1/λ, то
2Ψ(x, y, z) + (4π2/λ2) Ψ(x, y, z) = 0.
В полученном уравнении, используя соотношение де Бройля, можно заменить длину волны такими характеристиками частицы, как масса и кинетическая энергия.
Длина волны де Бройля λ= hp = mhv .
Кинетическая энергия электрона |
|
E |
=mv 2 |
= |
(mv )2 |
= |
p2 |
, |
||||||||
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
к |
|
2 |
|
|
2m |
|
2m |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
λ= |
h |
= |
|
h |
, |
λ2 = |
h2 |
|
|
|
||||||
p |
|
|
|
|
2mE |
|
|
|
|
|||||||
2mE |
|
|
|
|||||||||||||
|
|
|
|
к |
|
|
|
|
к |
|
|
|
||||
2Ψ(x,y,z)+8π2m Eк Ψ(x,y,z)=0 . h2
Как правило, при описании состояния электрона определяют его полную энергию. Поскольку кинетическая энергия электрона (Eк) равна разности между полной (E) и потенциальной (V) энергией: Eк = E – V, то можно записать:
2Ψ(x, y,z)+8π2m (E−V ) Ψ(x, y,z)=0 . h2
Таким образом получают волновое уравнение, независимое от времени, содержащее в качестве параметра массу электрона. Это уравнение известно как уравнение Шрёдингера, названное по имени австрийского физика Эрвина Шрёдингера, который предложил его в 1926 г. для описания состояния микрочастицы в потенциальном поле.
Прежде чем решать уравнение Шрёдингера для конкретных систем, выясним физический смысл волновой функции. Раскрыть
33
его достаточно непросто, поскольку в макромире нет аналогий корпускулярно-волновым свойствам микрообъектов. И до некоторой степени волновая функция представляет собой математическую абстракцию.
В 1926 г. Макс Борн, применив вероятностные идеи принципа неопределенности, дал общепринятую в настоящее время трактовку физического смысла волновой функции: квадрат волновой функции пропорционален вероятности нахождения (dP) частицы в элементарном объеме (dV):
dP = Ψ2(x, y, z) dV.
П р и м е ч а н и е. В общем случае, если Ψ-функция − комплексная величина, вероятность нахождения частицы (dP) в элементарном объеме (dV) пропорциональна квадрату ее модуля: dP = |Ψ|2dV = Ψ*ΨdV.
Величина dVdP = Ψ2(x, y, z) называется плотностью вероятности
и характеризует вероятность нахождения частицы в элементарном объеме пространства с координатами x, y, z. Для электрона ее часто называют электронной плотностью.
Вероятность нахождения частицы в каком-либо конечном объеме V равна интегралу квадрата волновой функции по данному объему:
PV =∫Ψ2 (x,y,z)dV .
V
Вероятность должна выражаться действительным положительным числом, меньшим или равным единице. Сама же волновая функция может быть положительной, отрицательной или мнимой.
Вероятностное толкование физического смысла волновой функции является одним из постулатов квантовой механики. Правомерность такой интерпретации подтверждается соответствием экспериментально определенного взаимного расположения атомов в молекулах и квантово-механического расчета.
Из условия, что вероятность события не может быть больше единицы, следует принцип нормирования волновых функций. Веро-
ятность нахождения частицы во всем рассматриваемом объеме должна быть равна единице (частица находится в этом объеме – событие достоверное):
P = ∫A2Ψ2 (x,y,z)dV =1 .
V
34

Здесь А – нормирующий множитель, коэффициент, входящий в волновую функцию, который подбирается таким образом, чтобы выполнялось условие нормировки.
2.2.2. Решение уравнения Шрёдингера для простейших случаев
Решение уравнения Шрёдингера даже для относительно простых реальных объектов, таких как атомы и молекулы, содержащих два и более электронов, представляет собой сложную математическую задачу. Для того чтобы понять характер и особенности результатов квантово-механического описания состояния электрона в атомах и молекулах, решим строго простейшую задачу нахождения электрона в так называемом «потенциальном ящике» – некоторой ограниченной области пространства, вне которой потенциальная энергия электрона обращается в бесконечность. Электрон не может покинуть пределы «потенциального ящика», т.е. он находится в связанном состоянии. Это, по сути своей, является моделью нахождения электрона в атоме.
Электрон в одномерном потенциальном ящике. Движение электрона происходит только вдоль оси X (рис. 2.3). Внутри ящика потенциальная энергия частицы принимается равной нулю (потенциальную энергию можно отсчитывать от любого выбранного уровня), вне его она равна бесконечности, т.е. частица находится внутри ящика и не может покинуть его пределы.
|
|
E |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V=∞ |
|
|
V=0 |
|
|
V=∞ |
|
|
x |
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
a |
|
|
|||||
Рис. 2.3. Электрон в одномерном потенциальном ящике: a − параметр (размер) потенциального ящика
С точки зрения классической механики частица, находящаяся в потенциальном ящике, может иметь, в принципе, любую энергию и находиться в любой точке ящика. При квантово-механическом рассмотрении ситуация меняется. Состояние электрона описывает уравнение Шрёдингера, и его характеристики (энергия и вероятность нахождения в пространстве) получают при решении этого уравнения.
35

Как и любое дифференциальное уравнение, уравнение Шрёдингера имеет бесконечное множество решений, но физический смысл содержат лишь некоторые из них. В нашем случае волновая функция описывает реальную физическую систему, поэтому она должна соответствовать определенным условиям:
•конечность – вероятность нахождения электрона в пространстве не может быть больше единицы;
•однозначность – вероятность нахождения электрона в точке однозначна;
•непрерывность – нет особых точек в пространстве. Поскольку электрон находится внутри одномерного «ящика»
(V = 0), уравнение Шрёдингера приобретает вид
d 2Ψ(x) +8π2m E Ψ(x)=0 . dx2 h2
Известно, что решением уравнения данного типа может быть функция Ψ(x)= A sin 2λπx – общее решение. Но вид функции мо-
жет быть и другим.
Используя общее решение, граничные условия нашей задачи и принцип нормировки, можно получить волновую функцию, описывающую состояние электрона в потенциальном ящике.
Граничными условиями является равенство волновой функции
нулю на стенках: Ψ(0)= Asin |
2π |
0=0 , |
Ψ(a)= Asin |
2π |
a =0 . |
|
λ |
|
|
λ |
|
Поскольку амплитуда волновой функции не равна нулю, то из второго условия следует:
sin |
2π |
a =0 , |
2π |
a = πn , n = 1,2,3…, |
λ= |
2a |
, |
Ψ(x)= Asin |
πn x . |
|
λ |
λ |
|
n |
|
|
a |
||
Значение амплитуды А находят из условия нормировки. Поскольку электрон находится в потенциальном ящике, то интеграл квадрата волновой функции по координате ящика (от нуля до a) равен единице:
a |
2 |
|
|
a |
2 |
|
2 |
|
πn |
|
|
1 |
a |
2 |
|
πn |
|
∫Ψ |
|
(x)dx=1 |
, |
∫A |
|
sin |
|
( |
|
x)dx=1 |
, |
|
=∫sin |
|
( |
|
)dx , |
|
|
|
a |
A2 |
|
a |
|||||||||||
0 |
|
|
|
0 |
|
|
|
|
|
|
0 |
|
|
|
36

a |
|
|
πn |
|
a |
|
1 |
|
a |
|
|
|
|
|
|
||
2 |
|
)dx= |
, |
= |
, |
A= |
2 |
. |
|||||||||
∫sin |
( |
||||||||||||||||
|
a |
2 |
A |
2 |
2 |
a |
|||||||||||
0 |
|
|
|
|
|
|
|
|
|
|
|
||||||
Таким образом, волновая функция электрона в одномерном потенциальном ящике
Ψ(x)= |
|
2 |
|
sin |
πn |
x , |
a |
|
|
||||
|
|
|
|
a |
||
где a – параметр потенциального ящика; n = 1,2,3…– целочисленный параметр. То есть состоянию электрона в потенциальном ящике соответствует набор волновых функций, различающихся целочисленным параметром n, называемым квантовым числом.
Для определения энергии электрона проделаем следующие математические операции.
1. Поскольку в уравнение Шрёдингера входят волновая функция и ее вторая производная, запишем их:
Ψ(x)=A sin πan x , dΨ(dxx) =A πan cos πan x ,
d 2Ψ(x) |
=A |
π2n2 |
(−sin |
πn |
x) . |
||
dx2 |
|
a2 |
a |
||||
|
|
|
|||||
2. Подставим выражения волновой функции и ее второй производной в уравнение Шрёдингера, описывающее состояние электрона внутри потенциального ящика:
A |
π2n2 |
(−sin |
πn |
x)+ |
8π2m |
E |
A sin |
πn |
|
=0 |
, |
|||||||
a2 |
a |
|
h2 |
|
a |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
A(sin |
πn |
x) [− |
π2n2 |
8π2m |
E]=0 . |
|
|
||||||||||
|
|
|
|
|
+ |
|
|
|
|
|
||||||||
|
a |
a2 |
|
|
h2 |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
3. Поскольку волновая функция внутри ящика не равна нулю
( Ψ(x)=A sin πan x≠0 ), то
− |
π2n2 |
+ |
8π2m |
E =0 |
и E = |
h2 |
n |
2 |
, n=1,2,3… |
|
a2 |
h2 |
8a2 |
m |
|
||||||
|
|
|
|
|
|
|
||||
Следовательно, набору волновых функций соответствует набор величин энергий (рис.2.4).
37
|
|
|
1) |
2) |
ψ2(x) |
3) |
|
|||
|
E |
|
|
ψ(x) |
|
|
||||
n=2 |
E2 |
|
|
|
|
ψ2(x) |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
ψ1(x) |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
n=1 |
E1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
0 a/2 a |
x |
0 |
a/2 a x |
|||
|
|
|
|
|
|
|||||
|
|
0 |
a |
|
x |
|
|
|
|
|
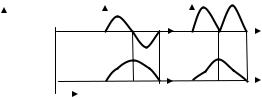
Рис. 2.4. Первое и второе энергетические состояния электрона в одномерном потенциальном ящике. Полная энергия Еi (1), соответствующая ей волновая функ-
ция Ψi(x) (2) и плотность вероятности Ψi2(x) (3) электрона
Из полученных результатов решения следуют особенности квантово-механического описания состояния электрона в потенциальном ящике.
1.Электрон может иметь только дискретные значения полной
энергии E1, E2, E3…, величины которых определяет целочисленный параметр n = 1,2,3…, называемый квантовым числом. То есть энергия связанного электрона квантована.
2.Распределение вероятности нахождения электрона (плотность вероятности) определяется его энергией.
3.Величина энергии и соответствующая ей волновая функция, характеризующая распределение вероятности нахождения элек-
трона в объеме (Еi -Ψi), определяют энергетическое состояние электрона. Каждому энергетическому состоянию соответствует квантовое число n.
Электрон в трехмерном потенциальном ящике. Вырожденные энергетические состояния. Задача о нахождении частицы в
трехмерном потенциальном ящике аналогична предыдущей. Граничные условия полностью совпадают: волновая функция на границах ящика обращается в нуль, потенциальная энергия внутри ящика равна нулю (V = 0), а за пределами ящика – бесконечности
(V = ∞), т.е. частица не может покинуть потенциальный ящик. Единственное отличие в том, что волновая функция является
функцией трех пространственных координат: Ψ(x,y,z).
Уравнение Шрёдингера для данного случая представляет собой дифференциальное уравнение в частных производных с тремя переменными:
38

∂2Ψ(x, y,z) |
+ |
∂2Ψ(x, y,z) |
+ |
∂2Ψ(x, y,z) |
+ |
8π2m |
E Ψ(x, y,z)=0. |
|
∂x2 |
∂y2 |
∂z2 |
h2 |
|||||
|
|
|
|
Стандартным приемом, которым пользуются при решении уравнений такого типа, является разделение переменных − представление волновой функции в виде произведения трех функций, каждая из которых зависит только от одной координаты:
|
|
|
|
Ψ(x,y,z)=X (x)Y (y)Z(z) , |
|
|
|
|
||||||||||
Y (y)Z(z) d 2 X (x) + X (x)Z(z) |
d 2Y (y) |
+ X (x)Y (y) |
d 2Z(z) |
= |
||||||||||||||
|
|
dz2 |
||||||||||||||||
|
|
dx2 |
|
|
|
|
|
|
|
dy2 |
|
|
|
|
|
|
||
|
|
|
|
=− |
8π2m |
E X (x)Y (y)Z(z), |
|
|
|
|
||||||||
|
|
|
|
|
h2 |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
1 |
|
d 2 X (x) |
+ |
1 |
|
|
d 2Y (y) |
+ |
1 |
|
d 2Z(z) |
=− |
8π2m E. |
|
||||
X (x) |
|
Y (y) |
|
Z(z) |
|
|
||||||||||||
|
dx2 |
|
dy2 |
|
|
dz2 |
|
h2 |
|
|||||||||
Поскольку правая часть уравнения не зависит от координат, то можно представить полную энергию электрона как сумму трех энергий: E = Ex + Ey + Ez. Уравнение Шрёдингера при этом преобразуется в три дифференциальных уравнения, аналогичных волновым уравнениям электрона в одномерном ящике, решение которых уже получено:
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
d 2 X (x) |
=− |
8π2m |
Ex , |
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
X (x) |
|
|
dx2 |
|
|
|
h2 |
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
1 |
|
d 2Y(y) |
=− |
8π2m |
Ey , |
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
Y(y) |
|
|
|
|
|
h2 |
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
dy2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
1 |
|
|
d 2Z(z) |
=− |
8π2m |
Ez . |
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
Z(z) |
|
dz2 |
|
|
|
h2 |
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
Для волновой функции |
|
|
|
|
|
|
|
|
|
|
nyπ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
n |
π |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
n |
π |
|
|||||
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
2 |
|
|
|
|
||||||||||
X (x)= |
|
|
sin |
x |
|
x , Y (y)= |
|
|
|
sin |
|
|
|
|
y , |
Z(z)= |
|
|
|
|
sin |
z |
|
z , |
|||||||||||||||
a |
|
a |
|
b |
|
b |
|
|
c |
|
c |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
n |
π |
|
|
|
|
|
|
|
nyπ |
|
n |
π |
|
|
|
|
|||||||
|
|
|
|
|
|
|
8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
Ψ(x,y,z)= |
|
|
|
|
|
|
sin( |
x |
|
x) sin( |
|
|
|
y) sin( |
z |
|
|
|
z) |
, |
|
|
|||||||||||||||||
|
a b c |
|
a |
|
b |
c |
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
a, b, c – параметры трехмерного потенциального ящика (размеры – длина, ширина, высота); nx, ny, nz – целочисленные параметры –
39
«квантовые числа». Необходимо отметить, что каждой координате соответствует свое квантовое число.
Для энергии
Ex = |
h2 |
2 |
|
Ey = |
|
h2 |
|
|
|
2 |
, Ez = |
h2 |
2 |
|
||||||
|
nx |
, |
|
|
|
|
ny |
|
nz |
, |
||||||||||
8ma2 |
8mb2 |
8mc2 |
||||||||||||||||||
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|||||||
|
|
|
|
h2 |
|
n |
2 |
|
ny |
|
n |
2 |
|
|
|
|
||||
|
|
E = |
|
( |
|
x |
|
+ |
|
|
|
+ |
z |
|
) . |
|
|
|
||
|
|
8m |
a2 |
b2 |
c2 |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Из полученных результатов решения следует:
1)энергия электрона в трехмерном потенциальном ящике квантована;
2)каждое энергетическое состояние электрона определяется набором из трех квантовых чисел.
Однако в реальных системах часто встречается ситуация, когда определенное энергетическое состояние (энергия частицы) может быть описано не единственным набором квантовых чисел, т.е. более чем одной волновой функцией. Тогда говорят о вырождении энергетического состояния.
Проиллюстрировать явление вырождения по энергии можно на примере частицы в трехмерном потенциальном ящике. Если рассмотреть энергетические состояния частицы в ящике, который представляет собою куб (а = b = c), то выражение для энергии приобретает вид
E = |
h2 |
2 |
|
2 |
|
2 |
|
|
(nx |
+ny |
|
+nz |
|
) , |
|
8ma2 |
|
|
|||||
|
|
|
|
|
|
|
а – параметр куба (величина ребра).
Составим энергетическую диаграмму состояния частицы в таком ящике, откладывая по вертикальной оси энергию частицы в
единицах |
h2 |
(рис. 2.5). |
|
8ma2 |
|||
|
|
В кубическом потенциальном ящике почти все энергетические состояния в той или иной степени вырождены. Степень вырожде-
ния − число вариантов наборов квантовых чисел (число волновых функций), при помощи которых можно описать данное энергети-
ческое состояние. Снятие вырождения является важной проблемой квантово-механического описания системы. В случае трехмерного потенциального ящика вырождение снимается частично
(a = b ≠ c) или полностью (a ≠ b ≠ c) при изменении параметров
40
