
- •ВВЕДЕНИЕ
- •1. ОСНОВНЫЕ ПОНЯТИЯ ХИМИИ
- •1.1. Химическая реакция
- •1.2. Классификация веществ
- •1.3. Количественные расчеты в химии
- •2. СТРОЕНИЕ АТОМА
- •2.1. Развитие представлений о строении атома
- •2.1.1. Теория строения атома Бора
- •2.1.2. Особенности описания микрочастиц
- •2.2. Основные понятия волновой механики
- •2.2.1. Волновое уравнение
- •2.2.2. Решение уравнения Шрёдингера для простейших случаев
- •2.3.1. Основное состояние атома водорода
- •2.3.2. Радиальное распределение электронной плотности. Электронная орбиталь
- •2.3.3. Возбужденные состояния атома водорода
- •2.3.4. Многоэлектронные атомы
- •2.4. Периодический закон и таблица элементов
- •2.4.1. Электронные конфигурации многоэлектронных атомов
- •2.4.2. Связь периодического закона со строением атома
- •2.4.3. Физико-химические характеристики атома
- •Контрольные вопросы
- •3. ХИМИЧЕСКАЯ СВЯЗЬ
- •3.1. Основные характеристики и классификация моделей химической связи
- •3.1.1. Основные параметры химической связи
- •3.1.2. Типы химической связи
- •3.2. Ковалентная химическая связь
- •3.2.1. Метод валентных связей
- •3.2.3. Геометрия простейших молекул. Гибридизация АО
- •3.2.4. Донорно-акцепторный механизм образования ковалентной связи
- •3.2.5. Метод молекулярных орбиталей
- •3.2.6. Полярность связи и дипольный момент молекулы
- •Контрольные вопросы
- •4. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ВЕЩЕСТВАХ
- •4.1. Межмолекулярные взаимодействия
- •4.1.2. Водородная связь
- •4.2. Химическая связь в твердом теле
- •4.2.1. Основные понятия о строении кристаллов
- •4.2.3. Ковалентные (атомные) кристаллы
- •4.2.4. Ионные кристаллы. Ионный тип химической связи
- •4.2.5. Химическая связь в металлах
- •4.2.6. Зонная модель кристаллического тела
- •4.2.7. Металлы, полупроводники и диэлектрики
- •4.2.8. Кристаллические материалы
- •4.2.9. Аморфные твердые тела
- •4.3. Химическая связь в жидкостях
- •Контрольные вопросы
- •5. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
- •5.1. Основные понятия и определения
- •5.1.1. Термодинамическая система
- •5.1.2. Термодинамический процесс
- •5.2. Тепловые эффекты физико-химических процессов
- •5.2.1. Внутренняя энергия
- •5.2.2. Первое начало термодинамики
- •5.2.3. Тепловой эффект химической реакции
- •5.2.4. Термохимические расчеты
- •5.3. Направление и пределы протекания химического процесса
- •5.3.1. Второе начало термодинамики
- •5.3.2. Энтропия
- •5.3.3. Направление химического процесса
- •5.3.4. Химический потенциал
- •Контрольные вопросы
- •6. КИНЕТИКА ХИМИЧЕСКИХ РЕАКЦИЙ
- •6.1. Механизм химической реакции
- •6.1.1. Частицы, участвующие в химической реакции
- •6.1.2. Классификация химических реакций
- •6.2. Элементарная химическая реакция
- •6.2.1. Скорость химической реакции
- •6.2.2. Зависимость скорости химической реакции от концентрации реагирующих веществ
- •6.2.3. Константа скорости химической реакции
- •6.3. Формальная кинетика гомогенных реакций
- •6.3.1. Кинетические уравнения реакций
- •6.3.2. Зависимость скорости реакции от температуры
- •6.3.3. Определение кинетических параметров реакции
- •6.4. Цепной механизм химической реакции
- •6.5. Индуцированные реакции
- •6.5.1. Фотохимические реакции
- •6.5.2. Радиационно–химические процессы
- •6.6. Макрокинетика
- •6.6.1. Гетерогенные реакции
- •6.6.2. Горение и взрыв
- •6.7. Катализ
- •6.7.1. Гомогенный катализ
- •6.7.2. Гетерогенный катализ
- •Контрольные вопросы
- •7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- •7.1. Термодинамическое условие химического равновесия
- •7.2. Кинетическое условие химического равновесия
- •7.3. Расчет равновесного состава газовой смеси
- •7.4. Равновесия в растворах
- •7.4.1. Растворы
- •7.4.2. Электролитическая диссоциация
- •7.4.3. Ионное произведение воды. Водородный показатель
- •7.4.4. Растворы кислот и оснований
- •7.4.5. Буферные растворы
- •7.4.6. Гидролиз солей
- •7.4.7. Обменные реакции с образованием осадка
- •7.5. Фазовые равновесия
- •7.5.1. Диаграмма состояния однокомпонентной системы
- •7.5.2. Диаграмма состояния двухкомпонентной системы
- •7.5.3. Кипение и кристаллизация растворов
- •7.5.4. Электролиты
- •Контрольные вопросы
- •8. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- •8.1. Основные понятия и определения
- •8.2. Электродные процессы
- •8.2.1. Скачок потенциала на границе «металл–электролит»
- •8.2.2. Уравнение Нернста
- •8.2.3. Электроды
- •8.3. Неравновесные электрохимические системы
- •8.3.1. Гальванический элемент
- •8.3.2. Окислительно-восстановительные реакции в водных растворах
- •8.3.3. Электролиз
- •8.4. Кинетика электрохимических процессов
- •8.4.1. Скорость электрохимических процессов
- •8.4.2. Поляризация электродов
- •8.5. Практическое использование электрохимических процессов
- •8.5.1. Химические источники тока
- •8.5.2. Применение электролиза
- •Контрольные вопросы
- •9. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- •9.1. Коррозионные процессы
- •9.2. Химическая коррозия
- •9.2.1. Высокотемпературная газовая коррозия
- •9.2.2. Кинетика роста оксидных пленок
- •9.2.3. Факторы, влияющие на скорость газовой коррозии
- •9.3. Электрохимическая коррозия
- •9.3.1. Анодные и катодные реакции
- •9.3.2. Термодинамические условия электрохимической коррозии металлов
- •9.3.3. Факторы, влияющие на скорость электрохимической коррозии
- •9.4. Коррозионные среды и влияние дополнительных факторов
- •9.4.1. Коррозионно-механическое разрушение металлов
- •9.4.2. Водородная коррозия
- •9.4.3. Радиационная коррозия
- •Контрольные вопросы
- •Библиографический список
С усовершенствованием приборов и техники спектроскопии обнаружили, что линии, принимавшиеся за единичные, в действительности состоят из нескольких близко расположенных друг к другу линий. Следовательно, для каждого квантового числа существует несколько близких друг к другу энергетических уровней. До некоторой степени это объяснил Арнольд Зоммерфельд, который допустил существование в атоме эллиптических орбит. Было введено еще два дополнительных квантовых числа: побочное и магнитное, существование которых непосредственно не вытекало из теории Бора. Однако в целом необходимо констатировать, что в рамках классической физики не удалось создать «хорошую» модель описания поведения микрочастиц. Основным недостатком теории Бора для химии явилась невозможность дать даже качественное и, тем более, количественное описание химической связи.
2.1.2. Особенности описания микрочастиц
Корпускулярно-волновой дуализм свойств материи. Одной из наиболее спорных проблем в истории естествознания была проблема природы лучистой энергии – электромагнитного излучения. Взгляды физиков на природу света (волна или поток частиц), начиная с Исаака Ньютона, периодически менялись. К концу XIX века общепринятым считалось, что электромагнитное излучение имеет волновую природу. Однако к началу XX века встала проблема описания явления излучения света нагретыми телами. Не удавалось создать на основе классической электродинамики модель, объясняющую излучательную способность нагретых тел. Макс Планк предложил гипотезу о квантовой природе процесса излучения (1900 г.), согласно которой излучение энергии нагретым абсолютно черным телом происходит не непрерывно, как того требовала классическая теория, а дискретными порциями – квантами. Минимальная энергия – величина энергии кванта – пропорциональна частоте излучения:
E = hν,
где h = 6,6262 10-34 Дж с – постоянная Планка, ν – частота излучения, с-1.
Альберт Эйнштейн высказал предположение о том, что идея квантования энергии относится не только к процессам поглощения и испускания света нагретыми телами, но и к излучению как тако-
28
вому. То есть электромагнитное излучение распространяется в ви-
де дискретных частиц с энергией E = hν, названых впоследствии фотонами. Такие радикальные изменения во взглядах на природу света, предложенные Планком и Эйнштейном, нашли экспериментальное подтверждение в исследовании фотоэффекта – испускания электронов веществом под действием света. Корпускулярные свойства электромагнитного излучения особенно проявились в рассеянии рентгеновского излучения различными веществами – эффект Комптона, все особенности которого можно объяснить упругим столкновением фотонов рентгеновского излучения со слабосвязанными электронами.
Таким образом, поток электромагнитного излучения, с одной стороны, является волной, что наблюдается при интерференции и дифракции, а с другой стороны, – потоком частиц, что экспериментально проявляется в процессах испускания, поглощения и рассеяния излучения твердыми телами.
Используя выражение Планка для энергии кванта излучения и формулу Эйнштейна, показывающую взаимосвязь энергии частицы и ее массы (E = mc2), можно связать характеристики фотона (масса, импульс) и характеристики волны (длина волны и частота):
E = hν E = mc2 → hν = mc2,
ν = c/λ → hc/λ = mc2 → m = h/cλ → λ = h/mc, p = mc → λ = h/p;
h – постоянная Планка; ν – частота излучения; m – масса фотона,
кг; c– скорость света в вакууме; λ – длина волны излучения, м; p – импульс фотона.
Так что же такое фотон – волна или частица? Скорее всего, сущность этой проблемы связана с ограниченностью наших жизненных представлений. Мы живем в макромире, где только по отдельности встречаются процессы, имеющие корпускулярную и волновую природу. Нигде в повседневной жизни мы не встречаемся с движением, которое было бы результатом наложения этих двух форм, но это не значит, что его не существует. Из этой д и- леммы возник совершенно новый подход к описанию физических
ихимических процессов микромира.
В1924 г. Луи де Бройль выдвинул гипотезу о том, что корпус-
кулярно-волновой дуализм присущ не только электромагнитному излучению, а является общим свойством материи. При этом он ввел понятие о волнах материи. Так, любому материальному объ-
29

екту, обладающему массой m и движущемуся со скоростью v, соответствует волновой процесс с длиной волны λ. По аналогии с
электромагнитным излучением, где λ = h/p, длина волны частицы (часто называется длиной волны де Бройля) вычисляется по уравнению
λ= hp =mhv .
Электроны, испускаемые нагретым катодом, разгоняются в электрическом поле напряжением примерно 100 В, приобретают кинетическую энергию около 100 эВ. При этом в случае, если формула де Бройля верна, электронам должна соответствовать
длина волны λ= |
h |
. Если E =m v 2 |
, то |
λ= |
|
h |
|
. При Eк = |
|
|
|
|
|
||||||
|
mv |
к |
2 |
|
|
|
2 m Eк |
|
|
|
|
|
|
|
|
|
|||
=100 эВ λ = 1,2 Å.
Если электроны обладают волновыми свойствами, то их пучок должен испытывать дифракцию на дифракционной решетке, по-
стоянная которой α соизмерима с длиной волны электрона (постоянная решетки − сумма ширин щели и промежутка между щелями). Так как длина волны электрона мала (λ = 1,2 Å),то роль дифракционной решетки, у которой α ≈ λ, могут играть кристаллические плоскости монокристаллов. В частности, была использована металлическая фольга (никель). Причем положение дифракционных полос должно определяться условием Уильяма Брэгга:
nλ = 2α sin ϑ (n − номер дифракционной полосы; ϑ − угол, под которым пучок электронов попадает на дифракционную решетку).
Экспериментальное подтверждение волновых свойств электро-
на было получено в 1927 г. Клинтоном Девиссоном и Лестером Джермером и, независимо от них, Джоржем Томсоном (1928 г.) в
опытах по рассеянию электронов. Действительно, при пропускании пучка электронов через металлическую фольгу была получена дифракционная картина в виде концентрических колец, положение которых изменялось в зависимости от кинетической энергии электронов (ускоряющего напряжения) – их длины волны, согласно условию Брэгга (рис. 2.2). Позднее наблюдали дифракцию и более тяжелых частиц, например протонов, нейтронов, атомов гелия.
Можно предположить, что и движению макрообъекта соответствует также волновой процесс. Движению тела массой m = 1 г со
30
скоростью v = 1 см/с соответствует волновой процесс с длиной волны λ = 6,6 10-29 м. Но нет таких дифракционных решеток, чтобы наблюдать этот процесс.
|
Дифракционная |
Люминесцентный |
+ Анод |
решетка |
экран |
− Катод
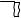 ē
ē
U
Eк = e U |
λ = |
|
h |
|
|
||
2 m e U |
Рис. 2.2. Схема опыта дифракции электронов: U (В) – напряжение ускоряющего электрического поля
Корпускулярно-волновой дуализм свойств электрона, как и других микрообъектов, является первым фундаментальным положением, на котором строится волновая механика – механика объектов атомных и субатомных размеров.
Принцип неопределенности. Вторым фундаментальным по-
ложением, на котором строится волновая механика, является принцип неопределенности Гейзенберга. Поскольку электрон обнаруживает одновременно свойства волны и частицы, возникают трудности, связанные с измерением корпускулярных свойств электрона, а именно одновременного определения координат и импульса электрона.
Вернер Гейзенберг в 1927 г. сформулировал следующее поло-
жение: для микрочастицы невозможно одновременно точно определить ее координаты и импульс. Ограничения в точности опре-
деления даются соотношением Гейзенберга:
x px ≥ , |
y py ≥ , |
z pz ≥ , ħ = h/2π – постоянная Планка. |
Из принципа неопределенности следует вероятностный подход к описанию механики микрообъектов. Точное определение координат частицы и ее импульса заменяется определением вероятности нахождения частицы в какой-то области пространства. Для движущейся частицы с вполне определенной энергией, а следовательно, и импульсом мы не можем указать точные значения коор-
31
