
- •ВВЕДЕНИЕ
- •1. ОСНОВНЫЕ ПОНЯТИЯ ХИМИИ
- •1.1. Химическая реакция
- •1.2. Классификация веществ
- •1.3. Количественные расчеты в химии
- •2. СТРОЕНИЕ АТОМА
- •2.1. Развитие представлений о строении атома
- •2.1.1. Теория строения атома Бора
- •2.1.2. Особенности описания микрочастиц
- •2.2. Основные понятия волновой механики
- •2.2.1. Волновое уравнение
- •2.2.2. Решение уравнения Шрёдингера для простейших случаев
- •2.3.1. Основное состояние атома водорода
- •2.3.2. Радиальное распределение электронной плотности. Электронная орбиталь
- •2.3.3. Возбужденные состояния атома водорода
- •2.3.4. Многоэлектронные атомы
- •2.4. Периодический закон и таблица элементов
- •2.4.1. Электронные конфигурации многоэлектронных атомов
- •2.4.2. Связь периодического закона со строением атома
- •2.4.3. Физико-химические характеристики атома
- •Контрольные вопросы
- •3. ХИМИЧЕСКАЯ СВЯЗЬ
- •3.1. Основные характеристики и классификация моделей химической связи
- •3.1.1. Основные параметры химической связи
- •3.1.2. Типы химической связи
- •3.2. Ковалентная химическая связь
- •3.2.1. Метод валентных связей
- •3.2.3. Геометрия простейших молекул. Гибридизация АО
- •3.2.4. Донорно-акцепторный механизм образования ковалентной связи
- •3.2.5. Метод молекулярных орбиталей
- •3.2.6. Полярность связи и дипольный момент молекулы
- •Контрольные вопросы
- •4. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ВЕЩЕСТВАХ
- •4.1. Межмолекулярные взаимодействия
- •4.1.2. Водородная связь
- •4.2. Химическая связь в твердом теле
- •4.2.1. Основные понятия о строении кристаллов
- •4.2.3. Ковалентные (атомные) кристаллы
- •4.2.4. Ионные кристаллы. Ионный тип химической связи
- •4.2.5. Химическая связь в металлах
- •4.2.6. Зонная модель кристаллического тела
- •4.2.7. Металлы, полупроводники и диэлектрики
- •4.2.8. Кристаллические материалы
- •4.2.9. Аморфные твердые тела
- •4.3. Химическая связь в жидкостях
- •Контрольные вопросы
- •5. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
- •5.1. Основные понятия и определения
- •5.1.1. Термодинамическая система
- •5.1.2. Термодинамический процесс
- •5.2. Тепловые эффекты физико-химических процессов
- •5.2.1. Внутренняя энергия
- •5.2.2. Первое начало термодинамики
- •5.2.3. Тепловой эффект химической реакции
- •5.2.4. Термохимические расчеты
- •5.3. Направление и пределы протекания химического процесса
- •5.3.1. Второе начало термодинамики
- •5.3.2. Энтропия
- •5.3.3. Направление химического процесса
- •5.3.4. Химический потенциал
- •Контрольные вопросы
- •6. КИНЕТИКА ХИМИЧЕСКИХ РЕАКЦИЙ
- •6.1. Механизм химической реакции
- •6.1.1. Частицы, участвующие в химической реакции
- •6.1.2. Классификация химических реакций
- •6.2. Элементарная химическая реакция
- •6.2.1. Скорость химической реакции
- •6.2.2. Зависимость скорости химической реакции от концентрации реагирующих веществ
- •6.2.3. Константа скорости химической реакции
- •6.3. Формальная кинетика гомогенных реакций
- •6.3.1. Кинетические уравнения реакций
- •6.3.2. Зависимость скорости реакции от температуры
- •6.3.3. Определение кинетических параметров реакции
- •6.4. Цепной механизм химической реакции
- •6.5. Индуцированные реакции
- •6.5.1. Фотохимические реакции
- •6.5.2. Радиационно–химические процессы
- •6.6. Макрокинетика
- •6.6.1. Гетерогенные реакции
- •6.6.2. Горение и взрыв
- •6.7. Катализ
- •6.7.1. Гомогенный катализ
- •6.7.2. Гетерогенный катализ
- •Контрольные вопросы
- •7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- •7.1. Термодинамическое условие химического равновесия
- •7.2. Кинетическое условие химического равновесия
- •7.3. Расчет равновесного состава газовой смеси
- •7.4. Равновесия в растворах
- •7.4.1. Растворы
- •7.4.2. Электролитическая диссоциация
- •7.4.3. Ионное произведение воды. Водородный показатель
- •7.4.4. Растворы кислот и оснований
- •7.4.5. Буферные растворы
- •7.4.6. Гидролиз солей
- •7.4.7. Обменные реакции с образованием осадка
- •7.5. Фазовые равновесия
- •7.5.1. Диаграмма состояния однокомпонентной системы
- •7.5.2. Диаграмма состояния двухкомпонентной системы
- •7.5.3. Кипение и кристаллизация растворов
- •7.5.4. Электролиты
- •Контрольные вопросы
- •8. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- •8.1. Основные понятия и определения
- •8.2. Электродные процессы
- •8.2.1. Скачок потенциала на границе «металл–электролит»
- •8.2.2. Уравнение Нернста
- •8.2.3. Электроды
- •8.3. Неравновесные электрохимические системы
- •8.3.1. Гальванический элемент
- •8.3.2. Окислительно-восстановительные реакции в водных растворах
- •8.3.3. Электролиз
- •8.4. Кинетика электрохимических процессов
- •8.4.1. Скорость электрохимических процессов
- •8.4.2. Поляризация электродов
- •8.5. Практическое использование электрохимических процессов
- •8.5.1. Химические источники тока
- •8.5.2. Применение электролиза
- •Контрольные вопросы
- •9. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- •9.1. Коррозионные процессы
- •9.2. Химическая коррозия
- •9.2.1. Высокотемпературная газовая коррозия
- •9.2.2. Кинетика роста оксидных пленок
- •9.2.3. Факторы, влияющие на скорость газовой коррозии
- •9.3. Электрохимическая коррозия
- •9.3.1. Анодные и катодные реакции
- •9.3.2. Термодинамические условия электрохимической коррозии металлов
- •9.3.3. Факторы, влияющие на скорость электрохимической коррозии
- •9.4. Коррозионные среды и влияние дополнительных факторов
- •9.4.1. Коррозионно-механическое разрушение металлов
- •9.4.2. Водородная коррозия
- •9.4.3. Радиационная коррозия
- •Контрольные вопросы
- •Библиографический список
4.2.Химическая связь в твердом теле
Втвердом состоянии вещества образующие его частицы находятся в фиксированных положениях в пространстве, вокруг которых они совершают колебательные и вращательные движения. Различают кристаллические и аморфные твердые тела. В кристаллах существует пространственная периодичность в равновесных положениях частиц, а в аморфных частицы колеблются около хаотически расположенных точек.
4.2.1.Основные понятия о строении кристаллов
Кристалл – тело, которое вследствие строго определенного внутреннего строения имеет самопроизвольно образующуюся форму, ограниченную плоскими гранями. Для кристаллов характерны правильные формы и симметрия. Атомы, образующие кристалл, располагаются строго определенным образом, соответствующим состоянию с минимумом энергии. Закономерности этого расположения определяются типом химических связей, существующих между атомами, и в известном смысле кристалл можно рассматривать как одну «большую молекулу».
В зависимости от характера химической связи между частицами, образующими кристаллы, они подразделяются на четыре типа:
молекулярные, ковалентные, ионные, металлические.
Для многих кристаллических веществ минимум энергии системы достигается при таком взаимном расположении частиц в пространстве, которое соответствует плотнейшей упаковке твердых шаров.
В плоскости твердые шары располагаются плотнейшим образом, если каждый шар окружают шесть соседей. Второй слой шаров помещается во впадины, образованные тремя соприкасающимися шарами. При укладке третьего слоя появляются два возможных варианта плотнейшей упаковки, поскольку имеется два различных типа впадин: впадины над центрами шаров первого слоя и впадины над пустотами первого слоя (рис. 4.3):
1) гексагональная (ГПУ). Шары третьего слоя помещаются во впадины, которые находятся над центрами шаров первого слоя. Расположение слоев по вертикали повторяется в последовательности 1,2,1,2,... Позиции шаров повторяются в нечетных и четных слоях;
100
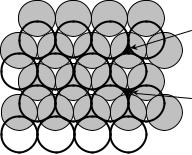
2) кубическая (КПУ). Шары третьего слоя помещаются во впадины, которые располагаются над пустотами первого слоя. Расположение слоев по вертикали повторяется в последовательности
1,2,3,1,2,3,..
ГПУ
КПУ
1
2
Рис. 4.3. Первые два слоя плотнейшей упаковки шаров
При плотнейшей упаковке шаров в кристалле образуются пустоты двух типов: тетраэдрические – между четырьмя сферами, и октаэдрические – между шестью сферами. Пустоты играют важную роль в процессах диффузии и образования дефектов кристаллов. Если кристалл, например (Na+Cl-), состоит из частиц разного
размера, то частицы крупного размера (rCl– = 1,81Å) образуют
плотнейшую упаковку, а частицы меньшего размера (rNa+ = =0,95Å) располагаются в пустотах.
Прямые линии, мысленно проведенные через центры частиц, создают так называемую кристаллическую решетку. Точки пересечения этих линий называются узлами кристаллической решетки, в которых располагаются образующие ее частицы. Кристаллическую решетку можно охарактеризовать элементарной ячейкой, которая представляет собой минимальный фрагмент решетки, полностью отражающий ее геометрию и чередование частиц в кристалле (рис. 4.4).
Элементарная ячейка является структурной единицей кристалла, ее параллельным переносом можно построить кристаллическую решетку. В трехмерном пространстве элементарная ячейка представляет собой варианты параллелепипеда с различным соотношением ребер и углов между ними.
101

a=b=c
α=β=γ=90
Рис. 4.4. Кристаллическая решетка и ее элементарная ячейка
Размеры элементарной ячейки называются постоянными решетки. В зависимости от равенства или неравенства этих углов между собой различают семь классов (сингоний) и 14 типов элементарных ячеек, которым соответствуют кристаллические решет-
ки. Самая несимметричная решетка – триклинная (a≠b≠c, α≠β≠
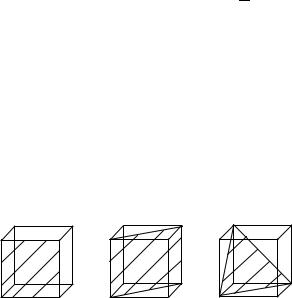
≠γ≠90°), а самая симметричная – кубическая, для которой возможны три варианта элементарной ячейки: простейшая кубическая решетка – ПК, кубическая объемно-центрированная решетка – ОЦК и кубическая гранецентрированная решетка – ГЦК (рис. 4.5).
ПК ОЦК ГЦК
102
соответствие плоскостей поверхности тела кристаллографическим плоскостям. Плоскости, мысленно проведенные через узлы решетки, называются кристаллографическими. Ряд параллельных кристаллографических плоскостей обозначают индексами Миллера, которые определяют следующим образом. Находят пересечение плоскости с осями координат, соответствующих элементарной ячейке (оси координат направлены вдоль ребер, углы между ними
равны α, β, γ). Отрезки, отсекаемые плоскостью на осях, измеряют в длинах ребер элементарной ячейки (x, y, z). Затем обратные значения этих величин умножают на соответствующие числа так, чтобы получить три наименьших возможных целых числа, кото-
рые и называются индексами Миллера (h, k, l): 1x: 1y :1z =h:k:l .
Вследствие симметрии кристаллической решетки отдельные плоскости образуют группы эквивалентных плоскостей. Например, равнозначными в кубических кристаллах являются плоскости (100), (010), (001),… Группа эквивалентных плоскостей обознача-
ется {100}.
Направление в кристалле определяется индексами Миллера [h, k, l] плоскости, перпендикулярной к заданному направлению.
В кубических кристаллах основными кристаллографическими плоскостями являются (1,0,0) – грань куба, (1,1,0) – диагональная плоскость куба, проходящая через два ребра, (1,1,1) – диагональная плоскость, проходящая через три вершины (рис. 4.6).
|
1 |
|
|
0 |
1 |
|
|
|
1 |
(100) |
|
|
|
|
1 |
|
|
0 |
1 |
|
|
|
1 |
(110) |
|
|
|
|
1 |
|
|
0 |
1 |
|
|
|
1 |
(111) |
|
|
|
103
