
- •ВВЕДЕНИЕ
- •1. ОСНОВНЫЕ ПОНЯТИЯ ХИМИИ
- •1.1. Химическая реакция
- •1.2. Классификация веществ
- •1.3. Количественные расчеты в химии
- •2. СТРОЕНИЕ АТОМА
- •2.1. Развитие представлений о строении атома
- •2.1.1. Теория строения атома Бора
- •2.1.2. Особенности описания микрочастиц
- •2.2. Основные понятия волновой механики
- •2.2.1. Волновое уравнение
- •2.2.2. Решение уравнения Шрёдингера для простейших случаев
- •2.3.1. Основное состояние атома водорода
- •2.3.2. Радиальное распределение электронной плотности. Электронная орбиталь
- •2.3.3. Возбужденные состояния атома водорода
- •2.3.4. Многоэлектронные атомы
- •2.4. Периодический закон и таблица элементов
- •2.4.1. Электронные конфигурации многоэлектронных атомов
- •2.4.2. Связь периодического закона со строением атома
- •2.4.3. Физико-химические характеристики атома
- •Контрольные вопросы
- •3. ХИМИЧЕСКАЯ СВЯЗЬ
- •3.1. Основные характеристики и классификация моделей химической связи
- •3.1.1. Основные параметры химической связи
- •3.1.2. Типы химической связи
- •3.2. Ковалентная химическая связь
- •3.2.1. Метод валентных связей
- •3.2.3. Геометрия простейших молекул. Гибридизация АО
- •3.2.4. Донорно-акцепторный механизм образования ковалентной связи
- •3.2.5. Метод молекулярных орбиталей
- •3.2.6. Полярность связи и дипольный момент молекулы
- •Контрольные вопросы
- •4. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ВЕЩЕСТВАХ
- •4.1. Межмолекулярные взаимодействия
- •4.1.2. Водородная связь
- •4.2. Химическая связь в твердом теле
- •4.2.1. Основные понятия о строении кристаллов
- •4.2.3. Ковалентные (атомные) кристаллы
- •4.2.4. Ионные кристаллы. Ионный тип химической связи
- •4.2.5. Химическая связь в металлах
- •4.2.6. Зонная модель кристаллического тела
- •4.2.7. Металлы, полупроводники и диэлектрики
- •4.2.8. Кристаллические материалы
- •4.2.9. Аморфные твердые тела
- •4.3. Химическая связь в жидкостях
- •Контрольные вопросы
- •5. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
- •5.1. Основные понятия и определения
- •5.1.1. Термодинамическая система
- •5.1.2. Термодинамический процесс
- •5.2. Тепловые эффекты физико-химических процессов
- •5.2.1. Внутренняя энергия
- •5.2.2. Первое начало термодинамики
- •5.2.3. Тепловой эффект химической реакции
- •5.2.4. Термохимические расчеты
- •5.3. Направление и пределы протекания химического процесса
- •5.3.1. Второе начало термодинамики
- •5.3.2. Энтропия
- •5.3.3. Направление химического процесса
- •5.3.4. Химический потенциал
- •Контрольные вопросы
- •6. КИНЕТИКА ХИМИЧЕСКИХ РЕАКЦИЙ
- •6.1. Механизм химической реакции
- •6.1.1. Частицы, участвующие в химической реакции
- •6.1.2. Классификация химических реакций
- •6.2. Элементарная химическая реакция
- •6.2.1. Скорость химической реакции
- •6.2.2. Зависимость скорости химической реакции от концентрации реагирующих веществ
- •6.2.3. Константа скорости химической реакции
- •6.3. Формальная кинетика гомогенных реакций
- •6.3.1. Кинетические уравнения реакций
- •6.3.2. Зависимость скорости реакции от температуры
- •6.3.3. Определение кинетических параметров реакции
- •6.4. Цепной механизм химической реакции
- •6.5. Индуцированные реакции
- •6.5.1. Фотохимические реакции
- •6.5.2. Радиационно–химические процессы
- •6.6. Макрокинетика
- •6.6.1. Гетерогенные реакции
- •6.6.2. Горение и взрыв
- •6.7. Катализ
- •6.7.1. Гомогенный катализ
- •6.7.2. Гетерогенный катализ
- •Контрольные вопросы
- •7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- •7.1. Термодинамическое условие химического равновесия
- •7.2. Кинетическое условие химического равновесия
- •7.3. Расчет равновесного состава газовой смеси
- •7.4. Равновесия в растворах
- •7.4.1. Растворы
- •7.4.2. Электролитическая диссоциация
- •7.4.3. Ионное произведение воды. Водородный показатель
- •7.4.4. Растворы кислот и оснований
- •7.4.5. Буферные растворы
- •7.4.6. Гидролиз солей
- •7.4.7. Обменные реакции с образованием осадка
- •7.5. Фазовые равновесия
- •7.5.1. Диаграмма состояния однокомпонентной системы
- •7.5.2. Диаграмма состояния двухкомпонентной системы
- •7.5.3. Кипение и кристаллизация растворов
- •7.5.4. Электролиты
- •Контрольные вопросы
- •8. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- •8.1. Основные понятия и определения
- •8.2. Электродные процессы
- •8.2.1. Скачок потенциала на границе «металл–электролит»
- •8.2.2. Уравнение Нернста
- •8.2.3. Электроды
- •8.3. Неравновесные электрохимические системы
- •8.3.1. Гальванический элемент
- •8.3.2. Окислительно-восстановительные реакции в водных растворах
- •8.3.3. Электролиз
- •8.4. Кинетика электрохимических процессов
- •8.4.1. Скорость электрохимических процессов
- •8.4.2. Поляризация электродов
- •8.5. Практическое использование электрохимических процессов
- •8.5.1. Химические источники тока
- •8.5.2. Применение электролиза
- •Контрольные вопросы
- •9. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- •9.1. Коррозионные процессы
- •9.2. Химическая коррозия
- •9.2.1. Высокотемпературная газовая коррозия
- •9.2.2. Кинетика роста оксидных пленок
- •9.2.3. Факторы, влияющие на скорость газовой коррозии
- •9.3. Электрохимическая коррозия
- •9.3.1. Анодные и катодные реакции
- •9.3.2. Термодинамические условия электрохимической коррозии металлов
- •9.3.3. Факторы, влияющие на скорость электрохимической коррозии
- •9.4. Коррозионные среды и влияние дополнительных факторов
- •9.4.1. Коррозионно-механическое разрушение металлов
- •9.4.2. Водородная коррозия
- •9.4.3. Радиационная коррозия
- •Контрольные вопросы
- •Библиографический список
K ≠ = |
CABС≠ |
, |
С |
|
≠ =K ≠C |
C . |
|
|
|||||
C |
CABCC |
|
|
ABС |
C |
AB C |
|
|
|
|
|
||
|
|
|
|
|
|
Тогда скорость реакции АВ + С → А + ВС будет описываться выражением v =χ kTh KC≠ CABCC . Согласно закону действующих
масс v =k CAB CC , следовательно, константа скорости реакции k =χ kTh KC≠ .
Константу равновесия можно определить через изменение термодинамических функций реакции образования активированного комплекса (реакция протекает при постоянных давлении и темпе-
|
|
p0 |
∆ν |
|
ратуре). Поскольку K ≠ =K 0≠ |
|
|
(в данном примере ∆ν= –1), а |
|
|
||||
C |
|
|
|
|
|
|
RT |
|
|
K 0≠ =e |
− |
∆G≠ |
|
− |
∆H ≠−T ∆S ≠ |
|
− |
Eак ∆S ≠ |
|||
|
|
|
|
|
|
|
|||||
RT |
=e |
RT |
=e |
RT e |
R , |
||||||
|
|
|
|||||||||
где ∆G≠ – изменение энергии Гиббса; ∆H≠ – изменение энтальпии,
которое и является фактически энергией активации; ∆S≠ – изменение энтропии при образовании активированного комплекса, то
k =χ kT |
|
p0 |
∆S ≠ |
e− |
Eак |
||
( |
)∆νe R |
RT |
. |
||||
RT |
|||||||
h |
|
|
|
|
|
||
Сравнение уравнения Аррениуса и формулы для расчета константы скорости по теории переходного состояния:
|
Eак |
|
p0 |
∆S ≠ |
|
Eак |
||
k =k0e− |
|
=χ kT |
|
)∆νe R |
e− |
|
||
RT |
( |
RT |
||||||
RT |
||||||||
|
|
h |
|
|
|
|
||
дает возможность оценить значение предэкспоненциального множителя (k0).
6.3. Формальная кинетика гомогенных реакций
Большинство гомогенных реакций имеют сложный механизм и протекают через ряд последовательных стадий, каждая из которых представляет собой моно-, биили тримолекулярную элементарную реакцию. Как правило, скорость превращения промежуточных веществ велика. Общая скорость реакции будет определяться
185
скоростью самой медленной стадии (лимитирующая стадия сложной химической реакции). В этом случае зависимость скорости сложной реакции от концентрации реагирующих веществ может быть описана законом действующих масс. Такие сложные реакции называются формально простыми. Но показатели степени в общем случае не равны стехиометрическим коэффициентам. Так,
для формально простой гомогенной реакции νAA + νBB → νDD + +νEE зависимость скорости реакции от концентрации реагентов определяется уравнением
v =kC xC y |
x≠νA; y≠νB. |
A B |
|
Такое уравнение называется кинетическим уравнением реакции.
П р и м е р. Экспериментально определенное кинетическое
уравнение реакции взаимодействия иодистого водорода с переки- |
||
|
ν |
|
сью водорода 2HI + H2O2 → 2H2O + I2 имеет вид |
=kCHI1 CH1 |
2O2 . |
Показатели степени в данном случае называются порядком реакции. Каждый из показателей степеней (x; y) называется порядком реакции по соответствующему компоненту, а сумма всех показателей (x + y) – кинетическим порядком реакции. Порядок реакций по компонентам определяется экспериментально.
В общем случае кинетический порядок реакции и порядок по компонентам может быть целым или дробным числом. В некоторых случаях, например в фотохимических реакциях, скорость реакции не зависит от концентрации реагирующих веществ и порядок реакции является нулевым.
Отметим, что для элементарных реакций молекулярность реакции и кинетический порядок численно совпадают, а порядок по компонентам совпадает со стехиометрическими коэффициентами в уравнении реакции. Также необходимо отметить, что в этом случае определение скорости реакции как числа элементарных актов в единицу времени в единице реакционного пространства теряет физический смысл. Для формально простых реакций скорость определяется через изменение количества исходных веществ и продуктов реакции в единицу времени.
При протекании химической реакции происходит превращение одних веществ в другие, в ходе которого количество исходных веществ уменьшается, а количество продуктов реакции возрастает.
Изменение количества i-го вещества (∆νi − число молей) в единицу
186

времени (∆t) в единице реакционного пространства (R) называется скоростью реакции по i-му компоненту (скоростью образования или расходования i-го вещества):
v i =± |
1 |
|
∆νi |
при ∆t→0 v i =± |
1 |
|
dνi |
. |
R |
∆t |
R |
|
|||||
|
|
|
|
dt |
||||
Изменение числа молей ∆νi продуктов реакции положительно, а исходных веществ отрицательно. Изменения количеств каждого из реагентов не являются независимыми, а связаны между собою сте-
хиометрическими коэффициентами. Так, для реакции νAA + νBB →
→νDD + νEE
−∆νA =−∆νB =+∆νD =+∆νE .
νA νB νD νE
Следовательно, величина v i =± |
1 |
|
1 |
|
dνi |
не зависит от выбора |
|
νi |
R |
|
dt |
|
|
реагента, изменение количества которого во времени наблюдают. Таким образом, она однозначно характеризует скорости превращения всех веществ в ходе химической реакции – скорость реакции в целом.
Практический интерес представляет изменение концентрации реагирующих веществ во времени (зависимость C = f(t)).
Поскольку скорость реакции является первой производной изменения концентрации во времени, то кинетическое уравнение есть дифференциальное уравнение, решением которого и является
функция C = f(t):
v =−dCdti =kCAxCBy .
6.3.1. Кинетические уравнения реакций
Кинетическое уравнение необратимой реакции первого по-
рядка. Рассмотрим необратимую (одностороннюю) реакцию распада:
A → B + D.
Кинетическое уравнение:
−ddtСA =kСA .
187
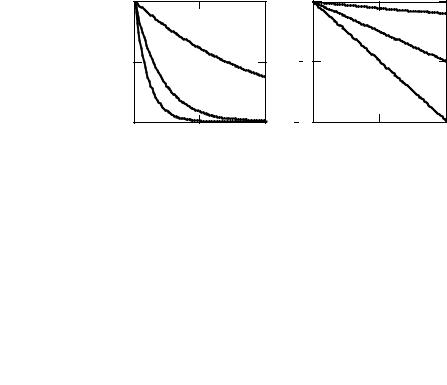
Начальные условия – концентрация вещества А в начальный момент времени (t = 0) равна CA0.
Уравнения данного типа решаются методом разделения переменных:
− |
dСA |
|
=kСA → |
dСA |
=−kdt → ∫ |
dСA |
=−k ∫dt , lnСA =−kt +const , |
dt |
|
|
|||||
|
|
СA |
СA |
||||
при t = 0 |
C = CA0 lnСA0 =const , |
lnСA =−kt +lnСA0 , СA =СA0e−k t . |
|||||
Поскольку концентрация вещества А уменьшается в ходе реакции (рис. 6.4) и асимптотически приближается к нулю, рассчитать точно время полного превращения вещетва А невозможно. Для оценки времени протекания реакции используется такая характе-
ристика, как время полупревращения (полураспада) – время, за ко-
торое прореагировала половина исходного вещества, т. е. концен-
трация вещества А уменьшилась в два раза (СA(t1 )= 12 СA0 ):
2
|
|
|
t1 = |
1 |
ln2 . |
|
|
|
|
|
2 |
k |
|
|
|
CA |
|
|
|
lnCA |
|
|
|
|
|
|
|
|
|
||
1 |
|
|
|
|
0 |
|
|
|
|
|
|
|
|
k=0,1 |
|
|
|
k=0,1 |
|
|
|
k=0,5 |
|
0.5 |
|
|
|
|
5 |
|
|
|
|
|
|
|
|
||
|
|
k=0,5 |
|
|
|
k=1 |
|
|
|
k=1 |
10 t |
|
|
|
10 t |
0 |
0 |
5 |
|
10 0 |
5 |
Рис. 6.4. Изменение концентрации вещества А во времени при протекании односторонней реакции первого порядка (CA0 = 1)
Время полупревращения для реакций первого порядка не зависит от исходной концентрации вещества, а определяется только величиной константы скорости.
Кинетическое уравнение необратимой реакции второго по-
рядка. К необратимым реакциям второго порядка относятся химические реакции типа
A + A → A2, A + B → AB, A + BС → AB + С.
188
Рассмотрим как наиболее простую первую реакцию. Ее кинетическое уравнение:
− ddtСA =kСA2 .
Начальные условия – концентрация вещества А в начальный момент времени (t = 0) равна CA0:
− dCA |
=kCA2 |
, |
dCA |
=−kdt , |
∫dCA =−k∫dt , |
1 |
=kt +const , |
||||||||
dt |
|
|
|
CA2 |
|
CA2 |
|
|
|
CA |
|
|
|
||
при t = 0; С = СA0 |
|
1 |
=const , |
1 |
=kt + |
1 |
, |
CA = |
CA0 |
|
. |
||||
|
CA0 |
CA |
CA0 |
CA0kt |
+1 |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
C A |
|
|
|
|
|
|
|
1/C A |
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|
|
|
|
|
k= 0,1 |
|
|
|
|
k= 1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
k= 0,5 |
|
|
||
0.5 |
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
k= 0,5 |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
k= 1 |
|
|
|
|
|
|
|
|
|
|
k= 0,1 |
|
|
0 |
0 |
|
|
10 |
|
20 |
|
0 |
0 |
|
|
10 |
|
20 |
|
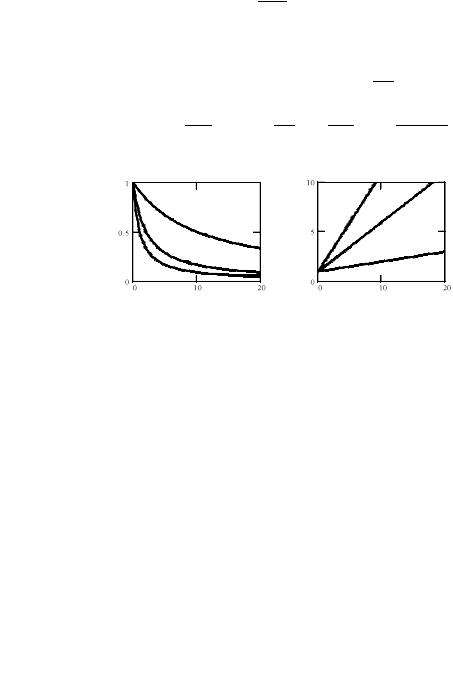
Рис. 6.5. Изменение концентрации вещества А во времени при протекании реакции второго порядка (CA0 = 1)
Зависимость концентрации вещества от времени для реакций
второго порядка (рис. 6.5) линейна в координатах |
1 |
– t, при- |
|
CA (t) |
|||
|
|
чем тангенс угла наклона равен константе скорости реакции. Время полупревращения для реакций второго порядка зависит
от исходной концентрации вещества А:
t1 |
= |
1 |
|
1 |
. |
k |
|
||||
2 |
|
|
cA0 |
||
Реакции нулевого порядка. Скорость реакций нулевого порядка не зависит от концентраций реагентов и определяется другими лимитирующими факторами, например площадью поверхности катализатора (в реакциях гетерогенного катализа) или поглощением света (в фотохимических реакциях):
189

− dCdti =kCAxCBy ... , x+ y +…= 0.
Кинетическое уравнение реакций нулевого порядка имеет вид
−dCdti =k .
Изменение концентрации реагирующих веществ во времени будет описываться уравнением
C(t)i =C0i −kt .
Время полупревращения t1 =C20ki .
2
Кинетическое уравнение обратимой реакции первого поряд-
ка. Изменение концентрации исходных веществ и продуктов реакции во времени в случае протекания обратимой (двусторонней) реакции можно показать на примере реакции первого порядка:
А ↔ В.
Согласно закону действующих масс скорость прямой и обратной реакций будут описываться уравнениями
→ |
→ |
← |
← |
v |
=−dCA = k C1А, |
v |
=−dCB = k C1B . |
|
dt |
|
dt |
Изменение концентраций исходного вещества А и продукта В определяется разностью скоростей прямого и обратного процессов:
dCA ← 1 → 1 dt = k CB − k CА ,
dCB → 1 ← 1 dt = k CА − k CB .
Кинетические уравнения содержат три переменные: CA, CB и t. Для интегрирования одну необходимо исключить. Это можно сделать на основе материального баланса. Пусть в начальный момент времени при t=0 концентрация исходного вещества А равняется C0A, а концентрация продукта В – C0B, к моменту времени t согласно уравнению реакции концентрации реагентов изменятся на величину x: CA = CA0 – x, CB= CB0 + x. Тогда
|
d(CA0 −x) |
← |
|
→ |
|
d(CB0 +x) |
→ |
← |
|
|
|
= k (CB0 |
+x)−k (CA0 −x) , |
|
|
= k (CA0 |
−x)− k (CB0 |
+x) , |
|
|
dt |
|
dt |
||||||
|
|
|
|
|
|
|
|
||
и соответственно |
← |
|
→ |
→ ← |
|
|
|||
dx =−( k CB0 |
− k CA0 )−x(k +k ) . |
|
|
||||||
|
|
|
|
dt |
|
|
|
|
|
Учитывая, что при t = 0 x = 0, решением уравнения будет
190
|
← |
|
→ |
|
|
→ ← |
|
|
|
k CB0 − k CA0 |
|
|
|
||||
x= |
[exp(−(k + k )t)−1] . |
|
||||||
|
→ ← |
|
||||||
|
|
k |
+ k |
|
|
|
|
|
|
|
|
← |
→ |
|
→ ← |
|
|
|
|
|
k CB0 − k CA0 |
|
||||
Следовательно, СA =CA0 − |
[exp(−( k + k )t)−1] |
, |
||||||
→ ← |
|
|||||||
|
|
|
k + k |
|
|
|
||
|
|
← |
→ |
|
|
→ ← |
|
|
|
|
k CB0 − k CA0 |
|
|
||||
СB =CB0 + |
[exp(−( k + k )t)−1]. |
|
||||||
|
→ ← |
|
|
|||||
|
|
|
k + k |
|
|
|
|
|
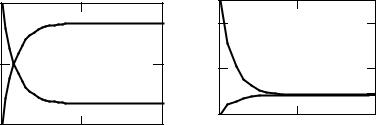
Изменение концентрации веществ А и В во времени приведено на рис. 6.6.
C(t) |
|
|
|
|
v(t) |
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
0 .5 |
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
0 |
0 |
|
1 |
2 t |
0 0 |
1 |
2 t |
|
|
|
|
|
|||
Рис. 6.6. Изменение концентрации ве- |
Рис. 6.7. Изменение во времени скоро- |
||||||
ществ А и В во времени при протека- |
стей прямой и обратной реакций пер- |
||||||
нии обратимой реакции первого поряд- |
|
→ |
← |
||||
|
|
→ |
← |
|
вого порядка А ↔ В: k |
= 5; k =1; |
|
ка А ↔ В. |
k |
= 5;k =1; C0A=1; |
C0B=0 |
|
C0A = 1; C0B = 0 |
||
По достижении равенства скоростей прямой и обратной реакции (рис. 6.7) концентрации исходного вещества и продукта изменяться не будут (в данном примере САр = 0,167; СВр = 0,833), система придет в состояние равновесия.
Кинетические уравнения последовательных и параллельных реакций. Принцип независимости протекания реакций заключается в том, что если в системе происходит несколько элементарных реакций, то каждая из них протекает по тем же законам, как и в отсутствие других реакций. Следовательно, если в нескольких реакциях участвует одно и то же вещество, то изменение его концен-
191
трации будет равно алгебраической сумме скоростей каждой реакции, умноженной на стехиометрический коэффициент этого вещества в данной реакции.
В случае последовательных реакций вещество, образующееся в первой реакции, является исходным для другой. Например, последовательная односторонняя реакция первого порядка:
k1 k2
|
|
|
|
|
A → B → D. |
|
|
|
|
|
|
|
|
|
|||||
Система кинетических уравнений для нее: |
|
|
|
|
|
|
|
|
|||||||||||
dCA =−k C |
A |
, |
dCB =k C |
A |
−k |
2 |
C |
B |
, |
dCD =k |
2 |
C |
B |
. |
|
||||
dt |
1 |
|
dt |
1 |
|
|
|
dt |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Результаты |
численного |
решения |
уравнений |
приведены |
на |
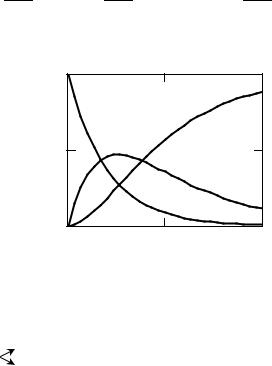
||||||||||||||
рис.6.8. |
C(t) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CA |
|
|
|
CD |
|
|
|
|
|
|
|
|
|
|
|
|
|
0.5 |
|
|
CB |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 0 |
|
|
|
|
|
5 |
|
|
|
|
|
|
10 t |
|
|
|
|
|
Рис. 6.8. Зависимость концентрации исходного (CA) промежуточного (CB) |
|
||||||||||||||||||
и конечного (CD) веществ от времени для последовательной односторонней |
|
||||||||||||||||||
реакции первого порядка (k1 = 0,5; k2 = 0,3; C0A=1) |
|
|
|
|
|
||||||||||||||
В случае параллельных реакций одно вещество является исходным для нескольких реакций. Например, две реакции первого по-
рядка: |
k1 |
B |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
A |
D |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
k2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Система кинетических уравнений в этом случае будет иметь |
||||||||||||||||||||||
вид |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
dCA |
=−k C |
A |
−k |
C |
A |
=−(k +k |
2 |
)C |
A |
, |
dCB |
=k C |
A |
, |
dCD |
=k |
C |
A |
. |
||
|
|
|
|
|
||||||||||||||||||
|
|
dt |
1 |
2 |
|
1 |
|
|
dt |
1 |
|
dt |
2 |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Аналогичным образом составляется система дифференциальных кинетических уравнений и для более сложных реакций. На-
192
