
- •ВВЕДЕНИЕ
- •1. ОСНОВНЫЕ ПОНЯТИЯ ХИМИИ
- •1.1. Химическая реакция
- •1.2. Классификация веществ
- •1.3. Количественные расчеты в химии
- •2. СТРОЕНИЕ АТОМА
- •2.1. Развитие представлений о строении атома
- •2.1.1. Теория строения атома Бора
- •2.1.2. Особенности описания микрочастиц
- •2.2. Основные понятия волновой механики
- •2.2.1. Волновое уравнение
- •2.2.2. Решение уравнения Шрёдингера для простейших случаев
- •2.3.1. Основное состояние атома водорода
- •2.3.2. Радиальное распределение электронной плотности. Электронная орбиталь
- •2.3.3. Возбужденные состояния атома водорода
- •2.3.4. Многоэлектронные атомы
- •2.4. Периодический закон и таблица элементов
- •2.4.1. Электронные конфигурации многоэлектронных атомов
- •2.4.2. Связь периодического закона со строением атома
- •2.4.3. Физико-химические характеристики атома
- •Контрольные вопросы
- •3. ХИМИЧЕСКАЯ СВЯЗЬ
- •3.1. Основные характеристики и классификация моделей химической связи
- •3.1.1. Основные параметры химической связи
- •3.1.2. Типы химической связи
- •3.2. Ковалентная химическая связь
- •3.2.1. Метод валентных связей
- •3.2.3. Геометрия простейших молекул. Гибридизация АО
- •3.2.4. Донорно-акцепторный механизм образования ковалентной связи
- •3.2.5. Метод молекулярных орбиталей
- •3.2.6. Полярность связи и дипольный момент молекулы
- •Контрольные вопросы
- •4. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ВЕЩЕСТВАХ
- •4.1. Межмолекулярные взаимодействия
- •4.1.2. Водородная связь
- •4.2. Химическая связь в твердом теле
- •4.2.1. Основные понятия о строении кристаллов
- •4.2.3. Ковалентные (атомные) кристаллы
- •4.2.4. Ионные кристаллы. Ионный тип химической связи
- •4.2.5. Химическая связь в металлах
- •4.2.6. Зонная модель кристаллического тела
- •4.2.7. Металлы, полупроводники и диэлектрики
- •4.2.8. Кристаллические материалы
- •4.2.9. Аморфные твердые тела
- •4.3. Химическая связь в жидкостях
- •Контрольные вопросы
- •5. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
- •5.1. Основные понятия и определения
- •5.1.1. Термодинамическая система
- •5.1.2. Термодинамический процесс
- •5.2. Тепловые эффекты физико-химических процессов
- •5.2.1. Внутренняя энергия
- •5.2.2. Первое начало термодинамики
- •5.2.3. Тепловой эффект химической реакции
- •5.2.4. Термохимические расчеты
- •5.3. Направление и пределы протекания химического процесса
- •5.3.1. Второе начало термодинамики
- •5.3.2. Энтропия
- •5.3.3. Направление химического процесса
- •5.3.4. Химический потенциал
- •Контрольные вопросы
- •6. КИНЕТИКА ХИМИЧЕСКИХ РЕАКЦИЙ
- •6.1. Механизм химической реакции
- •6.1.1. Частицы, участвующие в химической реакции
- •6.1.2. Классификация химических реакций
- •6.2. Элементарная химическая реакция
- •6.2.1. Скорость химической реакции
- •6.2.2. Зависимость скорости химической реакции от концентрации реагирующих веществ
- •6.2.3. Константа скорости химической реакции
- •6.3. Формальная кинетика гомогенных реакций
- •6.3.1. Кинетические уравнения реакций
- •6.3.2. Зависимость скорости реакции от температуры
- •6.3.3. Определение кинетических параметров реакции
- •6.4. Цепной механизм химической реакции
- •6.5. Индуцированные реакции
- •6.5.1. Фотохимические реакции
- •6.5.2. Радиационно–химические процессы
- •6.6. Макрокинетика
- •6.6.1. Гетерогенные реакции
- •6.6.2. Горение и взрыв
- •6.7. Катализ
- •6.7.1. Гомогенный катализ
- •6.7.2. Гетерогенный катализ
- •Контрольные вопросы
- •7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- •7.1. Термодинамическое условие химического равновесия
- •7.2. Кинетическое условие химического равновесия
- •7.3. Расчет равновесного состава газовой смеси
- •7.4. Равновесия в растворах
- •7.4.1. Растворы
- •7.4.2. Электролитическая диссоциация
- •7.4.3. Ионное произведение воды. Водородный показатель
- •7.4.4. Растворы кислот и оснований
- •7.4.5. Буферные растворы
- •7.4.6. Гидролиз солей
- •7.4.7. Обменные реакции с образованием осадка
- •7.5. Фазовые равновесия
- •7.5.1. Диаграмма состояния однокомпонентной системы
- •7.5.2. Диаграмма состояния двухкомпонентной системы
- •7.5.3. Кипение и кристаллизация растворов
- •7.5.4. Электролиты
- •Контрольные вопросы
- •8. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- •8.1. Основные понятия и определения
- •8.2. Электродные процессы
- •8.2.1. Скачок потенциала на границе «металл–электролит»
- •8.2.2. Уравнение Нернста
- •8.2.3. Электроды
- •8.3. Неравновесные электрохимические системы
- •8.3.1. Гальванический элемент
- •8.3.2. Окислительно-восстановительные реакции в водных растворах
- •8.3.3. Электролиз
- •8.4. Кинетика электрохимических процессов
- •8.4.1. Скорость электрохимических процессов
- •8.4.2. Поляризация электродов
- •8.5. Практическое использование электрохимических процессов
- •8.5.1. Химические источники тока
- •8.5.2. Применение электролиза
- •Контрольные вопросы
- •9. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- •9.1. Коррозионные процессы
- •9.2. Химическая коррозия
- •9.2.1. Высокотемпературная газовая коррозия
- •9.2.2. Кинетика роста оксидных пленок
- •9.2.3. Факторы, влияющие на скорость газовой коррозии
- •9.3. Электрохимическая коррозия
- •9.3.1. Анодные и катодные реакции
- •9.3.2. Термодинамические условия электрохимической коррозии металлов
- •9.3.3. Факторы, влияющие на скорость электрохимической коррозии
- •9.4. Коррозионные среды и влияние дополнительных факторов
- •9.4.1. Коррозионно-механическое разрушение металлов
- •9.4.2. Водородная коррозия
- •9.4.3. Радиационная коррозия
- •Контрольные вопросы
- •Библиографический список
труднее, чем молекулярного, но легче, чем атомного (механическая прочность, плавление).
|
|
Т а б л и ц а 4.3 |
Кристалл |
Энергия кристаллической решетки, кДж/моль |
|
|
эксперимент |
уравнение Борна |
NaCl |
757,8 |
749,1 |
NaBr |
744,0 |
712,7 |
NaI |
693,9 |
667,1 |
Таким образом, силы взаимодействия, определяющие ионную связь, характеризуются следующими свойствами: ненасыщенностью, ненаправленностью, дальнодействием. Поэтому координационное число в ионных кристаллах определяется геометрией плотнейшей упаковки. Например, в кубической простой решетке КЧ=6, в объемно-центрированной КЧ=8, а в гранецентрированной КЧ=12.
4.2.5. Химическая связь в металлах
Металлические кристаллы – металлы – отличаются от других прежде всего физическими свойствами. Они имеют характерный металлический блеск, высокую электро- и теплопроводность, способность легко пластически деформироваться без разрушения. Эти свойства определяются особым типом химической связи между атомами.
Кристаллическая решетка металлов, как правило, является плотной упаковкой (КПУ или ГПУ) атомов. Элементарная ячейка
– кубическая гранецентрированная (КЧ=12), кубическая объемноцентрированная (КЧ=8) или гексагональная (КЧ=12).
Такое строение кристалла характерно для веществ с ионной связью или межмолекулярным взаимодействием между частицами. Модель ионной связи не может быть использована, поскольку в узлах кристаллической решетки находятся одинаковые атомы с равной электроотрицательностью. Химическая связь между частицами за счет межмолекулярного взаимодействия не согласуется с экспериментальными данными по энергии, порядок величины которой характерен для ионных или ковалентных кристаллов. В то же время классическая модель ковалентной связи между атомами металла в кристаллической решетке не согласуется со значительно большим числом ближайших соседей (КЧ = 8÷12), чем число ва-
109
лентных электронов. Следовательно, химическая связь в металлах, получившая название металлической, должна быть описана особой моделью. Поскольку в узлах кристаллической решетки металлов находятся атомы, логично предположить, что модель металлической связи может быть построена на основе представлений ковалентной связи.
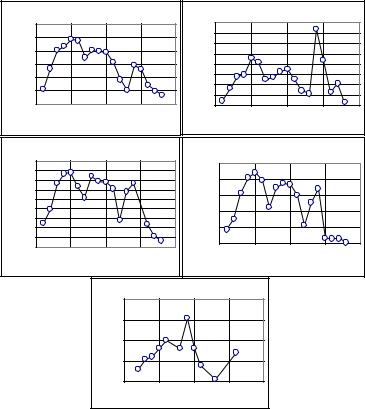
В табл. 4.4 и на рис. 4.9 приведены данные по изменению некоторых физико-химических характеристик простых веществ четвертого периода таблицы Д.И. Менделеева (первого, который содержит d-элементы) в зависимости от числа внешних электронов. Все они связаны с энергией взаимодействия между атомами в конденсированной фазе и в периоде закономерно изменяются. Характер изменения характеристик от числа электронов на внешнем уровне позволяет выделить отдельные области: возрастание (примерно 1…6), относительное постоянство (6…10), уменьшение значений (10…13), скачкообразное увеличение (14) и монотонное уменьшение (14…18).
|
|
|
|
|
|
|
Т а б л и ц а 4.4 |
|
|
|
|
|
|
|
|
|
|
nэ |
Электронная |
Тип |
tпл, |
∆Нпл, |
НВ, |
tкип, |
∆Нкип, |
|
|
конфигурация |
решетки |
оС |
кДж/моль |
МПа |
оС |
кДж/моль |
|
|
элемента |
|
|
|
|
|
|
|
1 |
K |
s1 |
ОЦК |
63,55 |
2,3 |
- |
760 |
89,4 |
2 |
Ca |
s2 |
ГЦК |
842 |
8,4 |
300 |
1485 |
152 |
3 |
Sc |
s2d1 |
Гекс. |
1541 |
14,1 |
550 |
2850 |
315 |
4 |
Ti |
s2d2 |
ГПУ |
1668 |
15 |
600 |
3330 |
410 |
5 |
V |
s2d3 |
ОЦК |
1920 |
23,0 |
800 |
3400 |
443 |
6 |
Cr |
s1d5 |
ОЦК |
1890 |
21,0 |
1000 |
2680 |
398 |
7 |
Mn |
s2d5 |
ОЦК |
1245 |
12,6 |
- |
2070 |
227 |
8 |
Fe |
s2d6 |
ОЦК |
1539 |
13,77 |
800 |
3200 |
350 |
9 |
Co |
s2d7 |
Гекс. |
1494 |
16,3 |
1550 |
2960 |
376 |
10 |
Ni |
s2d8 |
ГЦК |
1455 |
17,5 |
800 |
2900 |
370 |
11 |
Cu |
s1d10 |
ГЦК |
1084 |
12,97 |
400 |
2540 |
302 |
12 |
Zn |
s2d10 |
ГПУ |
419,5 |
7,24 |
- |
906 |
115 |
13 |
Ga |
s2d10p1 |
Ромб. |
29,75 |
5,59 |
60 |
2403 |
256 |
14 |
Ge |
s2d10p2 |
ПК |
958,5 |
37 |
- |
2850 |
343 |
15 |
As |
s2d10p3 |
Гекс. |
817 |
21,8 |
- |
Cубл. |
33 |
16 |
Se |
s2d10p4 |
Гекс. |
221 |
6,7 |
710 |
685,3 |
30 |
17 |
Br |
s2d10p5 |
- |
–7,25 |
10,6 |
- |
59,8 |
29,6 |
18 |
Kr |
s2d10p6 |
- |
–157 |
1,64 |
- |
–153 |
9,0 |
110
|
|
Температураплавления |
|
40 |
Энтальпия плавления |
|
|
|||
|
2500 |
|
|
|
|
|
|
|
|
|
|
2000 |
|
|
|
|
35 |
|
|
|
|
|
|
|
|
/моль |
30 |
|
|
|
|
|
|
1500 |
|
|
|
|
|
|
|
||
, С |
|
|
|
25 |
|
|
|
|
||
1000 |
|
|
|
20 |
|
|
|
|
||
tпл |
|
|
|
,кДж |
|
|
|
|
||
500 |
|
|
|
15 |
|
|
|
|
||
|
|
|
|
Н |
10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
-500 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
0 |
5 |
10 |
15 |
20 |
0 |
5 |
10 |
15 |
20 |
|
|
|
Число электронов |
|
|
|
|
Число электронов |
|
|
|
|
Температуракипения |
|
|
|
|
Энтальпия кипения |
|
|
||
|
4000 |
|
|
|
|
|
500 |
|
|
|
|
|
3500 |
|
|
|
|
|
400 |
|
|
|
|
|
3000 |
|
|
|
|
кДж, /моль |
|
|
|
|
|
tкип, С |
2500 |
|
|
|
|
300 |
|
|
|
|
|
2000 |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|||
1500 |
|
|
|
|
200 |
|
|
|
|
||
1000 |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
Н |
100 |
|
|
|
|
|
|
500 |
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
0 |
|
|
|
|
|
-500 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
5 |
10 |
15 |
20 |
|
|
0 |
5 |
10 |
15 |
20 |
|
|||||
|
|
|
|
|
|
|
|||||
|
|
|
Число электронов |
|
|
|
|
|
Число электронов |
|
|
|
|
Твердость по Бринелю |
|
|
|
|
2000 |
|
|
|
|
,МПа |
1500 |
|
|
|
|
1000 |
|
|
|
|
|
НВ |
|
|
|
|
|
|
500 |
|
|
|
|
|
0 |
|
|
|
|
|
0 |
5 |
10 |
15 |
20 |
|
|
|
Число электронов |
|
|
Рис. 4.9. Зависимость температуры плавления (tпл) и кипения (tкип), энтальпии плавления (∆Нпл) и кипения (∆Нкип), твердости по Бринелю простых веществ 4-го периода от числа электронов на внешнем энергетическом уровне (число электронов сверх полностью заполненной оболочки благородного газа Ar)
Подход к описанию металлической связи можно проиллюстрировать на примере кристалла калия. Атом калия на внешнем энергетическом уровне имеет один электрон. В изолированном атоме калия этот электрон находится на 4s-орбитали. В то же время имеются не сильно отличающиеся по энергии от 4s-орбитали свободные, не занятые электронами орбитали, относящиеся к 3d, 4p-подуровням. Можно предположить, что при образовании химической связи валентный электрон каждого атома может располагаться не только на 4s-орбитали, но и на одной из свободных орби-
111
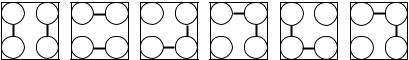
талей. Один валентный электрон атома, согласно методу валентных связей, позволяет ему реализовать одну единичную связь с ближайшим соседом. Наличие в электронной структуре атома мало различающихся по энергии свободных орбиталей позволяет предположить, что атом может «захватить» электрон от своего соседа на одну из свободных орбиталей и тогда у него появится возможность образовать две единичные связи с ближайшими соседями. В силу равенства расстояний до ближайших соседей и неразличимости атомов возможны различные варианты реализации химических связей между соседними атомами. Возможные варианты фрагмента кристаллической решетки из четырех соседних атомов показаны на рис. 4.10.
1) |
|
2) |
|
3) |
|
4) |
|
5) |
|
6) |
|
К |
К |
К |
К |
К+ |
К |
К |
К– |
К |
К+ |
К |
К– |
К |
К |
К |
К |
К |
К– |
К+ |
К |
К– |
К |
К+ |
К |
Рис. 4.10. Фрагмент кристаллической решетки калия и возможные варианты образования единичных химических (общих электронных пар) между соседними атомами
Полинг и Слэтер показали, что если имеется возможность одновременного существования нескольких электронных структур, способных свободно переходить друг в друга, то это приводит к понижению энергии системы. Эти структуры были названы резонансными. Каждая из них, взятая в отдельности, не отражает химическую связь. Описание связи в кристалле можно получить суперпозицией резонансов. То есть в металлическом кристалле положение связей между атомами соответствует не какой-то конкретной структуре, а всем сразу. Таким образом, положение химических связей в пространстве делокализовано. Возможность реализации резонансных структур обусловлена наличием у атома металла свободных орбиталей, незначительно отличающихся по энергии от валентных, которые были названы металлическими. Прочность металлической химической связи определяется как числом валентных электронов, так и числом металлических орбиталей. С учетом того, что в атомах металлов может происходить гибридизация s-, p- и d-электронных орбиталей, максимальное число валентных орбиталей равно шести.
112
