
- •ВВЕДЕНИЕ
- •1. ОСНОВНЫЕ ПОНЯТИЯ ХИМИИ
- •1.1. Химическая реакция
- •1.2. Классификация веществ
- •1.3. Количественные расчеты в химии
- •2. СТРОЕНИЕ АТОМА
- •2.1. Развитие представлений о строении атома
- •2.1.1. Теория строения атома Бора
- •2.1.2. Особенности описания микрочастиц
- •2.2. Основные понятия волновой механики
- •2.2.1. Волновое уравнение
- •2.2.2. Решение уравнения Шрёдингера для простейших случаев
- •2.3.1. Основное состояние атома водорода
- •2.3.2. Радиальное распределение электронной плотности. Электронная орбиталь
- •2.3.3. Возбужденные состояния атома водорода
- •2.3.4. Многоэлектронные атомы
- •2.4. Периодический закон и таблица элементов
- •2.4.1. Электронные конфигурации многоэлектронных атомов
- •2.4.2. Связь периодического закона со строением атома
- •2.4.3. Физико-химические характеристики атома
- •Контрольные вопросы
- •3. ХИМИЧЕСКАЯ СВЯЗЬ
- •3.1. Основные характеристики и классификация моделей химической связи
- •3.1.1. Основные параметры химической связи
- •3.1.2. Типы химической связи
- •3.2. Ковалентная химическая связь
- •3.2.1. Метод валентных связей
- •3.2.3. Геометрия простейших молекул. Гибридизация АО
- •3.2.4. Донорно-акцепторный механизм образования ковалентной связи
- •3.2.5. Метод молекулярных орбиталей
- •3.2.6. Полярность связи и дипольный момент молекулы
- •Контрольные вопросы
- •4. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ВЕЩЕСТВАХ
- •4.1. Межмолекулярные взаимодействия
- •4.1.2. Водородная связь
- •4.2. Химическая связь в твердом теле
- •4.2.1. Основные понятия о строении кристаллов
- •4.2.3. Ковалентные (атомные) кристаллы
- •4.2.4. Ионные кристаллы. Ионный тип химической связи
- •4.2.5. Химическая связь в металлах
- •4.2.6. Зонная модель кристаллического тела
- •4.2.7. Металлы, полупроводники и диэлектрики
- •4.2.8. Кристаллические материалы
- •4.2.9. Аморфные твердые тела
- •4.3. Химическая связь в жидкостях
- •Контрольные вопросы
- •5. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
- •5.1. Основные понятия и определения
- •5.1.1. Термодинамическая система
- •5.1.2. Термодинамический процесс
- •5.2. Тепловые эффекты физико-химических процессов
- •5.2.1. Внутренняя энергия
- •5.2.2. Первое начало термодинамики
- •5.2.3. Тепловой эффект химической реакции
- •5.2.4. Термохимические расчеты
- •5.3. Направление и пределы протекания химического процесса
- •5.3.1. Второе начало термодинамики
- •5.3.2. Энтропия
- •5.3.3. Направление химического процесса
- •5.3.4. Химический потенциал
- •Контрольные вопросы
- •6. КИНЕТИКА ХИМИЧЕСКИХ РЕАКЦИЙ
- •6.1. Механизм химической реакции
- •6.1.1. Частицы, участвующие в химической реакции
- •6.1.2. Классификация химических реакций
- •6.2. Элементарная химическая реакция
- •6.2.1. Скорость химической реакции
- •6.2.2. Зависимость скорости химической реакции от концентрации реагирующих веществ
- •6.2.3. Константа скорости химической реакции
- •6.3. Формальная кинетика гомогенных реакций
- •6.3.1. Кинетические уравнения реакций
- •6.3.2. Зависимость скорости реакции от температуры
- •6.3.3. Определение кинетических параметров реакции
- •6.4. Цепной механизм химической реакции
- •6.5. Индуцированные реакции
- •6.5.1. Фотохимические реакции
- •6.5.2. Радиационно–химические процессы
- •6.6. Макрокинетика
- •6.6.1. Гетерогенные реакции
- •6.6.2. Горение и взрыв
- •6.7. Катализ
- •6.7.1. Гомогенный катализ
- •6.7.2. Гетерогенный катализ
- •Контрольные вопросы
- •7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- •7.1. Термодинамическое условие химического равновесия
- •7.2. Кинетическое условие химического равновесия
- •7.3. Расчет равновесного состава газовой смеси
- •7.4. Равновесия в растворах
- •7.4.1. Растворы
- •7.4.2. Электролитическая диссоциация
- •7.4.3. Ионное произведение воды. Водородный показатель
- •7.4.4. Растворы кислот и оснований
- •7.4.5. Буферные растворы
- •7.4.6. Гидролиз солей
- •7.4.7. Обменные реакции с образованием осадка
- •7.5. Фазовые равновесия
- •7.5.1. Диаграмма состояния однокомпонентной системы
- •7.5.2. Диаграмма состояния двухкомпонентной системы
- •7.5.3. Кипение и кристаллизация растворов
- •7.5.4. Электролиты
- •Контрольные вопросы
- •8. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- •8.1. Основные понятия и определения
- •8.2. Электродные процессы
- •8.2.1. Скачок потенциала на границе «металл–электролит»
- •8.2.2. Уравнение Нернста
- •8.2.3. Электроды
- •8.3. Неравновесные электрохимические системы
- •8.3.1. Гальванический элемент
- •8.3.2. Окислительно-восстановительные реакции в водных растворах
- •8.3.3. Электролиз
- •8.4. Кинетика электрохимических процессов
- •8.4.1. Скорость электрохимических процессов
- •8.4.2. Поляризация электродов
- •8.5. Практическое использование электрохимических процессов
- •8.5.1. Химические источники тока
- •8.5.2. Применение электролиза
- •Контрольные вопросы
- •9. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- •9.1. Коррозионные процессы
- •9.2. Химическая коррозия
- •9.2.1. Высокотемпературная газовая коррозия
- •9.2.2. Кинетика роста оксидных пленок
- •9.2.3. Факторы, влияющие на скорость газовой коррозии
- •9.3. Электрохимическая коррозия
- •9.3.1. Анодные и катодные реакции
- •9.3.2. Термодинамические условия электрохимической коррозии металлов
- •9.3.3. Факторы, влияющие на скорость электрохимической коррозии
- •9.4. Коррозионные среды и влияние дополнительных факторов
- •9.4.1. Коррозионно-механическое разрушение металлов
- •9.4.2. Водородная коррозия
- •9.4.3. Радиационная коррозия
- •Контрольные вопросы
- •Библиографический список
лярного взаимодействия (сил Ван-дер-Ваальса) и водородных связей. Расположение частиц подчиняется законам плотнейшей упаковки с учетом геометрии и возможного расположения самих молекул. Межмолекулярное расстояние существенно больше, чем внутримолекулярное (длина связи в молекулах меньше, чем расстояние между молекулами). В ряде случаев из молекулярных кристаллов в отдельную группу выделяют кристаллы с преимущественно водородной связью между молекулами. Отличительной особенностью строения этих кристаллов (например, кристаллов льда) является расположение молекул в пространстве и число ближайших соседей, обусловленное водородными связями между молекулами.
П р и м е р. В кристаллах йода длина ковалентной связи в мо-
|
о |
|
|
лекуле I2 rI−I =2,67А, |
а расстояние между молекулами I2-I2 |
||
о |
|
o |
|
rI2 −I2 =3,60Аи |
rI2 −I2 =4,40A |
в зависимости от направления в кри- |
|
сталлической решетке.
Подобным образом кристаллизуются многие органические вещества, H2O, CO2, N2, Xe, Kr, H2 и т.д. Кристаллы обладают сравнительно низкой температурой плавления, низкой твердостью, неэлектропроводны.
4.2.3. Ковалентные (атомные) кристаллы
Ковалентные кристаллы образуют атомы с равной или близкой электроотрицательностью. Связь между атомами в решетке осуществляется за счет ковалентной связи, поэтому число ближайших соседей в решетке определяется валентностью атома (числом общих электронных пар с соседними атомами). Взаимное расположение ближайших соседних атомов определяется направленностью в пространстве валентных орбиталей. В случае ковалентных кристаллов координационное число равно числу ковалентных связей атома в узле кристаллической решетки.
П р и м е р. Как известно, углерод имеет несколько полиморфных (аллотропических) модификаций: алмаз, графит, карбин. Атомы углерода имеют четыре валентных электрона (C-2s22p2).
В случае sp3-гибридизации четыре гибридные орбитали образуют тетраэдрическую структуру, пространственное повторение
104

которой дает решетку алмаза. Каждый атом углерода связан с че-
о
тырьмя соседними атомами равноценными связями (rсв =1,54А ),
угол между которыми составляет примерно 109o. Алмазоподобную решетку имеют также и изоэлектронные углероду атомы кремния (Si-3s23p2), германия (Ge-4s24p2) и изоэлектронные молекулы (суммарное число валентных электронов такое же, как и у двух атомов углерода). Например, нитрид бора [B-2s22p1; N-2s22p3], арсенид галлия [Ga-4s24p1; As 4s24p3], карбид кремния [C-2s22p2; Si-3s23p2]. Отметим, что в нитриде бора и арсениде галлия четвертая ковалентная связь образуется по донорно-акцепторному механизму.
Вгибридизации могут участвовать не все валентные электроны.
Вслучае sp2-гибридизации три гибридные орбитали образуют плоский правильный треугольник, перпендикулярно которому располагается четвертая р-орбиталь. Каждый атом углерода связан с
тремя соседями равноценными σ-связями, образованными sp2- гибридными электронами. В результате в плоскости образуется
о
гексагональная сетка (rсв =1,4А ) связанных между собой атомов углерода (рис. 4.7, а).
а) |
|
в) |
||
|
|
|
|
|
|
|
|
|
|
б) |
г) |
3,4 Å
1,4 Å
Рис. 4.7. Кристаллы углерода с sp-гибридизацией: а – плоская сетка из атомов углерода; б – графит; в – нанотрубка; г – фуллерен
105
Отдельные плоскости сетки могут связываться между собой
о
более слабой связью (rсв =3,4А) за счет негибридизованных p-
электронов, образуя кристаллическую структуру графита (рис. 4.7, б). Таким образом, кристалл графита представляет собой набор параллельных, относительно слабо связанных между собой плоскостей.
Необходимо отметить, что отдельные плоскости сетки при определенных условиях могут существовать в виде наноструктур – графена, образовывать цилиндрические структуры – нанотрубки или сферы – фуллерены (рис. 4.7, в, г).
Случаю sp-гибридизации соответствует карбин. Структуру карбина образуют атомы углерода, соединенные в линейных цепочках двойными или чередующимися одинарными и тройными связями.
4.2.4. Ионные кристаллы. Ионный тип химической связи
Распространенным типом кристаллов являются кристаллы, образованные атомами с сильно различающимися значениями элек-
троотрицательностей (χВ>>χА). В первом приближении можно считать, что в этом случае пара валентных электронов полностью смещается к атому В, при этом образуются ионы противоположного знака: А+ – катион и В- – анион. Данное допущение считается справедливым, если перенос заряда составляет величину более 2/3 от максимально возможной, что соответствует разности в значениях электроотрицательностей по Полингу более чем 2,1
( χB −χA >2,1).
Минимум энергии системы соответствует чередованию катионов и анионов во всех направлениях в кристаллической решетке. В данном случае химическую связь относят к ионному типу, и ее описание сводится к определению энергии взаимодействия ионов, т.е. электрических зарядов. В первом приближении ионы можно представить недеформирующимися шарами. Поскольку электрическое поле сферически симметрично, энергия взаимодействия определяется только расстоянием между зарядами, а не их взаимным расположением. Минимум энергии достигается в случае наименьшего расстояния между зарядами, что выполняется при одном из вариантов плотнейшей упаковки ионов. Энергия электростатического взаимодействия одного моля ионов в кристалле (энергия
106
ионной связи) называется энергией кристаллической решетки.
Рассмотрим ее расчет.
Между катионом (A+) и анионом (B-) действуют силы электростатического притяжения и отталкивания. Энергия притяжения может быть описана законом взаимодействия точечных зарядов. Энергия отталкивания ближайших соседних ионов определяется взаимодействием системы точечных зарядов электронов и ядер и описывается более сложной зависимостью. Энергия взаимодействия пары ионов равна сумме энергий притяжения и отталкивания:
E =Eпр +Eот . Энергия притяжения противоположных по знаку зарядов в зависимости от расстояния между ними определяется за-
коном Кулона: Eпр =−ker2 , где r – расстояние между центрами ио-
нов, e – заряд электрона, k – константа в законе Кулона. Энергию отталкивания Макс Борн предложил определять по форму-
леEот = rBn , где B − постоянная величина, n – коэффициент бор-
новского отталкивания.
Таким образом, энергия двух взаимодействующих ионов в зависимости от расстояния между их центрами будет равна:
E(r) = − ker2 + rBn .
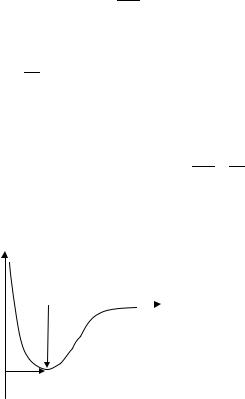
Энергия химической связи пары ионов (Eсв) соответствует минимуму энергии системы, который достигается на расстоянии между ионами, равном длине связи (r = rсв) (рис. 4.8).
E(r)
0 |
|
r |
Рис. 4.8. Энергия взаимодействия |
|
пары ионов в зависимости |
||
|
|
|
|
|
Eсв |
|
от расстояния между ними |
|
|
|
rсв
Постоянную B можно определить из условия равенства нулю первой производной функции в точке минимума:
107
dE(r) |
|
|
|
ke2 |
|
nB |
|
ke2r |
n−1 |
|
|
|
|
|
|
||||||
|
r=r |
|
= |
|
− |
|
=0 , → B = |
св |
. |
|
dr |
|
r2 |
rn+1 |
|
||||||
|
св |
|
|
|
n |
|
|
|||
|
|
|
|
|
|
|||||
Тогда энергия химической связи пары ионов будет равна:
E |
|
ke2 |
|
ke2rn−1 |
|
ke2 |
|
1 |
|||
=− |
|
+ |
|
|
=− |
|
1− |
|
. |
||
rсв |
r |
nn |
rсв |
n |
|||||||
св |
|
|
|
|
|
||||||
|
|
|
|
св |
|
|
|
|
|
|
|
Для определения энергии кристаллической решетки необходимо учесть, что один моль вещества содержит NА (число Авогадро) пар ионов. Кроме того, необходимо учесть энергию взаимодействия каждого иона как с ближайшими, так и с более удаленными ионами. Вклад этого взаимодействия зависит от типа кристаллической решетки и учитывается с помощью множителя А, который называется постоянной Маделунга. Таким образом, энергия кристаллической решетки, образованной однозарядными ионами, определяется уравнением (уравнение Борна)
E |
|
=− |
AN |
a |
ke2 |
|
1 |
, |
св |
|
|
1− |
|
||||
|
|
rсв |
|
n |
|
|||
|
|
|
|
|||||
где А – постоянная Маделунга, для кристаллической решетки типа
NaCl (ГЦК) A=1,7475, типа CsCl (ПК) A=1,763; n – коэффициент борновского отталкивания − определяется из сжимаемости кристалла – относительного уменьшения его объема при увеличении давления. Для галогенидов щелочных металлов n = 6÷12.
Реальные ионы в узлах кристаллической решетки не являются недеформирующимися шарами. Для более точного расчета величины энергии кристаллической решетки необходимо учитывать эффекты, связанные с деформацией ионов, которая приводит к разделению центров положительных и отрицательных зарядов, т.е. при рассмотрении взаимодействия точечных зарядов необходимо учесть взаимодействие диполей. Вклад этих эффектов невелик и составляет единицы процентов.
Электростатическая модель для кристаллов галогенидов щелочных металлов (ЩГК) дает хорошее совпадение величин энергии кристаллической решетки, рассчитанной по уравнению Борна и измеренной экспериментально (табл. 4.3).
Энергия ионной решетки существенно больше, чем энергия межмолекулярного взаимодействия в молекулярных кристаллах, и сравнима с энергией ковалентных связей в атомном кристалле. Поэтому, как правило, разрушение ионного кристалла происходит
108
