
- •Міністерство охорони здоров`я україни національний фармацевтичний університет
- •Дипломна робота
- •1.1Ботанічна характеристика деяких представників роду Echinacea Moench
- •2.4.14. Визначення кількісного вмісту діючих речовин в коренях ехінацеї пурпурової………………………………………………..
- •2.4.14.1.Кількісне визначення загального вмісту
- •Розділ 1. Огляд літератури. Рід ехінацея – джерело отримання біологічно активних речовин
- •1.2. Географічне поширення та культивування
- •1.3. Хімічний склад деяких видів ехінацеї
- •1.3.1. Вуглеводи
- •1.3.2. Фенольні сполуки
- •1.3.3. Нітрогеновмісні сполуки
- •1.3.4. Ефірна олія
- •1.3.5. Інші сполуки
- •1.4. Застосування в медичній практиці та інших галузях народного господарства
- •1.5. Номенклатура лікарських препаратів з ехінацеї на фармацевтичному ринку України
- •2.1. Ідентифікація за зовнішніми ознаками
- •2.2.2. Мікроскопія сировини, що досліджувалась
- •2.3. Якісні реакції
- •2.3.1. Визначення вуглеводів
- •2.3.1.2. Виявлення полісахаридів
- •2.3.1.3. Виявлення пектинових речовин
- •2.3.2. Виявлення вільних амінокислот
- •2.3.3. Виявлення фенольних сполук
- •2.3.3.1. Виявлення дубильних речовин
- •2.3.3.2. Виявлення гідроксикоричних кислот
- •2.3.3.3. Виявлення флавоноїдів
- •2.3.3.4. Виявлення кумаринів
- •2.3.4. Виявлення сапонінів
- •2.4. Числові показники
- •2.4.6. Сторонні домішки
- •2.4.7. Визначення питомої маси
- •2.4.8. Визначення об’ємної маси
- •2.4.9. Визначення насипної маси
- •2.4.10. Визначення пористості сировини
- •2.4.14. Визначення кількісного вмісту діючих речовин в коренях ехінацеї пурпурової
- •2.4.14.1.Кількісне визначення загального вмісту полісахаридів
- •Кількісний вміст полісахаридів в коренях ехінацеї пурпурової
- •2.4.14.2. Фракціонування полісахаридів
- •Результати визначення кількісного вмісту полісахаридних фракцій в коренях ехінацеї пурпурової
- •2.4.14.3. Визначення фенольних сполук
- •2.4.14.3.1. Кількісне визначення вмісту гідроксикоричних кислот
- •Кількісний вміст суми гідроксикоричних кислот в коренях ехінацеї пурпурової
- •2.4.14.3.2. Кількісне визначення гідроксикоричних кислот за методикою дфу
- •Кількісний вміст суми гідроксикоричних кислот в коренях ехінацеї пурпурової
- •2.4.14.3.3. Кількісне визначення вмісту флавоноїдів
- •Результати кількісного визначення вмісту флавоноїдів в коренях ехінацеї пурпурової
- •2.4.14.3.4. Визначення кількісного вмісту окиснюваних поліфенолів
- •Результати визначення кількісного вмісту суми окиснюваних поліфенолів в коренях ехінацеї пурпурової
- •2.4.14.4. Кількісне визначення вмісту аскорбінової кислоти
- •Результати кількісного визначення вмісту аскорбінової кислоти в коренях ехінацеї пурпурової та в густому екстракті
- •2.4.14.5. Визначення кількісного вмісту ефірної олії
- •2.5. Зберігання сировини
- •Параметри стандартизації коренів ехінацеї пурпурової
- •3.1. Отримання густого екстракту коренів ехінацеї пурпурової
- •3.3. Визначення параметрів стандартизації густого екстракту з коренів ехінацеї пурпурової
- •3.3.2.3. Виявлення полісахаридів
- •3.3.3. Важкі метали і вміст органічних розчинників
- •3.3.4. Втрата у масі при висушуванні
- •3.3.5. Визначення сухого залишку
- •3.3.6. Кількісне визначення
- •3.3.6. 1. Кількісне визначення полісахаридів
- •3.3.6.2. Визначення кількісного вмісту гідроксикоричних кислот
- •3.3.6.3. Кількісне визначення суми окиснюваних фенолів
- •3.3.7. Зберігання
- •3.3.8. Маркування
- •Параметри стандартизації густого екстракту коренів ехінацеї пурпурової
- •Загальний висновок
- •Список використаних джерел
- •Відгук на дипломну роботу студентки 4 курсу ссо1 групи Азаренко в. І. . На тему «Стандартизація густого екстракту ехінацеї пурпурової»
- •Рецензія на дипломну роботу студентки 4 курсу ссо1 групи Азаренко в. І. На тему «Стандартизація густого екстракту ехінацеї пурпурової»
3.3.2.3. Виявлення полісахаридів
Якісне визначення. У хімічний стаканчик вміщували 15 мл 96 % етанолу і поступово додавали 5 мл густого екстракту коренів ехінацеї пурпурової.
Спостереження: утворювався білий аморфний осад.
Хроматографічне вивчення. Для вивчення мономерного складу полісахаридів, 0,1 г їх розчиняли в мінімальній кількості води (1,5-2 мл) і гідролізували таким же об’ємом 20 % кислоти сульфатної при нагріванні на водяному огрівнику, контролюючи хід гідролізу методом хроматографії. Повний гідроліз проходив за 5 годин. Гідролізати нейтралізували барія карбонатом до нейтральної реакції за універсальним індикатором. Розчин фільтрували, промивали фільтр і осад на фільтрі водою. Фільтрат випарювали під вакуумом до сухого залишку, який розчиняли в 0,5 мл етанолу.
Отриманий розчин наносили на хроматографічний папір «Filtrak F» № 7. Хроматографували в системі розчинників: ацетон–бутанол–вода (7:4:2) нисхідним способом в присутності вірогідних зразків моносахаридів. Для ідентифікації вільних цукрів паралельно досліджували фугат, отриманий в ході висадження полісахаридів [34].
Хроматограму після закінчення хроматографування висушували на повітрі, обробляли анілін-фталатним реактивом і нагрівали в сушильній шафі протягом 10 хвилин при 100°С. Цукри проявлялися у вигляді коричневих (гексози) і рожевих плям (пентози)
Схема хроматограми представлена на рис. 3.2.
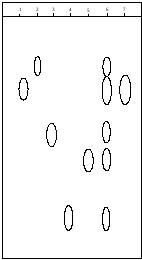
Рис. 3.2. Схема хроматограми вільних і зв’язаних цукрів в густому екстракті коренів ехінацеї пурпурової.
1 – глюкоза; 2 – галактоза; 3 – арабіноза; 4 – рамноза, 5 – ксилоза, 6 - гідролізат полісахаридів густого екстракту листя берези,
7 - густий екстракт коренів ехінацеї пурпурової.
Система розчинників: ацетон–бутанол–вода (7:4:2).
Спосіб хроматографування: нисхідний.
Реактив для проявлення: анілін-фталат.
В результаті вивчення, як видно з рис. 3.2 у вільному стані виявлено глюкозу, а в гідролізаті – глюкозу, галактозу, арабінозу, ксилозу і рамнозу.
3.3.3. Важкі метали і вміст органічних розчинників
(Метод А). До 1 г густого екстракту додають 1 мл кислоти сульфатної Р, обережно спалюють і прожарюють. До одержаного залишку додають при нагріванні 5 мл розчину 615 г/л амонію ацетату Р, фільтрують крізь беззольний фільтр, промивають 5 мл води Р і доводять об`єм фільтрату водою Р до 100 мл. 12 мл одержаного розчину мають витримувати випробування на важкі метали. Еталон готують з використанням еталонного розчину плюмбуму (1 ppm Pb) Р.
Вміст важких металів густого екстракту не більше 0,01 % (100 ppm).
Вміст важких металів склав 0,0057%.
Контроль наявності залишкових кількостей органічних розчинників може проводитися будь-якими валідованими методами. Найприйнятнішим є метод газової хроматографії. Відсутність в АНД такого розділу або відсутність у розділі методики визначення будь-якого з органічних розчинників, що використовувалися при виробництві лікарського засобу, має бути обґрунтована в кожному окремому випадку.
Граничний вміст залишкових кількостей органічних розчинників у субстанція і готових лікарських засобах – етанол 1,0 %.
75 мл густого екстракту вміщували у круглодонну колбу місткістю 250 мл і відганяли рідину на роторному вакуум-випарювачі у приймач (мірну колбу місткістю 50 мл). Приймач вміщували в ємкість з холодною водою, збирали близько 48 мл відгону, доводили його температуру до 200С і додавали води до позначки.
Густину відгону визначали пікнометром і по алкоголеметричним таблицям знаходили відповідний вміст спирту у відсотках за об’ємом..
Вміст спирту в сумарному екстракті (Х) у відсотках за об’ємом обчислювали за формулою:
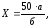
де 50 – об’єм відгону, мл;
а – вміст спирту в відсотках за об’ємом;
б – об’єм густого екстракту, який було взято для відгону; мл.
Вміст етанолу у густому екстракті, що досліджувався, склав 0,39%.
Вміст залишкової кількості етанолу в густому екстракті не більше 1,0 %.
