
- •Міністерство охорони здоров`я україни національний фармацевтичний університет
- •Дипломна робота
- •1.1Ботанічна характеристика деяких представників роду Echinacea Moench
- •2.4.14. Визначення кількісного вмісту діючих речовин в коренях ехінацеї пурпурової………………………………………………..
- •2.4.14.1.Кількісне визначення загального вмісту
- •Розділ 1. Огляд літератури. Рід ехінацея – джерело отримання біологічно активних речовин
- •1.2. Географічне поширення та культивування
- •1.3. Хімічний склад деяких видів ехінацеї
- •1.3.1. Вуглеводи
- •1.3.2. Фенольні сполуки
- •1.3.3. Нітрогеновмісні сполуки
- •1.3.4. Ефірна олія
- •1.3.5. Інші сполуки
- •1.4. Застосування в медичній практиці та інших галузях народного господарства
- •1.5. Номенклатура лікарських препаратів з ехінацеї на фармацевтичному ринку України
- •2.1. Ідентифікація за зовнішніми ознаками
- •2.2.2. Мікроскопія сировини, що досліджувалась
- •2.3. Якісні реакції
- •2.3.1. Визначення вуглеводів
- •2.3.1.2. Виявлення полісахаридів
- •2.3.1.3. Виявлення пектинових речовин
- •2.3.2. Виявлення вільних амінокислот
- •2.3.3. Виявлення фенольних сполук
- •2.3.3.1. Виявлення дубильних речовин
- •2.3.3.2. Виявлення гідроксикоричних кислот
- •2.3.3.3. Виявлення флавоноїдів
- •2.3.3.4. Виявлення кумаринів
- •2.3.4. Виявлення сапонінів
- •2.4. Числові показники
- •2.4.6. Сторонні домішки
- •2.4.7. Визначення питомої маси
- •2.4.8. Визначення об’ємної маси
- •2.4.9. Визначення насипної маси
- •2.4.10. Визначення пористості сировини
- •2.4.14. Визначення кількісного вмісту діючих речовин в коренях ехінацеї пурпурової
- •2.4.14.1.Кількісне визначення загального вмісту полісахаридів
- •Кількісний вміст полісахаридів в коренях ехінацеї пурпурової
- •2.4.14.2. Фракціонування полісахаридів
- •Результати визначення кількісного вмісту полісахаридних фракцій в коренях ехінацеї пурпурової
- •2.4.14.3. Визначення фенольних сполук
- •2.4.14.3.1. Кількісне визначення вмісту гідроксикоричних кислот
- •Кількісний вміст суми гідроксикоричних кислот в коренях ехінацеї пурпурової
- •2.4.14.3.2. Кількісне визначення гідроксикоричних кислот за методикою дфу
- •Кількісний вміст суми гідроксикоричних кислот в коренях ехінацеї пурпурової
- •2.4.14.3.3. Кількісне визначення вмісту флавоноїдів
- •Результати кількісного визначення вмісту флавоноїдів в коренях ехінацеї пурпурової
- •2.4.14.3.4. Визначення кількісного вмісту окиснюваних поліфенолів
- •Результати визначення кількісного вмісту суми окиснюваних поліфенолів в коренях ехінацеї пурпурової
- •2.4.14.4. Кількісне визначення вмісту аскорбінової кислоти
- •Результати кількісного визначення вмісту аскорбінової кислоти в коренях ехінацеї пурпурової та в густому екстракті
- •2.4.14.5. Визначення кількісного вмісту ефірної олії
- •2.5. Зберігання сировини
- •Параметри стандартизації коренів ехінацеї пурпурової
- •3.1. Отримання густого екстракту коренів ехінацеї пурпурової
- •3.3. Визначення параметрів стандартизації густого екстракту з коренів ехінацеї пурпурової
- •3.3.2.3. Виявлення полісахаридів
- •3.3.3. Важкі метали і вміст органічних розчинників
- •3.3.4. Втрата у масі при висушуванні
- •3.3.5. Визначення сухого залишку
- •3.3.6. Кількісне визначення
- •3.3.6. 1. Кількісне визначення полісахаридів
- •3.3.6.2. Визначення кількісного вмісту гідроксикоричних кислот
- •3.3.6.3. Кількісне визначення суми окиснюваних фенолів
- •3.3.7. Зберігання
- •3.3.8. Маркування
- •Параметри стандартизації густого екстракту коренів ехінацеї пурпурової
- •Загальний висновок
- •Список використаних джерел
- •Відгук на дипломну роботу студентки 4 курсу ссо1 групи Азаренко в. І. . На тему «Стандартизація густого екстракту ехінацеї пурпурової»
- •Рецензія на дипломну роботу студентки 4 курсу ссо1 групи Азаренко в. І. На тему «Стандартизація густого екстракту ехінацеї пурпурової»
2.3.1.3. Виявлення пектинових речовин
Реакція з карбазолом. До 1 мл отриманого розчину додавали по 0,25 мл 0,5% розчину карбазолу і 5 мл кислоти сульфатної концентрованої, перемішували і нагрівали на киплячому водяному огрівнику протягом 10 хв [28]. З’являлося червоно-фіолетове забарвлення, яке свідчило про наявність кислоти галактуронової в досліджуваному зразку.
2.3.2. Виявлення вільних амінокислот
Виявлення амінокислот проводили методом ПХ. Метод багаторазового розвинення хроматограми дозволяє фронту розчинника пройти більшу відстань при тій же самій довжині листа паперу, тем самим покращити розділення досліджуваних речовин. Хроматограму з нанесеними зразками вміщували в камеру з розчинниками. Після проходження розчинником однієї третини довжини листа паперу хроматограму виймали і ретельно висушували. Другий раз поступали аналогічно з тією різницею, що розчинник проходив одну другу довжини листа паперу і третій раз розчинник проходив весь лист до лінії фронту.
Фільтрат водного екстракту коренів хроматографували в системі розчинників н-бутанол-кислота оцтова-вода (4:1:2), з трьома розбіжками в присутності достовірних зразків. Для проявлення амінокислот використовували 0,1 % розчин нінгідрину в етанолі, хроматограму нагрівали в сушильній шафі при 90 ○С до появи плям амінокислот. При цьому амінокислоти забарвлювались у фіолетовий, рожево-фіолетовий, або жовтий (пролін) колір. Амінокислоти ідентифікували порівнюючи їх значення Rf із значенням Rf достовірних зразків амінокислот при паралельному їх хроматографуванні.
Результати хроматографічного аналізу визначення амінокислот в досліджуваних видах сировини наведені на рис.2.6.
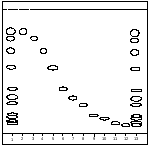
Рис. 2.6. Схема хроматограми виявлення вільних амінокислот в коренях ехінацеї пурпурової і густому екстракті.
1 – корені ехінацеї пурпурової; 2-12 – вірогідні зразки амінокислот: 2 – ізолейцин, 3 – лейцин, 4 – фенілаланін, 5 – валін, 6 – тирозин, 7 – пролін, 8 – аланін, 9 – гліцин, 10 – кислота аспарагінова, 11 – серин, 12 – метіонін; 13 –густий екстракт.
Система розчинників: н-бутанол-кислота оцтова-вода (4:1:2). Реактив для проявлення: 0,1 % розчин нінгідрину в етанолі.
Було ідентифіковано 11 амінокислот: ізолейцин (Rf=0,12), метіонін (Rf=0,14), серин (Rf=0,15), аспарагінова кислота (Rf=0,16), гліцин (Rf=0,17), аланін (Rf=0,25), пролін (Rf=0,31), тирозин (Rf=0,4), валін (Rf=0,59) та фенілаланін (Rf=0,71) [52, 83].
2.3.3. Виявлення фенольних сполук
2.3.3.1. Виявлення дубильних речовин
Виявлення дубильних речовин проводили у водному витягу, використовуючи наступні реакції.
Реакція з 1% розчином желатини. До водного витягу сировини, що вивчалася, по краплях додавали однакову кількість свіжоприготованого 0,5% розчину желатини і одну краплю 10% розчину кислоти хлоридної для підвищення чутливості реакції [48]. Утворювався осад.
Реакція з 1% розчином хініну гідрохлориду. До водного витягу сировини, що вивчалася, додавали по декілька крапель 1% розчину хініну гідро хлориду [48]. Утворювався білий аморфний осад.
Реакція з розчином залізоамонієвних галунів. До водного витягу сировини, що вивчалася, по краплях додавали розчин залізоамонієвних галунів [48]. З’являлося чорно-зелене забарвлення.
Проведені якісні реакції свідчать про наявність дубильних речовин конденсованої природи в коренях ехінацеї пурпурової.
