
- •Міністерство освіти і науки, молоді та спорту україни
- •1. За агрегатним станом компонентів горючої суміші в зоні горіння.
- •2. За способом утворення горючої суміші.
- •3. За механізмом поширення горіння.
- •4. За газодинамічним режимом горіння
- •Методика складання рівнянь реакції горіння.
- •2.1. Ланцюгові реакції
- •2.2. Зародження ланцюгів
- •2.3 Продовження ланцюгів
- •2.4 Хімічні процеси при горінні водню
- •3.1 Визначення матеріального балансу
- •3.2 Витрата повітря на горіння
- •3.5 Горіння індивідуальних речовин в конденсованому стані
- •3.7 Теплота згоряння. Види теплоти згоряння
- •1) Вид горючої речовини:
- •2) Склад горючої суміші:
- •3) Умови, в яких знаходиться горюча суміш:
- •4.1. Визначення полум'я та структура полум'я
- •4.2.Концентраційні межі поширення полум'я
- •4.2.1. Поняття концентраційних меж поширення полум'я
- •4.2.2. Метод визначення концентраційних меж поширення полум'я
- •4.2.3 Чинники, що впливають на концентраційні межі
- •4.2.4. Практичне значення концентраційних меж поширення полум'я
- •5.1 Види виникнення горіння
- •5.2 Теплова теорія само спалахування
- •5.3 Температура самоспалахування речовин
- •5.4 Фактори, що впливають на температуру самоспалахування
- •1) Вид горючої речовини,
- •2) Склад горючої суміші,
- •3) Умови, в яких знаходиться горюча суміш.
- •5.5 Визначення температури самоспалахування а її практичне значення
- •5.6 Класифікація процесів самозаймання. Відмінні особливості самозаймання
- •5.7 Умови, які необхідні для виникнення самозаймання.
- •5.8. Різні види самозаймання теплове самозаймання
- •Хімічне самозаймання
- •Самозаймання речовин при контакті з хімічними окислювачами.
- •Фізичне самозаймання
- •1.1. Механізм фізичного самозаймання вугілля
- •Мікробіологічне самозаймання
- •6.1 Поняття і особливості процесу запалювання
- •6.2 Ініціювання горіння в холодному газі нагрітими тілами
- •6.3 Чинники, що впливають на процес запалювання
- •6.4 Запалювання горючих систем електричними розрядами
- •Τ охол 3 τ хр
- •6.5 Підпалення фрикційними іскрами, краплями розплавленого металу
- •7.1 Загальні закономірності горіння газових сумішей
- •7.2 Закономірності поширення кінетичного горіння в газових сумішах
- •8.1 Загальні закономірності випаровування та горіння рідин
- •8.2 Температурні межі поширення полум'я
- •8.3 Класифікація твердих горючих матеріалів
- •8.4 Загальні закономірності горіння твердих речовин
- •Сргаз(Тзап - Tкип,(розкл))]
- •8.5 Особливості горіння металів
- •8.6 Загальна характеристика і властивості пилу
- •8.7 Запалювання дисперсних систем
- •8.8 Особливості горіння пилу в стані аерозоль та аерогель
- •9.2 Критичний час розвитку пожежі в огорожі.
- •9.6 Визначення висоти нейтральної зони. Методи регулювання газообміну на пожежі.
- •9.1 Динаміка розвитку пожежі в огорожі
- •9.2 Критичний час розвитку пожежі в огорожі
- •9.3 Основні положення інтегральної моделі температурного режиму
- •Фактори, що впливають на температуру пожежі в огородженні
- •9.5 Основні положення зонної моделі температурного режиму
- •Основні закономірності газообміну при пожежі в огородженні
- •9.6 Визначення висоти нейтральної зони. Методи регулювання газообміну на пожежі
- •10.1. Роль концентраційних меж поширеня полум'я у погасанні полум'я
- •10. 2 Погасання полум'я у вузьких каналах
- •11.5 Основи припинення горіння ізоляцією, інгібіруванням, розбавленням.
- •11. 1 Методи та способи припинення горіння
- •Припинення горіння
- •11.2 Запобігання виникнення горючого середовища
- •11.2 Запобігання виникнення горючого середовища та джерел запалювання в ньому
- •11.3 Поняття та загальні вимоги до вогнегасних речовин
- •1. Охолодження
- •2. Розбавлення
- •3. Ізоляція
- •4. Хімічне гальмування реакції горіння
- •11.4 Механізм припинення горіння охолодженням
- •Теоретична інтенсивність подачі води на гасіння пожежі
- •Qпогл q відв
- •Методи підвищення вогнегасної ефективності води на пожежі
- •11.5 Основи припинення горіння ізоляцією, інгібіруванням, розбавленням.
- •Механізм припинення горіння методом розбавлення
- •Список джерел
Теоретична інтенсивність подачі води на гасіння пожежі
Отже ми з’ясували яку кількість тепла потрібно відібрати від зони горіння, або від поверхневого шару горючої речовини для того, щоб припинити горіння. Тепло, яке потрібно відвести від зони горіння, може бути поглинене ВЗ для проходження ендотермічних процесів. Це тепло затрачується на нагрів і фазовий перехід вогнегасного засобу. Тому кількість поглиненої енергії складається з:
Qпогл = Qнагр 1 + Qф.п + Qнагр2, кДж/кг
Qнагр.1. – теплота нагріву ВЗ від початкової температури до температури фазового переходу
Qф.п. – теплота фазового переходу (сублімації або випаровування)
Qнагр.2. – теплота нагріву пари, що утворилася при фазовому переході ВЗ, від температури фазового переходу до температури зони горіння.
Так, питому кількість енергії, що поглинається 1 кг води, можна оцінити як:
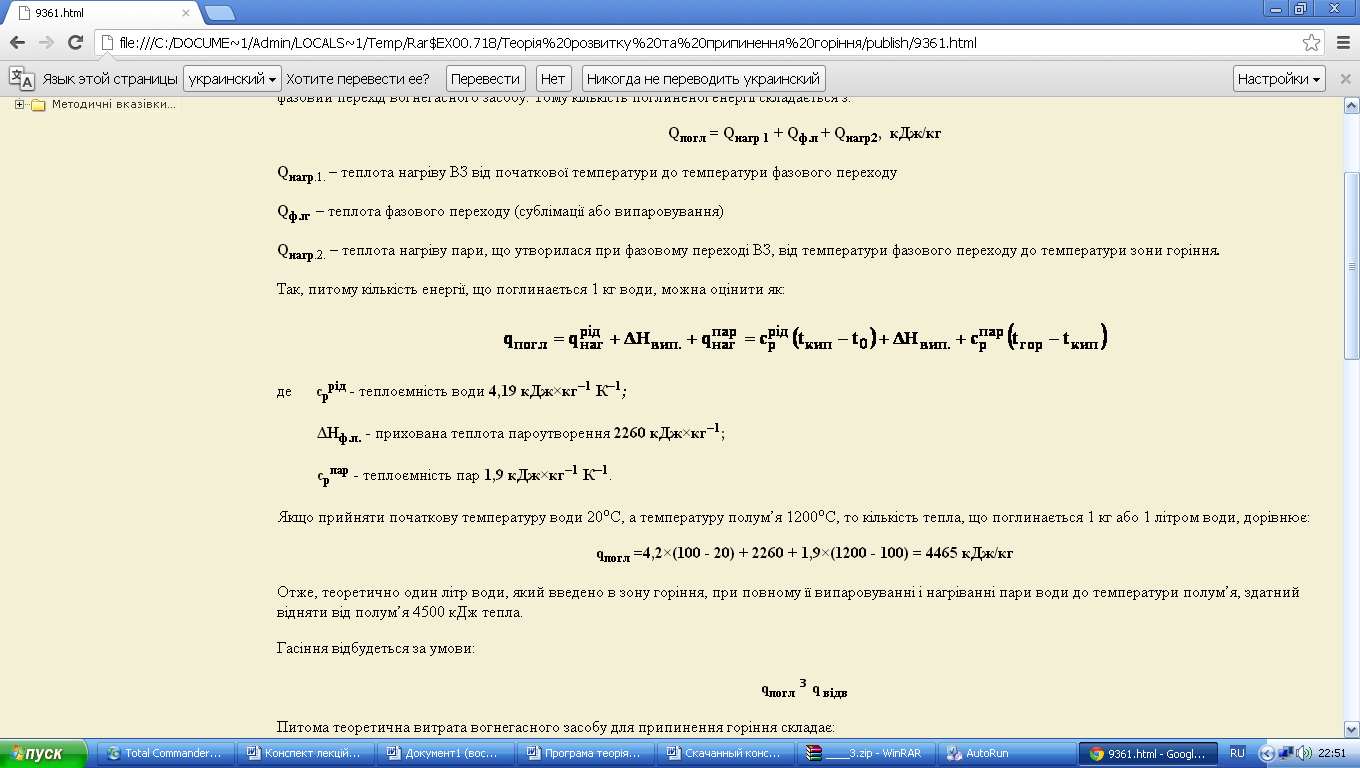
де cррід - теплоємність води 4,19 кДж×кг–1 К–1;
ΔНф.п. - прихована теплота пароутворення 2260 кДж×кг–1;
cрпар - теплоємність пар 1,9 кДж×кг–1 К–1.
Якщо прийняти початкову температуру води 20оС, а температуру полум’я 1200оС, то кількість тепла, що поглинається 1 кг або 1 літром води, дорівнює:
qпогл =4,2×(100 - 20) + 2260 + 1,9×(1200 - 100) = 4465 кДж/кг
Отже, теоретично один літр води, який введено в зону горіння, при повному її випаровуванні і нагріванні пари води до температури полум’я, здатний відняти від полум’я 4500 кДж тепла.
Гасіння відбудеться за умови:
Qпогл q відв
Питома теоретична витрата вогнегасного засобу для припинення горіння складає:

Якщо охолоджується зона горіння, питома витрата води дорівнює:

Якщо вважати, що теплота згоряння більшості вуглеводнів приблизно дорівнює Qн/ = 45000 кДж/кг, можна передбачити, що питома теоретична витрата води повинна складати:
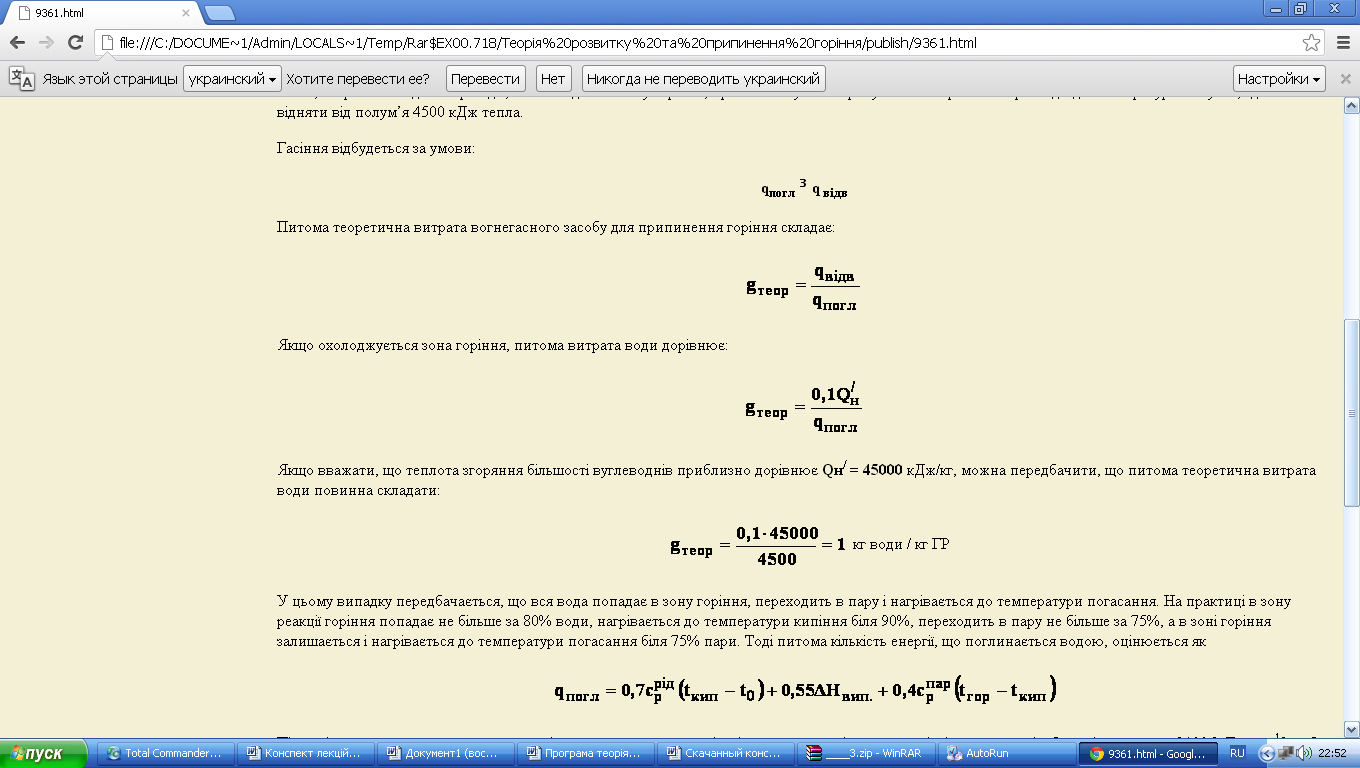
У цьому випадку передбачається, що вся вода попадає в зону горіння, переходить в пару і нагрівається до температури погасання. На практиці в зону реакції горіння попадає не більше за 80% води, нагрівається до температури кипіння біля 90%, переходить в пару не більше за 75%, а в зоні горіння залишається і нагрівається до температури погасання біля 75% пари. Тоді питома кількість енергії, що поглинається водою, оцінюється як
![]()
Після підстановки чисельних значень вхідних величин питома кількість тепла, що відводиться від факела полум'я, буде рівно qпогл = 2100 [кДж×кг–1], тобто приблизно вдвічі менше отриманого раніше значення. Відповідно і питомі витрати води, необхідні для припинення полум'яного горіння, будуть в два рази більше.

З урахуванням масової швидкості вигоряння горючої речовини теоретично необхідна інтенсивність подачі охолоджуючого вогнегасного засобу на гасіння можна розрахувати як

де vm - масова швидкість вигоряння речовини, кг/м мін;
gтеор - питома теоретична витрата води на гасіння, л/кг;
Кп - коефіцієнт поверхні горіння, реальне Кп = 2-2.5;
Але такою малою кількістю води припинити горіння на практиці ніколи не вдавалося. Фактично на пожежі для гасіння подається на багато більше води. Статистика гасіння пожеж показує, що питома витрата води на гасіння пожеж в приміщенні становить біля 200 – 400 л/м2.
Відношення теоретичної інтенсивності подачі вогнегасного засобу до фактичної інтенсивності називається коефіцієнтом використання вогнегасного засобу:

Коефіцієнт використання води на пожежі при подачі її в осередок горіння компактними струменями не перевищує 10%, а в деяких випадках становить 2%. Таким чином, підвищення ефективності використання води на пожежі є однією з головних задач, яку необхідно вирішувати, використовуючи науковий потенціал.
