
- •Міністерство освіти і науки, молоді та спорту україни
- •1. За агрегатним станом компонентів горючої суміші в зоні горіння.
- •2. За способом утворення горючої суміші.
- •3. За механізмом поширення горіння.
- •4. За газодинамічним режимом горіння
- •Методика складання рівнянь реакції горіння.
- •2.1. Ланцюгові реакції
- •2.2. Зародження ланцюгів
- •2.3 Продовження ланцюгів
- •2.4 Хімічні процеси при горінні водню
- •3.1 Визначення матеріального балансу
- •3.2 Витрата повітря на горіння
- •3.5 Горіння індивідуальних речовин в конденсованому стані
- •3.7 Теплота згоряння. Види теплоти згоряння
- •1) Вид горючої речовини:
- •2) Склад горючої суміші:
- •3) Умови, в яких знаходиться горюча суміш:
- •4.1. Визначення полум'я та структура полум'я
- •4.2.Концентраційні межі поширення полум'я
- •4.2.1. Поняття концентраційних меж поширення полум'я
- •4.2.2. Метод визначення концентраційних меж поширення полум'я
- •4.2.3 Чинники, що впливають на концентраційні межі
- •4.2.4. Практичне значення концентраційних меж поширення полум'я
- •5.1 Види виникнення горіння
- •5.2 Теплова теорія само спалахування
- •5.3 Температура самоспалахування речовин
- •5.4 Фактори, що впливають на температуру самоспалахування
- •1) Вид горючої речовини,
- •2) Склад горючої суміші,
- •3) Умови, в яких знаходиться горюча суміш.
- •5.5 Визначення температури самоспалахування а її практичне значення
- •5.6 Класифікація процесів самозаймання. Відмінні особливості самозаймання
- •5.7 Умови, які необхідні для виникнення самозаймання.
- •5.8. Різні види самозаймання теплове самозаймання
- •Хімічне самозаймання
- •Самозаймання речовин при контакті з хімічними окислювачами.
- •Фізичне самозаймання
- •1.1. Механізм фізичного самозаймання вугілля
- •Мікробіологічне самозаймання
- •6.1 Поняття і особливості процесу запалювання
- •6.2 Ініціювання горіння в холодному газі нагрітими тілами
- •6.3 Чинники, що впливають на процес запалювання
- •6.4 Запалювання горючих систем електричними розрядами
- •Τ охол 3 τ хр
- •6.5 Підпалення фрикційними іскрами, краплями розплавленого металу
- •7.1 Загальні закономірності горіння газових сумішей
- •7.2 Закономірності поширення кінетичного горіння в газових сумішах
- •8.1 Загальні закономірності випаровування та горіння рідин
- •8.2 Температурні межі поширення полум'я
- •8.3 Класифікація твердих горючих матеріалів
- •8.4 Загальні закономірності горіння твердих речовин
- •Сргаз(Тзап - Tкип,(розкл))]
- •8.5 Особливості горіння металів
- •8.6 Загальна характеристика і властивості пилу
- •8.7 Запалювання дисперсних систем
- •8.8 Особливості горіння пилу в стані аерозоль та аерогель
- •9.2 Критичний час розвитку пожежі в огорожі.
- •9.6 Визначення висоти нейтральної зони. Методи регулювання газообміну на пожежі.
- •9.1 Динаміка розвитку пожежі в огорожі
- •9.2 Критичний час розвитку пожежі в огорожі
- •9.3 Основні положення інтегральної моделі температурного режиму
- •Фактори, що впливають на температуру пожежі в огородженні
- •9.5 Основні положення зонної моделі температурного режиму
- •Основні закономірності газообміну при пожежі в огородженні
- •9.6 Визначення висоти нейтральної зони. Методи регулювання газообміну на пожежі
- •10.1. Роль концентраційних меж поширеня полум'я у погасанні полум'я
- •10. 2 Погасання полум'я у вузьких каналах
- •11.5 Основи припинення горіння ізоляцією, інгібіруванням, розбавленням.
- •11. 1 Методи та способи припинення горіння
- •Припинення горіння
- •11.2 Запобігання виникнення горючого середовища
- •11.2 Запобігання виникнення горючого середовища та джерел запалювання в ньому
- •11.3 Поняття та загальні вимоги до вогнегасних речовин
- •1. Охолодження
- •2. Розбавлення
- •3. Ізоляція
- •4. Хімічне гальмування реакції горіння
- •11.4 Механізм припинення горіння охолодженням
- •Теоретична інтенсивність подачі води на гасіння пожежі
- •Qпогл q відв
- •Методи підвищення вогнегасної ефективності води на пожежі
- •11.5 Основи припинення горіння ізоляцією, інгібіруванням, розбавленням.
- •Механізм припинення горіння методом розбавлення
- •Список джерел
11.4 Механізм припинення горіння охолодженням
Припинення горіння охолодженням основане на зниженні температури в зоні реакції горіння до температури погасання за рахунок:
· охолодження зони горіння;
· охолодження поверхні конденсованої горючої речовини.
Як було доведено в роботах Я.Б. Зельдовича, критична температура в зоні реакції при гомогенному дифузійному горінні наступає при зниженні температури на величину 3RT2ад/Еакт.

де Тад - адіабатична температура горіння;
Еакт - енергія активації горючої системи.
При цьому швидкість реакції знижується, стає менше граничного значення, за яким процес горіння припиняється. Отже, при температурах нижче за температуру погасання горіння стає неможливим. Графічно ця умова визначається таким чином (рис. 11.1):
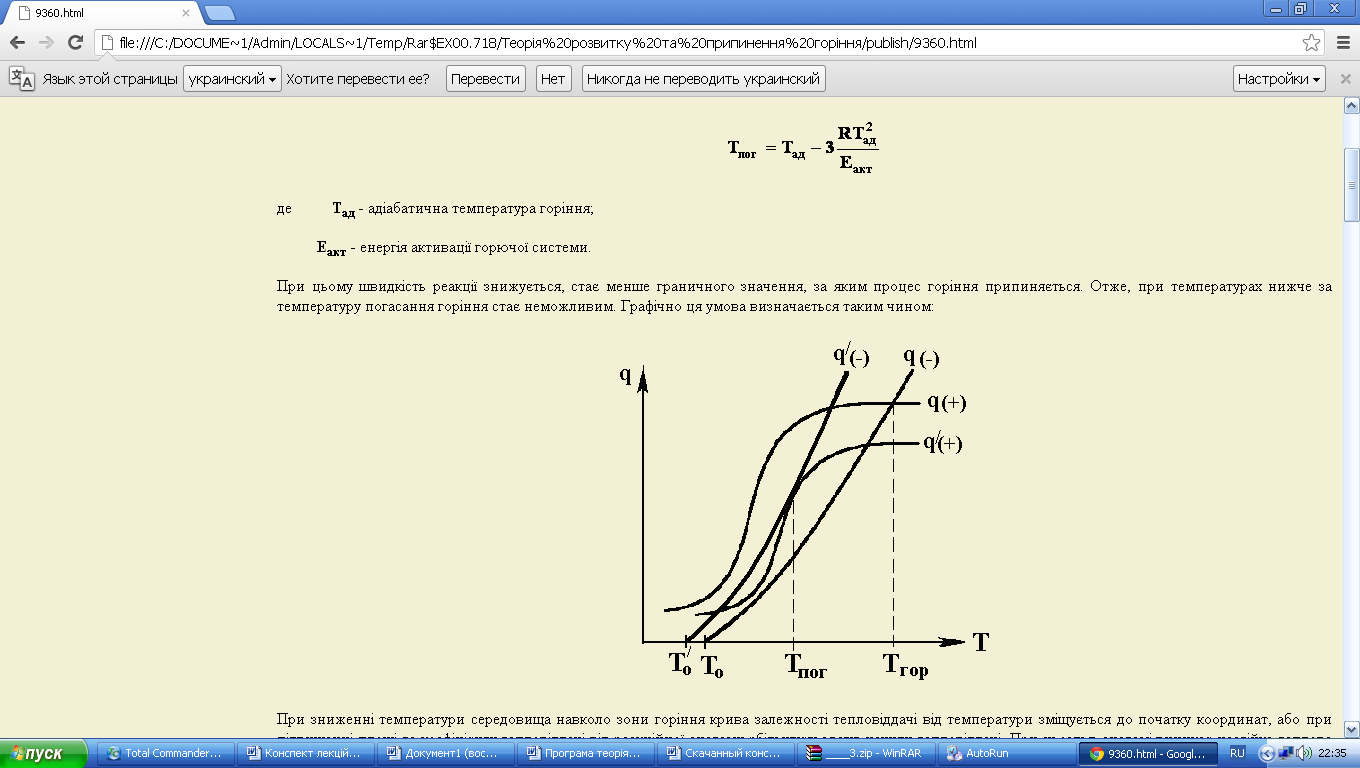
Рис. 11.1
При зниженні температури середовища навколо зони горіння крива залежності тепловіддачі від температури зміщується до початку координат, або при підвищенні площі та коефіцієнту тепловіддачі від реакційної системи збільшується кут нахилу тепловіддачі. При цьому в системі виникає нестійка теплова рівновага, при якій найменше зниження температури приводить до порушення теплового балансу. Система переходить в область низьких температур, швидкоплинна хімічна реакція горіння припиняється.
Отже, якщо охолоджується зона горіння, наприклад, при горінні газів або пароповітряних сумішей умовою припинення горіння є співвідношення:
Тзг < Тпог,
де Тзг – температура в зоні горіння, К;
Тпог – температура погасання, К.
Виконати цю умову можна, якщо забезпечити певну інтенсивність тепловідводу із зони реакції горіння. Необхідну інтенсивність тепловідводу із зони горіння можна оцінити вираженням:

Для більшості вуглеводнів дійсна температура горіння складає 1300-1500 К. Якщо вважати, що початкова температура горючої системи складала 300 К, то можна вважати, що температура системи підвищилась на 1200 К. На це підвищення температури затрачується приблизно 60% загального тепла Qн, яке виділяється при горінні даної горючої речовини (з урахуванням тепловтрат в навколишнє середовище за рахунок променистої теплопередачі). Температура погасання більшості вуглеводнів складає приблизно 1000оС (або 1200-1300 К), отже для припинення горіння методом охолоджування зони горіння потрібно знизити температуру полум’я приблизно на 200ос, або на (200/1200)×100%=17%. Таким чином, для того щоб припинити горіння від зони реакції потрібно відвести 0,17×0,6 Qн = 0,1 Qн.

Оскільки для більшості вуглеводнів теплота згоряння приблизно складає (40-50)×103 кДж×кг–1, то питома кількість відведеної енергії становить:
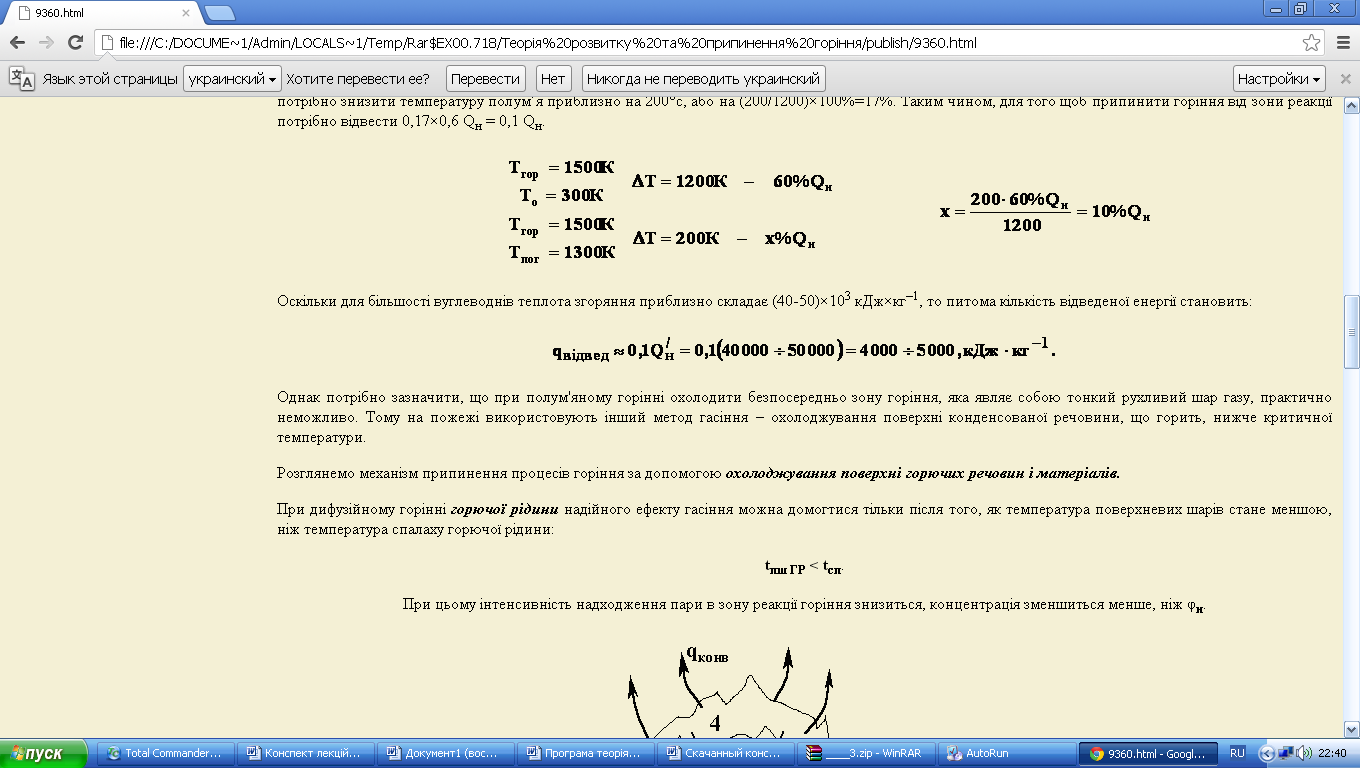
Однак потрібно зазначити, що при полум'яному горінні охолодити безпосередньо зону горіння, яка являє собою тонкий рухливий шар газу, практично неможливо. Тому на пожежі використовують інший метод гасіння – охолоджування поверхні конденсованої речовини, що горить, нижче критичної температури.
Розглянемо механізм припинення процесів горіння за допомогою охолоджування поверхні горючих речовин і матеріалів.
При дифузійному горінні горючої рідини надійного ефекту гасіння можна домогтися тільки після того, як температура поверхневих шарів стане меншою, ніж температура спалаху горючої рідини:
tпш ГР < tсп.
При цьому інтенсивність надходження пари в зону реакції горіння знизиться, концентрація зменшиться менше, ніж φн (рис. 11.2).

Рис. 11.2
1 – горюча рідина;
2 – поверхневий шар, прогрітий вище за температуру спалаху, товщиною δпш;
3 –суміш горючих газів, які утворюються в процесі випаровування;
4 – факел полум’я;
5 – епюра поля температур в рідині при сталому горінні.
Однак, для припинення горіння рідин необхідно не тільки охолодити її поверхневий шар до температури менше tсп, але також і компенсувати тепло, що весь час підводиться до поверхні рідини випромінюванням із зони горіння під час гасіння. Ця умова реалізовується, якщо буде відведено:

де Qвідв. рід – питоме відведення тепла від одиниці площі поверхневого шару горючої рідини, кДж×м-2;
qпром. – інтенсивність променистого теплового потоку від факела полум’я до поверхні горючої рідини, кДж×м-2 с-1;
τгас. – час гасіння, с;
Qзап. гр – питома кількість тепла, яка запасена в прогрітому шарі горючої рідини, віднесена до одиниці площі поверхні рідини, кДж×м-2.
Кількість тепла, що запасена шаром рідини, можна визначити як:
![]()
де сp гр – теплоємність рідини, кДж×кг–1×К–1;
ρгр – густина рідини, кг×м–3;
δпш гр – товщина прогрітого шару рідини, біля 0.005 м;
tсп – температура спалаху рідини, °с
tкип – температура кипіння рідини, °с.
Для припинення гомогенного дифузійного горіння ТГМ можна зробити подібний аналіз умов припинення горіння. Враховуючи, що основна маса газоподібних продуктів попадає в зону реакції горіння при термічному піролізі матеріалу, умову припинення їх виходу можна записати як:
tпш тгм < tпір,
де tтгм - температура поверхневого шару матеріалу, °с;
tпір - температура початку піролізу матеріалу, °с.
Враховуючи, що нагрів твердого горючого матеріалу відбувається як за рахунок променистого, так і за рахунок конвекційного теплообміну, умову охолоджування поверхневого шару можна записати як
![]()
де qкон - інтенсивність конвекційного теплового потоку до поверхні горючої речовини, кДж/(м2 с).
де ts - температура поверхневого шару матеріалу, °С
Крім того, при охолоджуванні палаючих речовин деяка кількість вогнегасних засобів випаровується і переходить в пару, завдяки чому відбувається розбавлення зони горіння негорючими компонентами і підвищується швидкість гасіння.
Вогнегасною речовиною охолоджуючої дії може бути будь-яка речовина, що відповідає загальним вимогам і що має досить високу теплоємність в первинному стані, низьку температуру випаровування або сублімації, велику теплоту фазових переходів і звичайно термічну стійкість в діапазоні температур горіння речовин.
Найбільш відповідними цим вимогам є вода, твердий діоксид вуглецю і зріджений азот.
Вода, як охолоджуючий ВЗ.
Потрапляючи в зону горіння або на поверхню палаючої речовини, вода віднімає велику кількість теплоти. При цьому вона частково випаровується, завдяки чому відбувається розбавлення реагуючих речовин і витіснення повітря із осередку пожежі. Крім того, розтікаючись по поверхні матеріалу, вода ізолює поверхню від дії променистого тепла, перешкоджає виходу горючих пар і газів.
Факторами, що зумовлюють переваги води як вогнегасного засобу, є:
· абсолютна екологічна чистота вогнегасної речовини, відсутність озоноруйнуючого ефекту і токсичності;
· відсутність шкідливого впливу на людей, що перебувають в приміщенні, яке захищається;
· доступність і дешевизна,
· простота зберігання і застосування,
· легкість транспортування води і доставки її в зону горіння (у вигляді компактних струменів) завдяки високій рухливості і малій стисливості;
· термічна стійкість, що набагато перевищує термічну стійкість інших негорючих рідин,
· поглинання теплового випромінювання (захисні екрани);
· адсорбційна здатність води при димоосадженні, що має першорядне значення для забезпечення безпечної евакуації людей з приміщень.
· деякі горючі рідини, змішуючись з водою, утворять негорючі або менш горючі розчини.
Вода є надійним вогнегасним засобом, але у неї є недоліки, через які її застосування для гасіння є малоефективним або неможливим. До негативних можна віднеси такі властивості як:
· порівняно висока реакційна здатність води, що обумовлює неможливість її використання для гасіння речовин, з якими вода бурхливо реагує, або для гасіння металів, температура горіння яких вище за температуру дисоціації води;
· електропровідність води, особливо водних розчинів, що обумовлює неможливість використання води для гасіння електроустановок під напругою.
· порівняно мала в'язкість води через що вода швидко стікає з поверхонь, що горять.
· високий коефіцієнт поверхневого натягнення, що ускладнює проникнення води углиб матеріалу, погано змочує ТГМ і особливо волокнисті матеріали.
· мала питома площа контакту компактних струменів з факелом полум'я, що знижує ефективність охолоджування зони горіння.
· висока температура замерзання води, що ускладнює використання води при від’ємних температурах.
· вода має більшу густину, ніж більшість горючих рідин (нафтопродуктів), що обумовлює занурення води при подачі її на поверхню горючої рідини.
Вогнегасна ефективність води залежить від способу подачі її в осередок пожежі (суцільним або розпиленим струменем).
Твердий діоксид вуглецю.
Твердий діоксид вуглецю частіше використовується в тих випадках, коли застосування води неможливе або малоефективне. Твердий діоксид вуглецю має ряд переваг перед водою:
· не проводить електричний струм;
· має низьку початкову температуру в рідкій фазі - 78.4оС;
· густина менше густини основних рідин;
· на відміну від води він повністю переходить в газову фазу;
· при фазовому переході минає рідку фазу і не змочує матеріалів (сублімація);
· газова фаза, що утворюється, має густину вище за густину повітря і активно флегматизує процес горіння.
Діоксид вуглецю застосовують не тільки для гасіння малих осередків пожежі, але і при гасінні пожеж в силосах елеваторів. У Харківській філії УкрНДІПБ МНС України розроблені методи подачі зрідженого діоксиду вуглецю в середину залізобетонних силосів при допомозі пневматичного пробійника. При такому методі гасіння одночасно відбувається і охолоджування зони горіння і флегматизація продуктів термічного розкладання, що забезпечує запобігання їх запаленню, при вивантаженні продукту, який горить.
Висновок: На основі енергетичного і матеріального балансу процесу горіння можна правильно розрахувати інтенсивність подачі вогнегасних засобів, оптимізувати їх подачу в зону реакції горіння. Це дозволяє розробляти нове пожежно-технічне озброєння, або вдосконалювати те, що є на озброєнні пожежної охорони.
