
- •Міністерство освіти і науки, молоді та спорту україни
- •1. За агрегатним станом компонентів горючої суміші в зоні горіння.
- •2. За способом утворення горючої суміші.
- •3. За механізмом поширення горіння.
- •4. За газодинамічним режимом горіння
- •Методика складання рівнянь реакції горіння.
- •2.1. Ланцюгові реакції
- •2.2. Зародження ланцюгів
- •2.3 Продовження ланцюгів
- •2.4 Хімічні процеси при горінні водню
- •3.1 Визначення матеріального балансу
- •3.2 Витрата повітря на горіння
- •3.5 Горіння індивідуальних речовин в конденсованому стані
- •3.7 Теплота згоряння. Види теплоти згоряння
- •1) Вид горючої речовини:
- •2) Склад горючої суміші:
- •3) Умови, в яких знаходиться горюча суміш:
- •4.1. Визначення полум'я та структура полум'я
- •4.2.Концентраційні межі поширення полум'я
- •4.2.1. Поняття концентраційних меж поширення полум'я
- •4.2.2. Метод визначення концентраційних меж поширення полум'я
- •4.2.3 Чинники, що впливають на концентраційні межі
- •4.2.4. Практичне значення концентраційних меж поширення полум'я
- •5.1 Види виникнення горіння
- •5.2 Теплова теорія само спалахування
- •5.3 Температура самоспалахування речовин
- •5.4 Фактори, що впливають на температуру самоспалахування
- •1) Вид горючої речовини,
- •2) Склад горючої суміші,
- •3) Умови, в яких знаходиться горюча суміш.
- •5.5 Визначення температури самоспалахування а її практичне значення
- •5.6 Класифікація процесів самозаймання. Відмінні особливості самозаймання
- •5.7 Умови, які необхідні для виникнення самозаймання.
- •5.8. Різні види самозаймання теплове самозаймання
- •Хімічне самозаймання
- •Самозаймання речовин при контакті з хімічними окислювачами.
- •Фізичне самозаймання
- •1.1. Механізм фізичного самозаймання вугілля
- •Мікробіологічне самозаймання
- •6.1 Поняття і особливості процесу запалювання
- •6.2 Ініціювання горіння в холодному газі нагрітими тілами
- •6.3 Чинники, що впливають на процес запалювання
- •6.4 Запалювання горючих систем електричними розрядами
- •Τ охол 3 τ хр
- •6.5 Підпалення фрикційними іскрами, краплями розплавленого металу
- •7.1 Загальні закономірності горіння газових сумішей
- •7.2 Закономірності поширення кінетичного горіння в газових сумішах
- •8.1 Загальні закономірності випаровування та горіння рідин
- •8.2 Температурні межі поширення полум'я
- •8.3 Класифікація твердих горючих матеріалів
- •8.4 Загальні закономірності горіння твердих речовин
- •Сргаз(Тзап - Tкип,(розкл))]
- •8.5 Особливості горіння металів
- •8.6 Загальна характеристика і властивості пилу
- •8.7 Запалювання дисперсних систем
- •8.8 Особливості горіння пилу в стані аерозоль та аерогель
- •9.2 Критичний час розвитку пожежі в огорожі.
- •9.6 Визначення висоти нейтральної зони. Методи регулювання газообміну на пожежі.
- •9.1 Динаміка розвитку пожежі в огорожі
- •9.2 Критичний час розвитку пожежі в огорожі
- •9.3 Основні положення інтегральної моделі температурного режиму
- •Фактори, що впливають на температуру пожежі в огородженні
- •9.5 Основні положення зонної моделі температурного режиму
- •Основні закономірності газообміну при пожежі в огородженні
- •9.6 Визначення висоти нейтральної зони. Методи регулювання газообміну на пожежі
- •10.1. Роль концентраційних меж поширеня полум'я у погасанні полум'я
- •10. 2 Погасання полум'я у вузьких каналах
- •11.5 Основи припинення горіння ізоляцією, інгібіруванням, розбавленням.
- •11. 1 Методи та способи припинення горіння
- •Припинення горіння
- •11.2 Запобігання виникнення горючого середовища
- •11.2 Запобігання виникнення горючого середовища та джерел запалювання в ньому
- •11.3 Поняття та загальні вимоги до вогнегасних речовин
- •1. Охолодження
- •2. Розбавлення
- •3. Ізоляція
- •4. Хімічне гальмування реакції горіння
- •11.4 Механізм припинення горіння охолодженням
- •Теоретична інтенсивність подачі води на гасіння пожежі
- •Qпогл q відв
- •Методи підвищення вогнегасної ефективності води на пожежі
- •11.5 Основи припинення горіння ізоляцією, інгібіруванням, розбавленням.
- •Механізм припинення горіння методом розбавлення
- •Список джерел
4.2.Концентраційні межі поширення полум'я
4.2.1. Поняття концентраційних меж поширення полум'я
Досвід показує, що виникнення та поширення горіння в сумішах горючої речовини і окислювача можливе тільки в обмеженому діапазоні їх концентрацій. При спробі підпалити суміші, склад яких виходить за ці межі, стійке горіння не утворюється, і реакція, яка викликана нагріванням в локальній зоні, або не виникає, або затухає на деякій відстані.
Для парогазових сумішей можна виділити як мінімальну, так і максимальну концентрацію горючої речовини, при якій наступають критичні умови виникнення та поширення полум'я. Тобто, для сумішей, які містять горючу речовину і окислювач, розрізнюють нижню і верхню концентраційну межу поширення полум'я φн і φв.
НКМПП - найменша концентрація горючої речовини в суміші з повітрям, при якій вже можливе виникнення та поширення горіння.
ВКМПП - найбільша концентрація горючої речовини в суміші з повітрям, при якій ще можливе виникнення та поширення горіння.
Перші відомості про наявність концентраційних меж були дані в роботі Малляра і Ле-Шателье в 1883 році. Чимало досліджень було присвячено поясненню природи КМПП. На теперішній час існують теплова і ланцюгова теорії поширення полум'я.
Ланцюгова теорія пояснює наявність концентраційних меж існуванням такого стану в системі, коли швидкість утворення активних центрів в розгалужених ланцюгових реакціях дорівнює швидкості обриву реакційних ланцюгів за рахунок загибелі АЦП. При зменшенні концентрації одного із компонентів горючої суміші менше ніж критичне значення швидкість реакції розгалуження стає менше ніж швидкість обриву ланцюгової реакції, отже швидкість реакції горіння в цілому зменшується, система переходить в стан повільної реакції окислення, горіння припиняється.
Теплова теорія пояснює наявність КМПП тепловими втратами від зони реакції в навколишнє середовище. Для виникнення горіння необхідною умовою є перевищення інтенсивності тепловиділення над інтенсивністю тепловіддачі. Інтенсивність тепловтрат збільшується при зменшенні швидкості горіння, оскільки при цьому збільшується тривалість процесу тепловіддачі від кожного елементу нагрітого газу. При певній критичній інтенсивності тепловиділення та тепловіддачі тепловий режим горіння перестає бути стаціонарним, зона реакції прогресивно охолоджується, реакція окислення гальмується, полум’я загасає.
Інтенсивність тепловиділення насамперед залежить від швидкості хімічної реакції:
q(+) = Qн Vгс w хр
Швидкість окислення, в свою чергу, залежить від концентрації компонентів горючої суміші.
W хр = φгрn φокm k exp (-Eакт /RT)
Максимальна швидкість реакції спостерігається при стехіометричному співвідношенні компонентів. По мірі пониження вмісту одного з компонентів горючої суміші (при відхиленні від стехіометричного співвідношення) меншає швидкість хімічної реакції, а з нею і інтенсивність тепловиділення. Значна частина енергії, що виділилася внаслідок взаємодії, затрачується на нагрів газу, який не бере участі в процесі горіння.
Так, при φгр < φстм швидкість тепловиділення меншає
через нестачу пального, а розігрівання існуючого надлишку окислювача приводить до додаткових тепловтрат. При φгр > φстм зниження тепловиділення
відбувається через нестачу окислювача, а тепловтрати збільшуються на розігрівання надлишку палива, що не бере участі в хімічній реакції.
Область концентрації горючої речовини, яка лежить між нижньою і верхньою КМПП, характеризується можливістю запалення і стійкістю горіння суміші і називається областю вибухонебезпечних концентрацій. За концентраційними межами суміші стають вибухобезпечними. Але якщо при концентраціях горючої речовини менше НКМПП не можливо виникнення ніякого горіння, то при концентраціях горючої речовини більше ВКМПП можливе виникнення дифузійного горіння при виході струменю газу в навколишній простір і наявності джерела запалювання (сумішоутворення до потрібних горючих концентрацій буде відбуватися в зоні горіння).
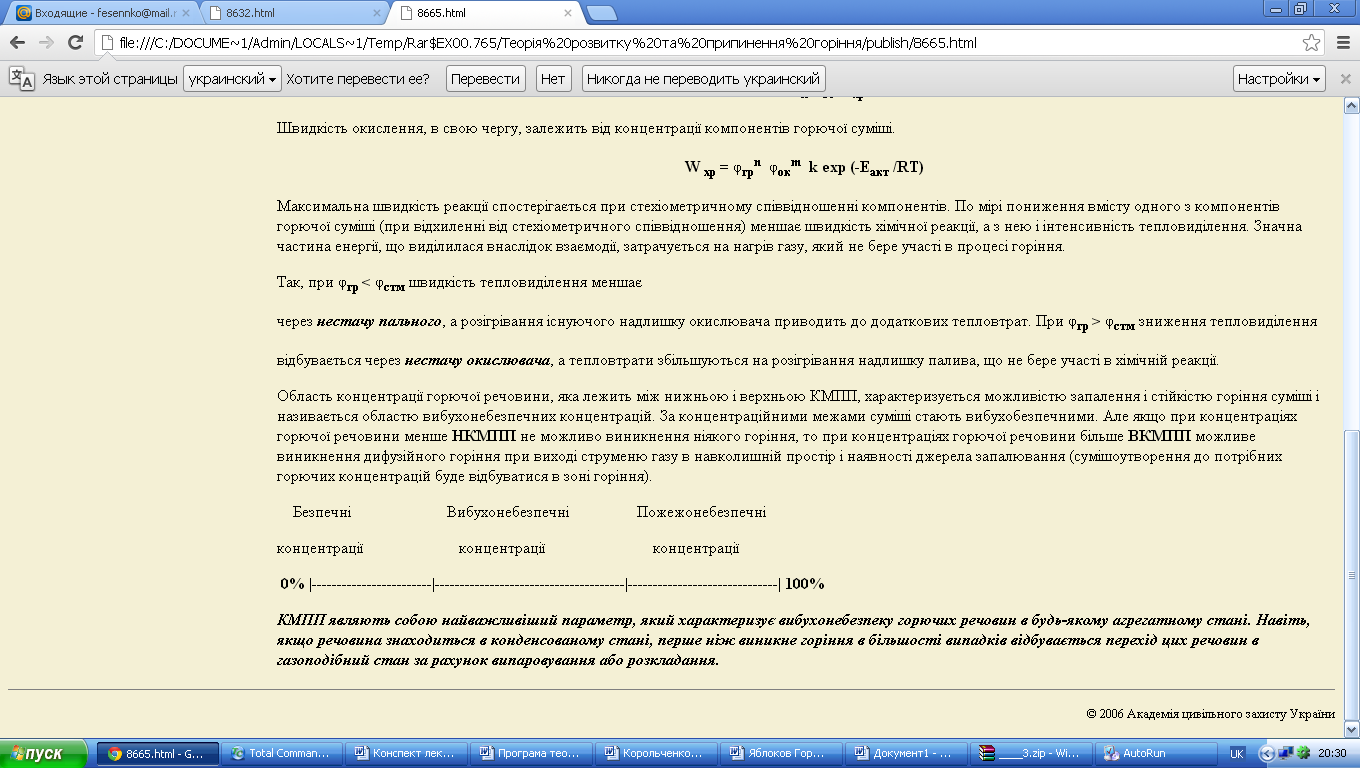
КМПП являють собою найважливіший параметр, який характеризує вибухонебезпеку горючих речовин в будь-якому агрегатному стані. Навіть, якщо речовина знаходиться в конденсованому стані, перше ніж виникне горіння в більшості випадків відбувається перехід цих речовин в газоподібний стан за рахунок випаровування або розкладання.
