
monomers-Платэ-книга
.pdf
311
ние к хлориду палладия таких компонентов, как хлорид лития, катализирует процесс пиролиза этилидендиацетата до винилацетата и уксусной кислоты.
В начале ХХI столетия ~ 66% производимого в мире винилацетата– мономера - вырабатывают из этилена, 33% - из ацетилена и 1% - из ацетальдегида и уксусного ангидрида. Имеется также устойчивый интерес к процессу получения винилацетата через этилидендиацетат.
8.5. ПРОИЗВОДНЫЕ ПОЛИВИЛОВОГО СПИРТА – ПОЛИВИНИЛАЦЕТАЛИ
Поливинилацетали сами по себе или в виде сополимеров
—CH—CH2—CH—CH2— —CH2—CH— —CH2—CH— |
|||
O— CHR—O |
x |
OH y |
OCOCH3 z |
где R = H, Alk, фурфурильная и другие группы, являются важнейшими производными поливинилового спирта, имеющими большое техническое значение. Они получаются обычно конденсацией поливинилового спирта с различными альдегидами или гидролизом поливинилацетата с последующим присоединением альдегида (или кетона) к образовавшемуся поливиниловому спирту.
Впервые поливинилацеталь был синтезирован В. Германом и В. Генелем в 1927 г., а первое промышленное производство поливинилацеталей было организовано в Канаде в 1932 г.
Наибольшее промышленное значение имеют поливинилформаль, поливинилбутираль, поливинилэтилаль, поливинилформальэтилаль и поливинилкеталь.
Поливинилформаль содержит винилформальные звенья
—CH—CH2—CH—CH2— |
|
O— CH2 —O |
x |
Его получают ацеталированием поливинилового спирта формальдегидом в водной среде при 363-368 К в присутствии в качестве катализатора соляной или какой-либо другой кислоты. Выход продукта составляет 68-72%. Поливинилформаль применяют главным образом для производства электроизоляционных лаков, стойких к действию масел, жиров, как связующее при изготовлении магнитных лент для звуко- и видеозаписи. Из смесей поливинилформаля с синтетическими каучуками, имеющими повышенную ударную вязкость, формуют изделия для машиностроения и электротехники.

312
Поливинилбутираль – аморфный бесцветный полимер, содержащий 6578% винилбутиральных звеньев
—CH—CH2—CH—CH2— O—-CH-—O
CH2—CH2—CH3 n
а также 32-19% винилспиртовых и до 3% винилацетатных звеньев. В промышленности поливинилбутираль получают обработкой масляным альдегидом поливинилового спирта в водной среде, а также его суспензии в органических растворителях, в которых поливинилбутираль растворяется. Пластифицированный поливинилбутираль применяют в производстве безосколочных стекол типа триплекс, спиртовые растворы поливинилбутираля используют для изготовления некоторых синтетических клеев (типа БФ), лаков, грунтовок, эмалей. Методом газопламенного напыления поливинилбутираля на металлические изделия получают антикоррозионные и декоративные покрытия.
Поливинилэтилаль содержит винилэтилальные, винилспиртовые и винилацетатные звенья. Его используют для производства лаков и политур, пластифицированный полимер перерабатывают литьем под давлением, экструзией и выдуванием.
Поливинилформальэтилаль содержит винилметилальные, винилэтилальные, винилспиртовые и винилацетатные звенья. Его применяют для производства электроизоляционных лаков.
Поливинилкеталь, получаемый взаимодействием поливинилового спирта с циклогексаноном, содержит винилкетальные, винилспиртовые и винилацетатные звенья. Его используют в композициях с резольными и другими термореактивными смолами для изготовления термостойких клеев и высокопрочных термостойких эмалей, для изоляции проводов и деталей электротехнических приборов.


315
|
|
|
|
433 |
623 |
O |
|
O |
CO |
|
|
|
|
|
n |
|
|
|
|
|
|
478 |
- |
O |
SO2 |
O |
CO |
|
|
|
|
|
|
n |
|
|
|
|
|
428 |
521 |
O |
C(CH3)2 |
O |
CO |
|
|
|
|
|
|
n |
|
O |
C(CH3)2 |
O |
O |
423 |
- |
|
|
||||
|
|
|
NO2 |
n |
|
|
|
|
|
|
|
|
|
|
|
453 |
523 |
O |
|
C(CH3)2 |
O |
|
|
N=N n
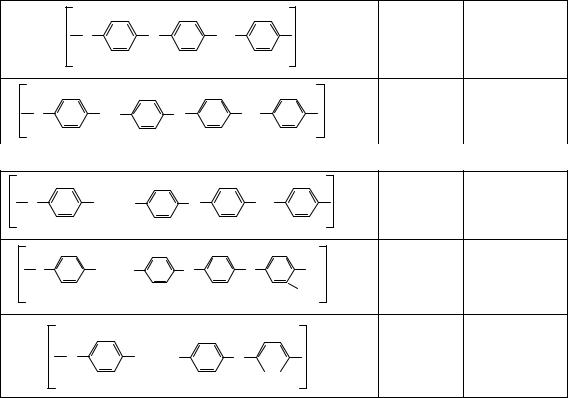
Наличие полярных групп и высокая гибкость макромолекул обусловливают относительно хорошую растворимость простых полиэфиров. Они, однако, характеризуются значительно меньшей термической стойкостью, чем полиолефины.
Из простых полиэфиров наибольшее практическое применение нашли полиформальдегид, полиметилен-, полиэтилен- и полипропиленоксиды, полиацетальдегид, политетрагидрофуран, пентапласт, пропиленоксидный и эпихлоргидриновые каучуки, полифениленоксиды, полиариленсульфоны, поли- 1,4-эпоксициклогексан, поли-1,2,5,6-диэпоксигексан, поли-1,2- поксициклогексан.

316
9.1. ФОРМАЛЬДЕГИД
Формальдегид Н2С=О – мономер, широко применяемый для получения полиформальдегида. Полиформальдегид (полиметиленоксид, полиоксиметилен) [—СН2—О—]n - полимер со степенью полимеризации выше 1000, т. пл. 448-453 К, т. стекл. 213 К. Он растворяется только в моногидрате гексафторацетона и гексафторацетоноксиме.
Полиформальдегид применяют, главным образом, как литьевой конструкционный материал в машино-, автомобиле- и приборостроении, для выработки полиформальдегидных волокон, которые используются для производства фильтровальных тканей, рыболовных изделий, канатов и швейных ниток. По теплостойкости полиформальдегидные волокна уступают полиамидным, но превосходят полипропиленовые. Они устойчивы в органических растворителях, нефтепродуктах, щелочах, к действию микроорганизмов, но недостаточно устойчивы в минеральных кислотах.
В промышленности полиформальдегид получают анионной или катионной гомополимеризацией формальдегида и катионной сополимеризацией формальдегида или триоксана.
9.1.1 Механизм и катализаторы окислительного дегидрирования метанола
Основной промышленный метод получения формальдегида - окислительное дегидрирование метанола кислородом воздуха:
CH3OH + 0,5O2  CH2O + H2O Н = 147,4 кДж/моль.
CH2O + H2O Н = 147,4 кДж/моль.
Процесс осуществляют в присутствии твердых катализаторов, как правило, серебряных и в значительно меньших масштабах – оксидных.
Первая промышленная установка окислительного дегидрирования метанола на медном катализаторе была построена в Германии в начале 90-х годов XIX века. В качестве сырья использовали метанол лесохимического происхождения. В 20-е годы ХХ-ого столетия были разработаны серебряные катализаторы, существенно более эффективные, чем медные.
Механизм окислительного дегидрирования метанола
Окислительное дегидрирование метанола сопровождается реакцией простого дегидрирования и рядом других побочных реакций:
CH3OH |
CH2O + H2 |
Н = -93,4 кДж/моль, |
CH3OH + 1,5O2 |
CO2 + 2H2O |
Н = 575,1 кДж/моль, |
CH2O + 0,5O2 |
HCOOH |
Н = 270,4 кДж/моль, |
HCOOH +0,5O2 |
CO2 + H2O |
Н = 14,5 кДж/моль , |

|
|
|
317 |
HCOOH |
CO + H2O |
Н = -53,7 кДж/моль, |
|
2CH2O + H2O |
CH3OH + HCOOH |
Н = 122,0 кДж/моль, |
|
H2 + 0,5O2 |
H2O |
|
Н = 241,8 кДж/моль, |
2CH3OH + CH2O |
CH2(OCH3)2 + H2O |
Н = 131,0 кДж/моль, |
||
|
|
Метилаль |
|
|
2CH2O |
HCOOCH3 |
Н = 132,6 кДж/моль, |
||
HCOOH + (n-1)CH2O |
|
HCOO(CH2O)nCH2OH , |
||
CO + 0,5O2 |
CO2 |
|
Н = 283,0 кДж/моль, |
|
2CO |
CO2 + C |
|
окислительного |
Н = 172,5кДж/моль, |
Константа равновесия реакции |
дегидрирования значи- |
|||
тельно выше, чем реакции простого дегидрирования. Это означает, что реакция может развиваться до практически полного исчерпания реагента - в данном случае, кислорода, взятого в недостаточном количестве. Степень превращения метанола по целевой реакции окислительного дегидрирования составляет ~60%, а по остальным реакциям - 10%. Подавляющее большинство побочных реакций экзотермичны и поэтому суммарный тепловой эффект положителен. Реально процесс осуществляется без отвода тепла, т.е. в условиях адиабатического режима.
Рассмотрение приведенных выше реакций показывает, что ключевые превращения протекают с увеличением объема, а побочные – как с увеличением объема, так и с уменьшением объема реакционной смеси. В связи с тем, что реакционная смесь разбавлена азотом, система мало чувствительна к изменению давления (объема). Термодинамические расчеты показали, что изменение общего давления от 0,01 до 1 МПа практически не влияет на состав продуктов.
Активными центрами катализатора дегидрирования являются поверхностные оксиды серебра, на которых сорбируются метанол и кислород. В процессе хемосорбции кислорода осуществляется перенос заряда с атомов серебра на адсорбированный кислород, и поверхность заряжается отрицательно. При степени покрытия серебра кислородом до 0,10-0,12 см3 О2/м2 Ag, т.е. в пределах покрытия поверхности монослоем кислорода, один атом кислорода связан с двумя поверхностными атомами серебра (Ag2O). С увеличением степени окисления до 0,22-0,26 см3 О2/м2 Ag преобладают соединения, в которых атом кислорода связан с одним атомом поверхностного серебра (Ags или Ags2O2). При дальнейшем возрастании степени окисления образуются структуры с большим содержанием кислорода на один атом серебра. Структуры всех типов можно
представить в виде: |
|
|
|
|
|
|
|
|
|
O |
O |
|
|
O— O |
|
|
O—O—O |
|
|
|
|
|
|||||||
Ags Ags ; |
Ags ; |
Ags Ags ; |
Ags Ags |
||||||

318
Каталитическая специфичность серебра объясняется особым состоянием кислорода на серебре. В то время, как на других металлах при активированной адсорбции кислорода возникают только атомные ионы О- (или О2-), вызывающие окисление исходного продукта до диоксида углерода, на серебре возникают поверхностные молекулярные ионы типа О2- (или О22-). За мягкое окисление метанола в формальдегид ответственен относительно прочно связанный с катализатором ион О-. Более прочно связанный с поверхностью ион О2- способствует образованию формальдегида по реакции дегидрирования метанола. Исследования по окислению спиртов на серебре в условиях наложения на катализатор электрического заряда показали, что отрицательный заряд увеличивает выход формальдегида, а положительный - уменьшает. Наложение отрицательного заряда, т.е. избыток электронов, увеличивает долю ионов О2- и О-, наиболее прочно связанных с поверхностью катализатора, и селективность процесса повышается. Таким образом, превращение метанола в формальдегид на серебре - окислительно-восстановительная реакция.
Под действием хемосорбированного на поверхности серебра кислорода происходит ассоциативная адсорбция метанола, который, в отличие от кислорода, распадается не на ионы, а на радикалы. Методами ЯМР-, ЭПР- и массспектроскопии было найдено, что при 653-903 К на поверхности серебра образуются свободные радикалы: СН3, ОН-, НО2 . Некоторые из протекающих на поверхности реакций можно представить схемой:
s
O2(г) 2O
2O
s |
[О] (CH3O ) + (HO ) |
CH3OH  (CH3OH)адс.
(CH3OH)адс.
 (CH3 ) + (HO2 )
(CH3 ) + (HO2 )
(CH2O) + O2 |
(HCO ) + (HO2 ) |
[о] |
(HCO ) + (H ) |
(CH2)O
CO + H2
(H ) + O2 (HO2 )
(HO2 )
(HCO ) + O2  (HO2 ) + CO и т.д.
(HO2 ) + CO и т.д.

319
Как свободные радикалы, так и молекулы реагентов, могут диффундировать с поверхности в объем. Большинство побочных реакций развивается под влиянием высокой температуры в свободном пространстве между зернами катализатора, а также в объеме под слоем катализатора до зоны резкого охлаждения (закалки) продуктов реакции. К числу этих превращений относятся реакции полного окисления и распада, протекающие по свободнорадикальному цепному механизму.
При температурах, применяемых обычно на практике, скорость превращения метанола в формальдегид лимитируется подводом реагентов к поверхности зерен катализатора, т.е. процесс протекает во внешнедиффузионной области. Кинетическая область протекания процесса реализуется при температуре ниже 573 К. Выход формальдегида и степень конверсии метанола в этих условиях не превышают соответственно 3,6 и 4,6% (мол.), рис. 9.1.
Рис. 9.1. Зависимость степени конверсии кислорода от линейной скорости потока реагентов и от температуры реакции
Циркуляционно-проточная установка, катализатор – нарезанная серебряная проволока 0,5- 1,0 мм)
При температурах выше 643-673 К процесс переходит в область внешней диффузии. Протекание процесса в диффузионной области обусловливает значительную разность концентраций реагентов и продуктов реакции на поверхности серебра и в потоке. Само химическое взаимодействие между реагентами происходит очень быстро и разогрев катализатора настолько велик, что он оказывается достаточным для поддержания высокой температуры реакции.
Термодинамический расчет равновесия реакции дегидрирования (1) и окислительного дегидрирования (2) метанола в формальдегид в интервале температур 573-1073 К показывает, что равновесие существенно смещено в сторону образования продуктов реакции. При этом значения константы равновесия реакции окислительного дегидрирования (2) метанола на 5-20 порядков выше соответствующих значений для простого дегидрирования (1), рис. 9.2.
Рис. 9.2. Температурная зависимость константы равновесия реакции дегидрирования (1) и окислительного дегидрирования (2) метанола в формальдегид.

320
Итак, реакция (1) может протекать до практически полного исчерпания компонента, взятого в недостаточном количестве. Поскольку таким компонентом является кислород, последний расходуется полностью, а метанол подвергается лишь дегидрированию и распаду. Согласно расчетам мольная доля метанола, израсходованного на окислительное дегидрирование в условиях технологического процесса, составляет 60%, а на дегидрирование - 40%.
Если на входе в реактор метанольно-воздушная смесь нагрета до 413-433 К, то температура в слое катализатора за счет разогрева достигает 923-1023 К. Основным параметром, позволяющим регулировать температуру процесса, является соотношение кислород:метанол. Чем больше кислорода подается в реактор с сырьем, тем выше температура в реакторе. Зависимость показателей процесса от температуры представлена на рис. 9.3. Как видно из рисунка, с повышением температуры степень конверсии (1) метанола возрастает.
Рис. 9.3. Зависимость параметров процесса и состава отходящих газов от температуры реакции
Катализатор - 20% серебра на алюмосиликате, нагрузка по метанолу - 2500 кг/м2 · ч; сырье - 90%-й метанол.
1 – степень конверсии метанола; 2 -селективность по формальдегиду; 3 - выход формальдегида; 4-7 - содержание в отходящих газах H2, CO, CO2 и O2 соответственно.
Селективность процесса (2) практически постоянна при повышении температуры от 673 до 973 К, но с дальнейшим ростом температуры она снижается. Выход (содержание) водорода и оксидов углерода (4-6) с увеличением температуры возрастает.
Поскольку на выходе из слоя катализатора реакция образования формальдегида практически прекращается, а термический распад продолжается, селективность процесса уменьшается. В связи с этим продукты реакции подвергают закалке, т.е. резкому охлаждению на выходе из реактора путем смеше-

 Cl n
Cl n