
monomers-Платэ-книга
.pdf
281
7.6.5. Получение других алкилметакрилатов
Синтез метакриламида
Метакриламид СН2=С(СН3)СОNН2 является мономером для производства полиметакриламида и акриловых сополимеров. Из сополимеров метакриламида с N-метилметакриламидом и метилметакрилатом вырабатывают органические стекла с повышенной теплостойкостью.
Метакриламид представляет собой бесцветные кристаллы с т. пл. 383-384 К, растворяется в воде, метакрилонитриле, этилацетате, пропионитриле.
В промышленности метакриламид получают из ацетонциангидрина:
(CH3)2C(OH)CN H2SO4 |
CH2=C(CH3)CN |
|
398-413 К |
|
|
CH2=C(CH3)CONH2 H2SO4 |
NH3 |
CH2=C(CH3)CONH2. |
|
||
Сульфат метакриламида обрабатывают аммиаком, карбонатами или гидроксидами щелочных металлов в воде. Метакриламид очищают перекристаллизацией из бензола, этилацетата или сублимацией в вакууме. Выход метакриламида составляет ~ 96%.
Метакриламид можно получать также омылением метакрилонитрила в присутствии серной кислоты или гетерогенных катализаторов; аммонолизом метилметакрилата водным раствором аммиака, изомеризацией оксима метакролеина на меднохромовом катализаторе, Однако все эти способы пока не получили промышленного развития.
Синтез гидроксиэтилметакрилата
В 60-х годах XX столетия чешский ученый О. Вихтерле предложиил использовать полиоксиэтилметакрилат в качестве материала для контактных линз (в виде сшитого гидрогеля). Эти линзы стали носить миллионы людей во всем мире и потребовалась организация промышленного производства мономера – гидроксиэтилметакрилата (этиленгликольмонометакрилат).
CH2=C—C-O—CH2—CH2OH CH3 O
Гидроксиэтилметакрилат получают этерификацией метакриловой кислоты этиленгликолем:

282
O |
|
O |
CH2=C—C |
+ OHCH2CH2OH -H2O |
CH2=C—C |
CH3 OH |
|
CH3 OCH2CH2OH |
|
|
Гидроксиэтилметакрилат |
7.7.ОЛИГОЭФИРАКРИЛАТЫ
Олигоэфиракрилаты (полиэфиракрилаты) – олигомерные сложные и простые эфиры с концевыми или регулярно чередующимися акриловыми (метакриловыми, хлоракриловыми и др.) группами. Олигоэфиры – бесцветные прозрачные нелетучие жидкости различной вязкости или твердые бесцветные кристаллические продукты с молекулярной массой 300-5000.
Олигоэфиракрилаты, при синтезе которых образуются сложноэфирные группы, получают в промышленности обратимой конденсационной теломеризацией путем введения в конденсацию наряду с диили полифункциональными реагентами (спиртами и карбоновыми кислотами) регуляторов роста цепи - телогенов. Последние содержат группу, принимающую участие в конденсации, а также полимеризационно-способную группу, не участвующую в конденсации. Телогенами служат кислоты акрилового ряда и их моноэфиры с диоксисоединениями.
Исходными соединениями для синтеза олигоэфиракрилатов служат:
-гликоли, полиолы или двухатомные фенолы, например моно-, ди- и триэтиленгликоли, 1,3- пропиленгликоль, 1,4- бутиленгликоль, 1,6- гексаметиленгликоль, триметилпропан, глицерин, пентаэритрит, ксилит, дифенилпропан, фенолфталеин;
-алифатические дикарбоновые насыщенные кислоты с числом метиленовых групп в цепи 2-8, а также ароматические двухили полиосновные кислоты либо их ангидриды, например изофталевая, терефталевая, тримеллитовая кислоты, фталевый ангидрид;
-α,β- ненасыщенные монокарбоновые кислоты акрилового ряда, как
правило, акриловая и метакриловая кислоты. Для синтеза олигоэфиров с ограниченной горючестью и рядом других специфических свойств используют галогенсодержащие компоненты.
Процессы производства мономеров для получения олигоэфиракрилатов рассмотрены в настоящей и других главах.

283
Глава 8
спирты и виниловые эфиры
Из полимерных спиртов и их производных наибольшее промышленное значение имеют: поливиниловый и полиаллиловые спирты; простые эфиры поливинилового спирта – винилметиловый, винилизопропиловый, винил-н- бутиловый, винилизобутиловый; сложные эфиры поливинилового спирта, например поливинилацетат; производные поливинилового спирта – поливинилацетали, например поливинилбутираль, поливинилэтилаль, поливинилформальэтилаль, поливинилкеталь.
Оптическими материалами, успешно конкурирующими с неорганическим стеклом при производстве оптических изделий, являются полимеры на основе диэтиленгликольбис(аллилкарбоната). Линзы из полиаллилгликолькарбоната отличаются малой плотностью (в 2-2,5 раза легче стеклянных) и пониженной тенденцией к запотеванию. Важно, что при разрушающих ударах не образуются опасные осколки. Преимуществом линз из этого материала является большой срок эксплуатации по сравнению с линзами из акрилового и карбонатного стекол.
Американская фирма "Юнион Оптикал Корп." разработала способ получения гидрогелевых контактных линз на основе сополимеров N- аллилпирролидона-2 с глицидилметакрилатом в присутствии инициатора.
Большой интерес представляют ненасыщенные аллиловые мономеры, содержащие одновременно карбаматную и карбонатную функциональные группы, имеющие структурную формулу
СН2=СН—СН2—ОСNН-(СН2)2-ОС-(СН2)2-НNCО-СН2—СН=СН2.
О |
О |
О |
Эти материалы используют для производства органических стекол, обладающих отличными прочностью, гибкостью и абразивостойкостью.
Французская фирма "Сосьетэ Насьональ де Пудр э эксплозив" также разработала способ получения смешанных аллилакриловых мономеров, содержащих и карбаматную, и карбонатную функциональные группы общей формулы
СН2=СН—СН2-ОС |
|
|
|
|
|
|
R1 |
NН-R—ОСО |
-(СН2)2-ОС |
|
—С=СН2 , |
||||
|
|
|
|||||
О |
О |
О |
|||||
где R-Alk, содержащий 1-4 атома углерода; R1 = Н или СН3.
284
Полимеры на основе этих соединений применяют для изготовления прозрачных и твердых изделий в строительстве (панели, оконные стекла и т.д.), в автомобилестроении (для ветровых стекол и т.д.).
8.1.ПОЛИВИНИЛОВЫЙ И АЛЛИЛОВЫЙ СПИРТЫ
Поливиниловый спирт [-CH2CH(OH)-]n – водорастворимый полимер, устойчивый к действию большинства органических растворителей, разбавленных кислот и щелочей, к действию света. При 443-493 К начинается деструкция поливинилового спирта, сопровождающаяся дегидратацией и образованием карбонильных групп. Поливиниловый спирт используют для производства поливинилспиртовых волокон, которые применяют в производстве тканей и трикотажа, в качестве носителя лекарственных средств. В Японии из нетканного поливинилового спирта делают синтетическую бумагу.
Поливиниловый спирт в отличие от других полимеров нельзя синтезировать полимеризацией как бы исходного мономера СН2=СН—ОН, его получают омылением простых и сложных эфиров. Это объясняется тем, что виниловый спирт в свободном состоянии не существует. При попытке его синтеза, например нагреванием винилбромида с водой, образуется изомерный виниловому спирту ацетальдегид.
Предпринимались неоднократные попытки синтезировать поливиниловый спирт полимеризацией ацетальдегида в присутствии различных катализаторов: триэтиламина, ацетиленидов, амидов, ртутных амальгам щелочных металлов и других соединений. Однако в результате этих процессов получаются лишь химически неоднородные олигомеры с молекулярной массой до 3000. Поэтому синтез поливинилового спирта осуществляют путем превращений полимеров простых и сложных виниловых эфиров. Простые виниловые эфиры (винилбензиловый, винил-трет-бутиловый и др.) используют в основном для препаративного синтеза поливинилового спирта. В промышленных условиях поливиниловый спирт получают омылением наиболее доступного и дешевого полимера сложного винилового эфира – поливинилацетата.
Полимеры аллилового спирта начали выпускать в промышленном масштабе в 1946 г. после того как был разработан синтез аллилового спирта из пропилена.
Аллиловый спирт (пропен-2-ол-1) представляет собой бесцветную жидкость с едким запахом; т. пл. 275,15 К, т. кип. 369,9 К и D420 0,850.Обладает высокой реакционной способностью, хорошо растворяется в обычных химических растворителях, смешивается с водой в любых соотношениях.

285
Аллиловый спирт используют для получения глицерина, акролеина, глицидилового спирта, простых и сложных аллиловых эфиров:
OH |
OH- |
H2C=CH—CH2OH Cl2; H2O ClCH2—CH—CH2OH |
|
HCl |
Cl; H2O |
 H2C—CH—CH2OH
H2C—CH—CH2OH
O
Глицерин получают взаимодействием аллилового спирта с пероксидом водорода:
H2C=CH—CH2OH + H2O2  H2C—CH—CH2OH
H2C—CH—CH2OH
OH OH OH
Аллиловый спирт, а также аллиловые эфиры, эпихлоргидрин, глицерин получают из аллилхлорида:
 H2C=CH—CH2OH
H2C=CH—CH2OH  Аллиловые эфиры H2C=CH—CH2Cl Аллиловый спирт
Аллиловые эфиры H2C=CH—CH2Cl Аллиловый спирт
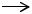 ClCH2—CH(OH)—CH2Cl
ClCH2—CH(OH)—CH2Cl 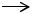 H2C—CHCH2Cl
H2C—CHCH2Cl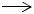
О ЭпихлоргидO рин
 CH2(OH)—CH(OH)—CH2OH
CH2(OH)—CH(OH)—CH2OH
Глицерин
Аллилхлорид, в свою очередь, образуется в результате высокотемпературного хлорирования пропилена:
CH2=CH—CH3 Cl2 CH2=CH—CH2Cl.
HCl
Аллиловый спирт может быть получен не только в результате щелочного гидролиза аллилхлорида, но также гидролизом в присутствии катализатора. Гидролиз осуществляется 0,2%-ным раствором хлорида одновалентной меди в 2,5-3,0%-ной соляной кислоте при 350 К. В качестве побочных продуктов наряду с диаллиловым эфиром образуется пропионовый альдегид (вследствие изомеризации спирта под влиянием кислоты):
СН2=СН—СН2ОН Н+ СН3—СН2—СНО.

286
В промышленности аллиловый спирт получают также восстановлением акролеина вторичными спиртами. При этом происходит каталитическое перераспределение водорода с восстановлением вторичных спиртов в кетоны в паровой фазе над оксидными катализаторами – оксидами магния или цинка:
СН2=СНСН О2 СН2=СН-СНО |
СН3СН(ОН)СН3 |
О |
||||
|
||||||
|
СН2=СНСН2ОН + СН3 |
|
|
|
ССН3. |
|
|
|
|
||||
Способ получения аллилового спирта через акролеин предпочтительнее метода хлорирования пропилена и гидролиза аллилхлорида вследствие использования вместо хлора и щелочи более дешевого вспомогательного агента – воздуха.
Полимеры аллиловых соединений получают полимеризацией аллилового спирта и его производных.
Из других полимерных спиртов практическое значение имеют поливинилацетиленовые спирты, которые образуются из винилацетилена и кетонов в присутствии едкого кали. При этом получаются стекловидные продукты, способные склеивать самые разнообразные материалы, включая металлы.
8.2. ОСНОВЫ ПРОЦЕССОВ ВИНИЛИРОВАНИЯ
Реакция винилирования представляет собой введение винильной группы в молекулу органического соединения путем замещения атома водорода. Промышленное значение приобрели процессы винилирования ацетиленом соединений, содержащих реакционноспособный атом водорода, например, карбоновых кислот, спиртов, аминов, амидов. Реакцию винилирования в общем виде можно представить схемой:
CH CH + RXH  CH2=CH—RX,
CH2=CH—RX,
где Х = O, S или N.
Впервые синтез виниловых эфиров был осуществлен А.М. Бутлеровым в 1870 г. взаимодействием ацетилена с алифатическими спиртами в присутствии катализаторов:
CH CH + ROH  CH2=CH-OR.
CH2=CH-OR.

287
Эту реакцию можно проводить в присутствии в качестве катализатора сульфата ртути:
ROH + CH CH |
Hg2+ |
CH2=CH-OR. |
Однако интенсивно протекающая побочная реакция присоединения второй молекулы спирта с образованием ацеталей
ROCH=CH2 + ROH |
H+ |
(RO)2CH—CH3 |
затрудняет промышленное использование этого метода.
Большой вклад в исследование реакций винилирования внесли В. Реппе, А.Е. Фаворский, М.Ф. Шостаковский. Наличие в молекуле винильной группы придает соединению способность к полимеризации, поэтому многие подобные вещества являются мономерами для производства полимерных материалов.
Более удобный способ синтеза простых виниловых эфиров является винилирование спиртов в присутствии щелочей, открытое А.Е. Фаворским. Реакция протекает без заметного образования ацеталей с выходом целевого продукта ~ 95%.
Карбоновые кислоты также реагируют с ацетиленом в жидкой фазе в присутствии серной кислоты и сульфата ртути. Однако первичный продукт реакции – сложный виниловый эфир - способен к дальнейшему присоединению кислоты с образованием насыщенных диэфиров. Так, при винилировании уксусной кислоты ацетиленом образуются винилацетат и этилидендиацетат:
CH CH + CH3COOH |
CH2=CH-OCOCH3 |
CН3COOH |
(CH3COO)2CHCH3. |
|
Винилацетат |
|
Этилидендиацетат |
Вследствие высокой токсичности ртутных катализаторов и низкой селективности реакций ртутные катализаторы не получили распространения в промышленности.
Промышленное применение в качестве катализаторов получили соли цинка. Реакция протекает через промежуточное образование -комплексов металла с ацетиленом с последующей атакой углеродного атома ацетилена, имеющего частичный положительный заряд, молекулой карбоновой кислоты и заключительным разрушением комплекса в кислой среде:
|
+ |
+ |
OH |
||
СH CH + Zn2+ |
|
|
+ |
||
|
|||||
CH CH CH3COOH |
СН≡CH ← O=C—CH3 Н |
||||
|
|
|
↓ |
||
|
|
Zn2+ |
Zn2+ |
||

288
O
 СH2=CH—OC—CH3 + Zn2+.
СH2=CH—OC—CH3 + Zn2+.
Практическое значение имеют также соли одновалентной меди. Хлорид меди (I) мало растворим в воде и для повышения его каталитической активности обычно добавляют соли, образующие с ним растворимые комплексы. Так, при введении в катализаторный раствор хлорида аммония образуется комплекс
Cu2Cl2 2NH4Cl.
Ацетилен с солями одновалентной меди дает комплексные соединения, когда в -комплексе углеродные атомы ацетилена приобретают частичный положительный заряд.
Винилирование ацетиленом может протекать и по атому азота в аминах или амидах, обладающих слабокислыми свойствами вследствие сопряжения аминогруппы с соседними ненасыщенными связями или ароматическими системами, как, например, в -пирролидоне или карбазоле:
CH2—CH2 |
CH2—CH2 |
CH CH + CH2 C=O |
CH2 C=O |
NH |
N—СН=СН2 |
Реакционная способность спиртов при винилировании уменьшается с повышением их кислотности. Поэтому из насыщенных одноатомных спиртов медленнее всех реагирует метиловый спирт. В качестве катализаторов реакции винилирования спиртов используют алкоголяты или гидроксиды щелочных металлов.
Винилирование триэтаноламина ацетиленом приводит к образованию мо- но-, ди- и тривиниловых эфиров, представляющих интерес как азотсодержащие мономеры:
(HOCH2CH2)3N + CH CH |
|
CH2=СH-OСH2СH2N(СH2СH2OH)2 |
|
||
|
(CH2=CH-OCH2CH2)2NCH2CH2OH |
|
|
||
|
|
(CH2=CH-OCH2CH2)3N |
|
|
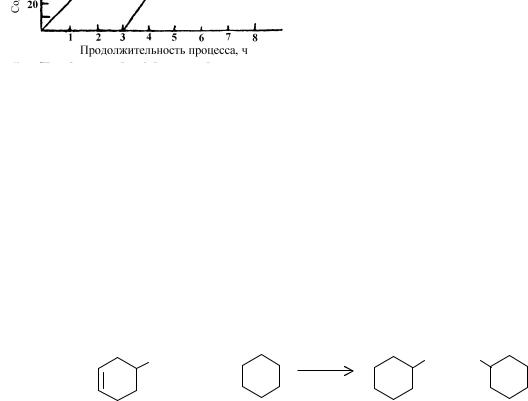
Присутствие в триэтаноламине трех гидроксильных групп, по которым происходит винилирование, делает процесс винилирования весьма чувствительным к условиям его проведения. Процесс осуществляют в интервале температур 433-473 К и давлении от 0,2 до 1,2 МПа. В качестве катализатора используют КОН. Содержание продуктов винилирования триэтаноламина в реакционной смеси в зависимости от продолжительности процесса показано на рис. 8.1. Как видно из рисунка, в начальный период реакции наблюдается образова-
289
ние только моновинилового эфира (МВЭ), затем дивинилового (ДВЭ) и тривинилового (ТВЭ) эфиров.
Рис. 8.1. Зависимость содержания продуктов винилирования триэтаноламина в реакционной смеси от продолжительности процесса.
По аналогичной схеме, взаимодействием циклогексана с ацетиленом может быть получен винилциклогексен. Однако вследствие высокой реакционной способности винилциклогексен реагирует далее со второй молекулой циклогексана с образованием дициклогексилэтана:
CH=CH2 + |
CH2-CH2 |
8.3. ПРОСТЫЕ ВИНИЛОВЫЕ ЭФИРЫ
Простые виниловые эфиры ROCH=CH2 являются мономерами для получения
поливиниловых эфиров, которые представляют собой жидкие, каучукоподобные или твердые (в зависимости от длины R), светостойкие, химически инертные, термостойкие (до 473-523 К) продукты, обладающие высокой адгезией к различным поверхностям.
Олигомеры винилизобутилового эфира – прекрасное средство для заживления ран и ожогов (М.Ф. Шостаковский, Ф.П. Сидельковская).
Промышленное производство простых виниловых эфиров и продуктов на их основе было начато в Германии в начале 30-х годов ХХ-го столетия, а позднее и в США по технологии, разработанной В. Реппе. В 1966 г. американская фирма "Дженерал энд Филм Корп." начала промышленный выпуск винилметилового и других винилалкиловых эфиров. Обычно выпускаются следующие эфиры:
290
Эфиры для |
Эфиры для |
промышленного использования |
исследовательских целей |
Винилметиловый |
Винилпропиловый |
Винилизопропиловый |
Винил-трет-бутиловый |
Винил-н-бутиловый |
Винилизооктиловый |
Винилизобутиловый |
Винил-2-этилгексиловый |
Винилэтиловый |
Винилгексадециловый |
Винилоктадеиловый |
Винилдодециловый |
|
Винил-н-гидроксибутиловый |
|
Дивиниловый эфир бутандиола-1,4 |
|
Дивиниловый эфир диэтилегликоля |
Виниловые эфиры производятся также фирмами "Юнион Карбайд"(США), БАСФ (ФРГ), "АйСиАй" (Великобритания). В Советском Союзе до 1978 г. в опытно-промышленном масштабе вырабатывался лишь винилбутиловый эфир. Ереванским отделением НПО "Пластполимер" в 1975-1978 гг. был разработан процесс получения виниловых эфиров гликолей.
В промышленном масштабе производят гомополимеры винилметилового, винилэтилового, винилизобутилового, винилбутилового и винил-н-бутилового и винилоктадецилового эфиров и некоторые их сополимеры.
Виниловые эфиры в промышленности получают в основном следующими способами:
-из ацетилена и соответствующих спиртов;
-термическим разложением ацеталей;
-переэтерификацией и алкоголизом винилацетата;
-дегидрированием -галогенэфиров;
-из этилена и спиртов.
Наибольшее распространение получил синтез виниловых эфиров из ацетилена и соответствующих спиртов.
8.3.1. Получение простых виниловых эфиров винилированием спиртов
Винилирование спиртов можно проводить как под избыточным давлением ацетилена, так и при атмосферном давлении при условии, если температура кипения спирта выше температуры синтеза.
Винилирование спиртов при атмосферном давлении
Винилирование при атмосферном давлении можно вести и в жидкой фазе, и в реакторах с неподвижным слоем катализатора. Наибольшее распростране-
