
Анестезиология и интенсивная терапия (Гельфанд Б.Р
.).pdf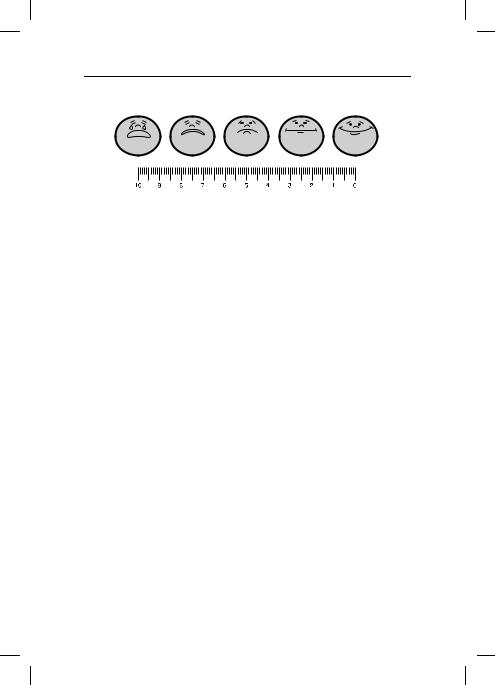
5.Вопросы общей и частной анестезиологии
5.9.1.1.ВизуальноFаналоговая шкала
Рис. 45. Определение интенсивности боли
10 — мучительная нестерпимая боль; 0 — нет боли. Пациенту предлагается сделать на этой линейке отметку, соответствующую интенсивности испытываемых им в данный момент болей.
5.9.1.2. Словесная рейтинговая шкала
•Нет болей.
•Крайне слабые.
•Едва заметные.
•Очень слабые.
•Слабые.
•Легкие.
•Умеренные.
•Беспокоящие.
•Сильные.
•Интенсивные.
•Очень сильные.
•Крайне интенсивные.
•Особо интенсивные.
•Непереносимые.
•Мучительные.
5.9.2. Лекарственные препараты, наиболее часто используемые для лечения острой боли
•Неопиоидные аналгетики (парацетамол, НСПВП).
•Опиоиды и опиаты (наркотические анальгетики).
•Местные анестетики.
•Центральные α адренопозитивные препараты (клофе лин и его аналоги).
321

Анестезиология и интенсивная терапия
•Ингибиторы протеаз.
•Вспомогательные лекарственные средства (бензодиазе пины, кофеин, декстроамфетамин, дифенин, карбама зепин, фенотиазины, бутирофеноны).
5.9.2.1. Парацетамол
Парацетамол (ацетаминофен) — неселективный инги битор ЦОГ 1 и ЦОГ 2, действующий преимущественно в центральной нервной системе.
Парацетамол оказывает анальгетическое и жаропони жающее действие, подавляя простагландиновую синтетазу в гипоталамусе, препятствует выработке спинального про стагландина и тормозит синтез оксида азота в макрофагах.
Препарат способен снижать выраженность центральной гиперальгезии, что подтверждает центральный механизм его действия.
При пероральном приеме парацетамола возможны зна чительные колебания концентрации препарата в плазме в раннем послеоперационном периоде, в том числе опасно достижение высоких уровней (Petterson P., 2004).
Появление внутривенной формы существенно повыси ло ценность и расширило показания к применению препа рата в качестве базисного компонента мультимодальной послеоперационной анальгезии. Внутривенная форма пре восходит таблетированные формы по безопасности, по скольку характеризуется более предсказуемой плазменной концентрацией в раннем послеоперационном периоде.
Использование внутривенной формы предпочтительно у пациентов групп высокого риска, особенно с патологией печени.
Инъекционный парацетамол представляет собой рас твор для инфузии, в миллилитре которого содержатся 10 мг парацетамола. Показаниями для назначения инъекционно го парацетамола являются:
•болевой синдром умеренной интенсивности, особенно после хирургических вмешательств;
•лихорадочный синдром на фоне инфекционно воспа лительных заболеваний.
322

5. Вопросы общей и частной анестезиологии
Способ применения — в/в однократная инфузия в тече ние 15 мин. Для борьбы с послеоперационной болью инфу зию инъекционного парацетамола в дозе 1 г можно начи нать уже перед переводом больного из операционной в вос становительную палату, так как болеутоляющий эффект достигает максимума через 1 ч после введения. В послеопера ционном отделении инфузии инъекционного парацетамола можно проводить с минимальным интервалом в 4 ч. Макси мальная суточная доза парацетамола для взрослых — 4 г.
5.9.2.2. Нестероидные противовоспалительные препараты
НСПВП широко используют для лечения острой и хронической боли. Они не вызывают эйфории, угнетения дыхания, лекарственной зависимости.
5.9.2.2.1. Дозирование нестероидных противовоспалительных препаратов
Препарат |
Доза |
Т1/2 |
Кратность |
|
(мг/сут) |
(ч) |
приема (сут) |
Карбохолиновые кислоты |
|
|
|
|
|
|
|
Салициловые кислоты: |
|
|
|
Ацетилсалициловая кислота |
1000—6000 |
4—15 |
2—4 |
(аспирин) |
|
|
|
|
|
|
|
Неацетилированные салицилаты: |
|
|
|
Холинтриацетилат магнезии |
1500—5000 |
4—15 |
2—4 |
(трилизат) |
|
|
|
Салицил салицилат (дисальцид) |
1500—5000 |
4—15 |
2—4 |
Дифлюнизал (долобид) |
500—1500 |
7—15 |
2 |
|
|
|
|
Уксусная кислота |
|
|
|
|
|
|
|
Индолы: |
|
|
|
Индометацин (индоцин) |
50—200 |
3—11 |
2—4 |
Сулиндак (хлинорил) |
300—400 |
16 |
2 |
|
|
|
|
Пиролуксусная кислота: |
|
|
|
Толметин (толектин) |
600—2000 |
1—2 |
3—6 |
Кеторолак (торадол) |
75—150 в/м |
3—8 |
4 |
|
или в/в, |
3—8 |
4 |
|
40 — энте> |
|
|
|
рально |
|
|
|
|
|
|
|
|
|
323 |

Анестезиология и интенсивная терапия
|
|
|
Окончание |
|
|
|
|
|
|
Препарат |
Доза |
Т1/2 |
Кратность |
|
|
(мг/сут) |
(ч) |
приема (сут) |
|
|
|
|
|
|
Фенилацетиловые кислоты: |
|
|
|
|
Диклофенак (вольтарен) |
150 |
2 |
2—4 |
|
|
|
|
|
|
Пропионовые кислоты |
|
|
||
|
|
|
|
|
Фенилацетиловые кислоты: |
|
|
|
|
Ибупрофен (мотрин) |
1200—3200 |
2 |
3—6 |
|
Фенопрофен (налфон) |
1200—3200 |
2 |
3—4 |
|
Флурбипрофен (ансайд) |
200—300 |
3—4 |
2—3 |
|
Кетопрофен (кетонал, орудис) |
100—400 |
2 |
3—4 |
|
|
|
|
|
|
Нафтипропионовые кислоты: |
250—1500 |
13 |
2 |
|
Напроксен (напросин, анапрокс) |
||||
|
|
|
||
|
|
|
|
|
Антраниловые кислоты |
|
|
||
|
|
|
|
|
Фенаматы: |
200—400 |
2—3 |
4 |
|
Меклофенамат (мекломен) |
||||
|
|
|
||
|
|
|
|
|
Пиразолы |
|
|
||
|
|
|
|
|
Фенилбутазон (бутазолидин) |
200—800 |
40—80 |
1—4 |
|
|
|
|
|
|
Оксикамы |
|
|
||
|
|
|
|
|
Пироксикам (Фельден) |
20 |
30—86 |
1 |
|
|
|
|
|
|
Принципиальный механизм противовоспалительного действия НСПВП обусловлен подавлением активности циклооксигеназы (ЦОГ) — ключевого фермента синтеза гипералгезических простагландинов. ЦОГ имеет 2 изофор мы — ЦОГ 1 и ЦОГ 2, обладающие соответственно физио логическим цитопротективным действием и индуцируемым провоспалительным.
НСПВП, подавляющие преимущественно активность ЦОГ 1 (например, ацетилсалициловая кислота), чаще вы зывают поражение ЖКТ, чем препараты, подавляющие преимущественно ЦОГ 2 или обладающие равноэффектив
324
5. Вопросы общей и частной анестезиологии
ным действием в отношении обеих ЦОГ (диклофенак нат рия) либо времязависимым эффектом в отношении ЦОГ 1 (ибупрофен).
5.9.2.2.2. Патогенетическая классификация НСПВП
Селективные ингибиторы ЦОГ>1
Низкие дозы ацетилсали> циловой кислоты
Неселективные ингибиторы ЦОГ
Большинство известных НСПВП
Преимущественно селективные
Мелоксикам, нимесулид
ингибиторы ЦОГ>2
Специфические ингибиторы ЦОГ>2 |
Целекоксиб, рофекоксиб |
Среди неселективных НСПВП наибольший интерес представляет кетопрофен (кетонал).
Время достижения максимальной концентрации кетопрофена в плазме
Способ введения |
Тmax при различных способах |
|
введения кетопрофена |
|
|
Внутрь |
1—2 ч |
|
|
Ректально |
2,4—4 ч |
|
|
Парентерально |
15—30 мин |
|
|
Аппликационно |
5—8 ч |
|
|
Препарат характеризуется быстрым и мощным анальге тическим эффектом, сравнимым с опиоидным, отличается коротким периодом полувыведения (1,5—2 ч), исключаю щим кумуляцию, не оказывает угнетающего воздействия на кроветворение.
Весьма эффективна комбинация НСПВП с наркотиче скими анальгетиками (возможность уменьшить дозу и крат ность введения опиоида при сохраненном высоком аналь гетическом эффекте).
325

Анестезиология и интенсивная терапия
5.9.3. Опиоидные анальгетики
Одно из наиболее эффективных средств при острой и хронической боли. Необходимо индивидуально подби рать путь введения, дозы и интервалы между приемами пре парата.
Пути введения опиоидов: per os, в/м и в/в введение.
5.9.3.1. Per os
Оптимальный путь введения для больных с хронической болью в связи с удобством и простотой. Анальгетический эффект развивается в течение 30—60 мин.
5.9.3.2. Внутримышечное введение
|
Эквианальгетическая |
Начальная доза внутрь |
|||
|
|
доза (мг) |
|||
|
|
|
|
||
Препарат |
|
|
|
|
|
|
Внутрь |
Паренте+ |
Взрослым |
Детям |
|
|
рально1 |
(мг) |
(мг/кг) |
||
|
|
|
|||
|
|
|
|
|
|
Морфин |
30 |
|
10 |
15—30 |
0,3 |
|
|
|
|
|
|
Гидроморфон |
7,5 |
|
1,5 |
4—8 |
0,06 |
|
|
|
|
|
|
Оксикодон |
30 |
|
— |
15—30 |
0,3 |
|
|
|
|
|
|
Метадон |
20 |
|
10 |
5—10 |
0,2 |
|
|
|
|
|
|
Леворфанол |
4 |
|
2 |
2—4 |
0,04 |
|
|
|
|
|
|
Фентанил |
— |
|
0,1 |
— |
— |
|
|
|
|
|
|
Оксиморфон |
— |
|
1 |
— |
— |
|
|
|
|
|
|
Меперидин |
300 |
|
75 |
—2 |
—2 |
1 Стандартные дозы для в/м введения взрослым при острой боли. Для однократного в/в болюсного введения используют половину дозы для в/м введения. Для детей младше 6 месяцев доза для в/в введения = па> рентеральная эквианальгетическая доза × масса тела (кг)/100.
2 Не рекомендуется.
326

5.Вопросы общей и частной анестезиологии
5.9.3.3.Внутривенное введение
•Болюс.
•Продолжительная инфузия.
•Контролируемое пациентом обезболивание (КПО).
Болюсное введение — наиболее быстрый способ дости жения аналгезии. Быстрее действуют те препараты, которые более липофильны. КПО — метод, использующий быстрый анальгетический эффект болюсного введения.
Контролируемая пациентом аналгезия
|
|
Препарат |
|
|
Параметры режима |
|
|
|
|
Морфин |
Гидро+ |
Мепери+ |
||
|
||||
|
морфон |
дин |
||
|
|
|
|
|
Концентрация (мг/мл) |
1 |
0,5 |
10 |
|
|
|
|
|
|
Доза по требованию (мл) |
1 |
0,5 |
1 |
|
|
|
|
|
|
Интервал блокировки (мин) |
6 |
10 |
6 |
|
|
|
|
|
|
Скорость постоянной инфузии (мл/час): |
|
|
|
|
Днем |
0 |
0 |
0 |
|
Ночью |
0,5 |
0,5 |
0,5 |
|
|
|
|
|
|
Предельная доза за 1 ч (мл) |
< 12 |
< 6 |
< 10 |
|
|
|
|
|
|
Нагрузочная доза (каждые 5 мин до |
2 |
0,5 |
2 |
|
сост. комфорта) (мг) |
||||
|
|
|
||
|
|
|
|
|
Максимальная нагрузочная доза (мг) |
10—15 |
2—4 |
75—150 |
|
|
|
|
|
Указанные дозы рассчитаны на пациентов с массой тела 55—70 кг, не принимающих опиоиды; следует корригиро вать дозы в соответствии с состоянием пациента, опытом приема опиоидов и т.д.
Метод КПО можно применять и у детей. Важно, чтобы ребенок понимал связь между стимулом (боль), действием (нажатие кнопки) и ожидаемым результатом (болеутоле ние), для того чтобы КПО было эффективным.
Для детей младшего возраста и новорожденных с острой послеоперационной болью применяют продолжительную инфузию морфина (10—25 мкг/кг/ч).
327

Анестезиология и интенсивная терапия
Дети младше 7 лет
Используют разведенный раствор 0,2 мг/мл.
Параметры |
Доза (мг/кг) |
|
|
|
|
Скорость постоянной инфузии (в 1 ч) |
0,01—0,05 |
|
|
|
|
Предельная доза за 1 ч |
0,03 |
|
|
|
|
Начальная болюсная доза |
0,02 |
|
(каждые 5 мин до состояния комфорта) |
||
|
||
|
|
|
Максимальная болюсная доза |
0,1 |
|
|
|
|
При усиливающейся боли |
В 2—3 раза увеличи> |
|
вают скорость инфузии |
||
|
||
|
|
|
При отсутствии доступа в вены, если необхо> |
0,05—0,1 |
|
димо парентеральное введение морфина |
||
|
||
|
|
Дети от 7 до 11 лет
Эти дети часто могут освоить метод КПО; для него при
меняют разведенный раствор 0,2 |
мг/мл. |
||
|
|
|
|
Возраст |
Средняя масса тела (кг) |
|
Режим КПО* |
|
|
|
|
7—8 лет |
20 |
|
1/6/0 |
|
|
|
|
9—11 лет |
30 |
|
2/6/0 |
|
|
|
|
* Разовая доза/интервал блокировки/скорость инфузии во время сна.
Дети от 12 до 15 лет
Эти дети могут хорошо освоить метод КПО; для него применяют стандартный раствор 0,1 мг/мл, у подростков старше 15 лет терапия как у взрослых.
Возраст |
Средняя масса тела (кг) |
Режим КПО* |
|
|
|
12—14 лет |
40—50 |
0,5/6/0 |
|
|
|
15 лет |
> 50 |
1/6/0 |
|
|
|
* Разовая доза/интервал блокировки/скорость инфузии во время сна.
328

5. Вопросы общей и частной анестезиологии
5.9.3.4.Трансдермальное применение
Фентанил, будучи высоколипофильным веществом, лег ко проникает через кожу. Наклейки с фентанилом позволяют поддерживать постоянную концентрацию препарата в кро ви с помощью системы, которую заменяют каждые 3 суток. Трансдермальная система высвобождает препарат со скоро стью 25 мкг/ч. Максимальный болеутоляющий эффект пос ле наложения наклейки развивается в течение 24—72 ч.
5.9.3.5. Ректальное введение опиоидов
Этот путь введения широко не примеяется, однако явля ется хорошей альтернативой в/в пути введения, особенно если тот недоступен. Из прямой кишки опиоиды быстро всасываются и попадают в систему нижней полой вены, а затем, минуя печень, в системный кровоток.
5.9.3.6. Эпидуральное введение
Обеспечивает полноценное интра и послеоперацион ное обезболивание.
Эпидуральная аналгезия предпочтительна в следующих случаях:
•при выполнении хирургических вмешательств на груд ной клетке или верхнем этаже брюшной полости;
•при операциях на нижнем этаже брюшной полости при тяжелых заболеваниях легких;
•при операциях на нижних конечностях при необходи мости ранней мобилизации;
•при вмешательствах на сосудах нижних конечностей, если желательна симпатэктомия.
Особенности эпидуральной аналгезии у детей
У детей от 1 года до 7 лет рекомендуется применять смесь 0,1% раствора бупивакаина и раствора фентанила (3 мкг/мл). Грудным детям нельзя добавлять фентанил в эпидуральные смеси, поскольку они очень чувствительны к опиоидам (легко возникает угнетение дыхания).
329

Анестезиология и интенсивная терапия
Возраст |
Раствор |
|
|
|
|
До 1 года |
0,1% раствор бупивакаина |
|
|
|
|
1—7 лет |
Смесь 0,1% раствора бупивакаина и раствора фента> |
|
нила 3 мкг/мл |
||
|
||
|
|
|
Старше 7 лет |
Смесь 0,1% раствора бупивакаина и раствора фента> |
|
нила 10 мкг/мл |
||
|
||
|
|
Зуд, задержка мочеиспускания и тошнота — нередкие побочные эффекты, встречающиеся при эпидуральной ин фузии опиоидов. Эти симптомы легко устраняются введе нием налоксона в дозе 0,04—0,1 мг в/в. При развитии избы точной седации и угнетения дыхания доза налоксона составляет 0,1—0,4 мг в/в.
Эпидуральный катетер, как правило, удаляют через 3— 7 суток. Эпидуральная аналгезия заменяется п/о приемом НСПВП и других препаратов.
5.9.4. Сбалансированная (мультимодальная) аналгезия
Сбалансированная (мультимодальная) аналгезия преду сматривает одновременное использование двух или более анальгетиков, обладающих различными механизмами дейст вия и позволяющих достичь адекватного обезболивания при минимуме побочных эффектов, присущих назначению боль ших доз одного анальгетика в режиме монотерапии. Напри мер, эпидуральное введение опиоидов должно сочетаться с аналогичным введением местных анестетиков, внутривенная анальгезия опиоидами успешно комбинируется с назначе нием НПВП, обладающих опиоид сберегающим эффектом.
В настоящее время сбалансированная анальгезия явля ется методом выбора для послеоперационного обезболива ния. Ее базисом является назначение парацетамола и НПВП, которое у пациентов с болью средней и высокой интенсив ности сочетается с внутривенным (подкожным, внутримы шечным) введением опиоидных анальгетиков и/или ис пользованием методов регионарной анальгезии.
330
