- •И.С. Колпащикова, е.Р. Кофанов, е.М. Алов углеводороды. Галогенпроизводные углеводородов
- •1. Алканы
- •1.1. Гомологический ряд, изомеры
- •Гомологический ряд алканов. Число структурных изомеров
- •1.2. Строение метана
- •1.3. Строение этана
- •1.4. Вращение вокруг простой углерод-углеродной связи. Конформации
- •1.5. Физические свойства
- •1.6. Химические свойства
- •1.6.1. Хлорирование и бромирование метана. Механизм реакции
- •1.6.2. Строение метильного радикала
- •1.6.3. Расчет изменения энергии в ходе реакции
- •1.6.4. Энергетическая диаграмма реакции. Связь энергии
- •Хлорирования метана
- •Бромирования метана
- •1.6.5. Причина различной реакционной способности галогенов
- •Зависимость реакционной способности галогенов от энергии связи h–Hal
- •1.6.6. Галогенирование высших алканов. Механизм
- •1.6.7. Медленная стадия. Энергетическая диаграмма
- •1.6.8. Причина различной устойчивости радикалов
- •1.6.9. Зависимость скорости образования радикалов
- •1.6.10. Расчет реакционной способности различных связей
- •1.6.11. Селективность в реакциях хлорирования
- •Малореакционного Br• с пропаном
- •1.6.12. Нитрование
- •1.6.13. Сульфоокисление и сульфохлорирование
- •1.6.14. Окисление
- •1.6.15. Термическое разложение алканов, крекинг
- •1.6.16. Ионные реакции алканов
- •1.7. Методы синтеза алканов
- •1.7.1. Гидрирование алкенов и алкинов
- •1.7.2. Реакция Вюрца
- •1.7.3. Гидрирование галогеналканов
- •2.2. Плоскополяризованный свет. Оптическая активность
- •2.3. Строение молекул и оптическая активность
- •2.4. Обозначение конфигураций
- •2.5. Соединения с несколькими хиральными центрами.
- •2.6. Методы разделения энантиомеров
- •3. Циклоалканы
- •3.1 Номенклатура. Изомерия
- •3.2. Физические свойства
- •3.3. Строение
- •Теплоты сгорания и энергии напряжения циклоалканов
- •3.4. Химические свойства
- •3.5. Способы получения
- •4.2. Строение этена
- •4.3. Физические свойства
- •Физические свойства алкенов
- •4.4. Химические свойства
- •4.4.1. Гидрирование. Теплота гидрирования
- •4.4.2. Теплота гидрирования и устойчивость алкенов
- •4.4.3. Присоединение галогенов
- •4.4.3.1. Механизм реакции
- •4.4.3.2. Реакционная способность галогенов в реакции АdЕ
- •4.4.4. Присоединение галогеноводородов
- •4.4.4.1. Механизм реакции
- •4.4.4.2. Направление электрофильного присоединения
- •К пропену
- •4.4.4.3. Реакционная способность и селективность
- •4.4.4.4. Перегруппировка
- •Механизм реакции
- •4.4.5. Присоединение бромистого водорода в присутствии
- •1. Инициирование:
- •2. Рост цепи:
- •3. Обрыв цепи:
- •4.4.6. Присоединение серной кислоты
- •4.4.7. Гидратация алкенов. Присоединение спиртов
- •4.4.8. Гидроборирование алкенов
- •4.4.9. Алкилирование алкенов
- •4.4.10. Полимеризация алкенов
- •4.4.11. Окисление
- •4.4.12. Реакция аллильного замещения. Галогенирование
- •4.5. Способы получения алкенов
- •Характеристики химических связей в молекуле алкинов
- •Характеристики связей с-н в алканах, алкенах и алкинах
- •5.2. Физические свойства
- •5.3. Химические свойства
- •5.3.1. Реакции присоединеня
- •5.3.1.1. Каталитическое гидрирование и восстановление
- •5.3.1.2. Реакции электрофильного присоединения Галогенирование
- •Гидрогалогенирование
- •Гидратация
- •5.3.1.3. Нуклеофильное присоединение
- •5.3.2. Кислотность алкинов
- •Константы кислотности некоторых соединений
- •5.3.3. Взаимодействие алкинов с карбонильными соединениями
- •5.3.4. Окисление алкинов
- •5.3.5. Радикальное присоединение бромоводорода
- •5.4. Способы получения
- •6. Диены
- •6.1. Устойчивость сопряженных диенов
- •Теплоты гидрирования алкенов и диенов
- •Гибридизация атомов углерода и длины простых углерод-углеродных связей
- •6.2. Химические свойства
- •6.2.1. Электрофильное присоединение
- •6.2.3. Диеновый синтез. Реакция Дильса-Альдера
- •6.2.4. Полимеризация
- •6.3. Способы получения
- •7. Арены
- •7.1. Сравнение свойств бензола со свойствами алкенов
- •Сравнение химических свойств циклогексена и бензола
- •7.2. Теплота гидрирования. Энергия резонанса
- •7.3. Строение бензола
- •7.4. Ароматичность
- •7.5. Физические свойства
- •Физические свойства аренов
- •7.6. Химические свойства
- •7.6.1. Электрофильное замещение
- •7.6.1.1. Нитрование
- •Превращения -комплекса
- •1.6.1.2. Галогенирование
- •7.6.1.3. Сульфирование
- •7.6.1.3. Алкилирование по Фриделю-Крафтсу
- •7.6.1.4. Ацилирование
- •7.6.1.5. Хлорметилирование
- •7.6.1.6. Формилирование
- •7.6.2. Свободнорадикальное замещение в боковой цепи аренов
- •7.6.3. Реакции окисления
- •7.7. Методы синтеза
- •8. Электрофильное замещение в производных
- •8.1. Влияние заместителей на реакционную способность
- •8.2. Механизм ориентации - влияние заместителей на выбор
- •Классификация заместителей. Электронные эффекты
- •9. Многоядерные ароматические соединения
- •9.1. Нафталин
- •9.1.1. Строение нафталина
- •9.1.2. Химические свойства
- •9.1.2.1. Реакции электрофильного замещения
- •9.1.2.2. Ориентация в реакциях электрофильного замещения
- •9.1.2.3. Восстановление и окисление нафталина
- •9.2. Антрацен и фенантрен
- •10. Гетероциклические соединения
- •10.1. Пятичленные гетероциклы
- •10.1.1. Строение
- •10.1.2. Химические свойства
- •10.1.3. Способы получения
- •10.2. Пиридин
- •10.2.1. Строение пиридина
- •10.2.2. Химические свойства
- •10.3. Хинолин
- •11. Галогеналканы
- •11.1. Нуклеофильное замещение
- •Реакции нуклеофильного замещения
- •11.1.1. Бимолекулярное нуклеофильное замещение
- •Бимолекулярного нуклеофильного замещения, sn2 - процесс согласованный одностадийный:
- •11.1.2. Мономолекулярное нуклеофильное замещение
- •Мономолекулярного нуклеофильного замещения. Sn1-двухстадийный процесс
- •Мономолекулярного нуклеофильного замещения
- •11.1.3. Сравнение реакций sn 1 и sn 2
- •Влияние условий реакции на относительное значение двух механизмов
- •11.1.4. Амбидентные ионы
- •11.2. Реакции отщепления (элиминирование)
- •11.2.1. Бимолекулярное отщепление е2
- •Состав продуктов е2-реакции 2-замещенных пентанов (под действием c2h5oөk)
- •Состав продуктов реакции трет-пентилбромида с алкоголятами калия roөk (70-75о с)
- •5.2.2. Мономолекулярное отщепление е1
- •11.2.3. Сравнение реакций нуклеофильного замещения и элиминирования
- •11.3. Методы синтеза галогеналканов
- •12.2. Нуклеофильное замещение, протекающее через стадию образования дегидробензола. Отщепление – присоединение
- •12.3. Бимолекулярное нуклеофильное замещение путем
- •12.4. Ориентация при нуклеофильном замещении
- •13. Магнийорганические соединения
- •13.1. Получение и строение магнийорганических соединений
- •13.2. Синтез спиртов и кислот
- •Оглавление
- •Углеводороды.
11.3. Методы синтеза галогеналканов
11.3.1. Галогенирование алканов
11.3.2. Присоединение галогеноводородов к олефинам
11.3.3. Замещение гидроксильной группы спиртов на галоген
Реакция проводится действием на спирты галогенводородов
![]()
![]()
или галогенидов фосфора
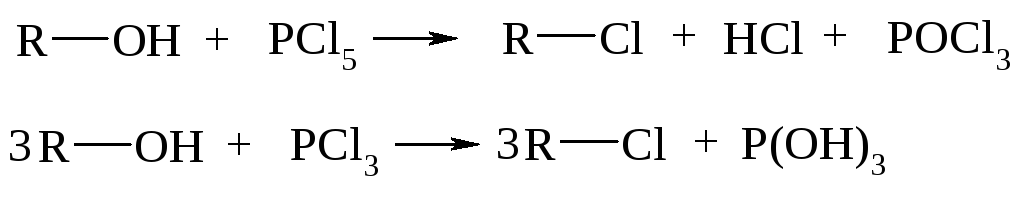
или хлористым тионилом
![]()
12. Галогенарены
Галогенаренами называются соединения, содержащие атом галогена, связанный непосредственно с ароматическим кольцом.
12.1. Причина низкой реакционной способности галогенаренов
Галогенарены нереакционноспособны в реакциях нуклеофильного замещения, которые характерны для галогеналканов. Низкая реакционная способность галогенаренов обусловлена двумя факторами: 1) делокализацией электронов вследствие резонанса и 2) более высокой энергией -связи.
1). Хлорбензол можно представить как гибрид граничных структур I-V, причем в структурах III, IV и V хлор связан с атомом углерода двойной связью.
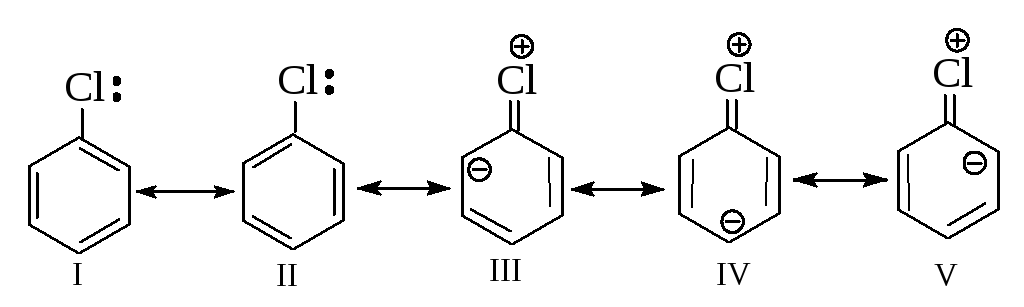
Вклад структур III, IV и V показывает, что углерод и хлор связаны более чем одной парой электронов, следовательно, связь углерод - хлор является не простой, а кратной.
2). В галогеналканах углерод, соединенный с галогеном, находится в sp3-гибридном состоянии. В галогенаренах атом углерода, связанный с галогеном, находится в sp2-cостоянии, поэтому связь углерод-галоген в галогенаренах короче и прочнее, чем в галогеналканах.
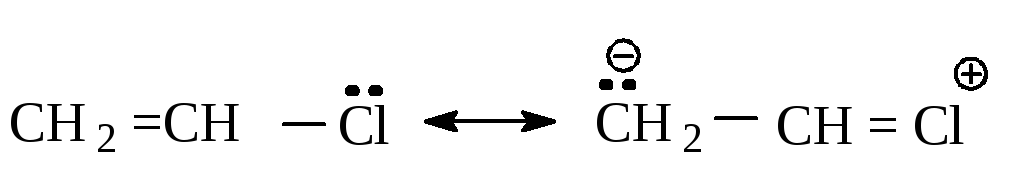
Подобным же образом можно объяснить низкую реакционную способность винилгалогенидов CH2 = CH-X.
12.2. Нуклеофильное замещение, протекающее через стадию образования дегидробензола. Отщепление – присоединение
Нуклеофильное замещение галогена в галогенаренах происходит в жестких условиях. Если хлорбензол ввести в реакцию с очень сильным основанием NH2 в жидком аммиаке, то он превращается в анилин.
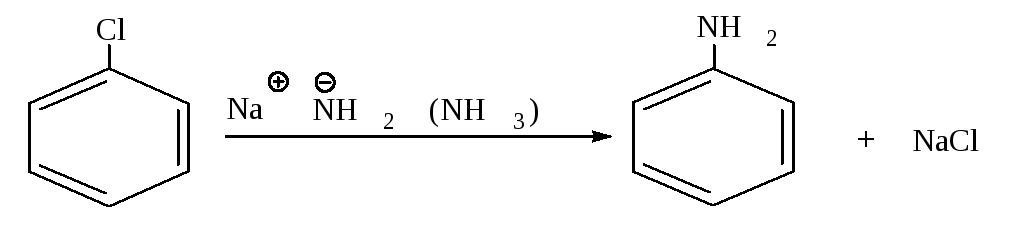
Реакция протекает в две стадии.
Первая стадия - отщепление хлороводорода с образованием дегидробензола.
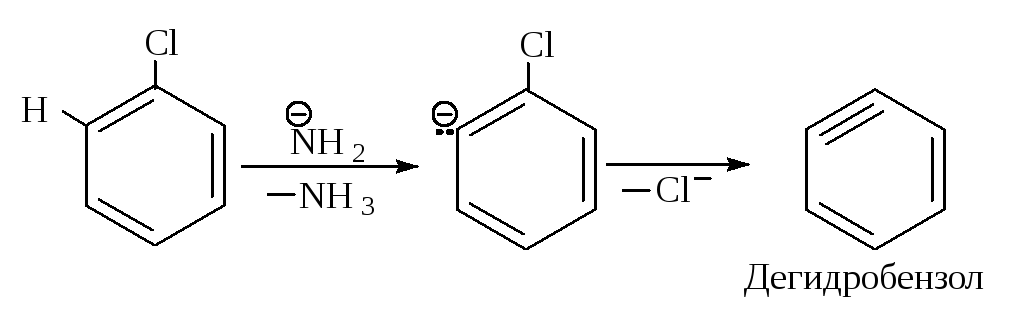
В дегидробензоле дополнительная связь образована между атомами углерода за счет бокового перекрывания sp2-орбиталей, эта связь мало взаимодействует с -электронным облаком кольца.
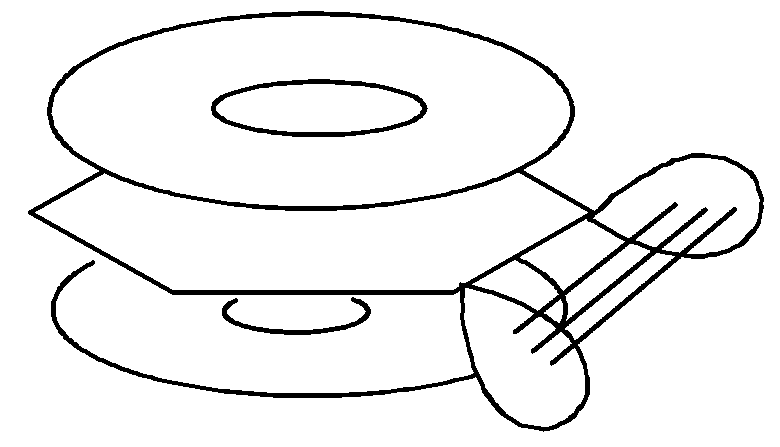
Новая связь довольно слабая и дегидробензол очень реакционноспособен.
Вторая стадия - присоединение аммиака к дегидробензолу.
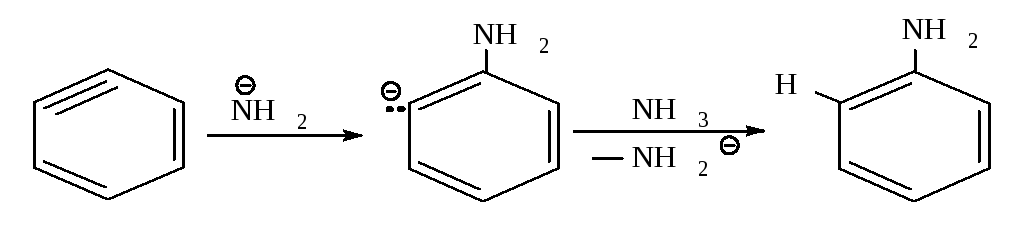
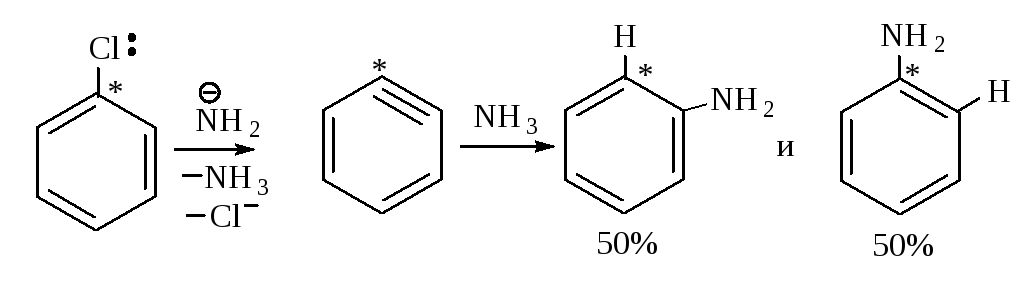
Подтверждением указанного механизма служит следующий факт: хлорбензол с меченым атомом углерода 14С (обозначенным С*) в реакции с амидом натрия превращается в анилин, в котором половина молекул содержит аминогруппу при углероде 14С, а половина - при соседнем углероде.
12.3. Бимолекулярное нуклеофильное замещение путем
присоединения - отщепления
Присутствие электроноакцепторных групп (например нитрогруппы), особенно в орто- или пара-положении к хлору резко увеличивает его подвижность.
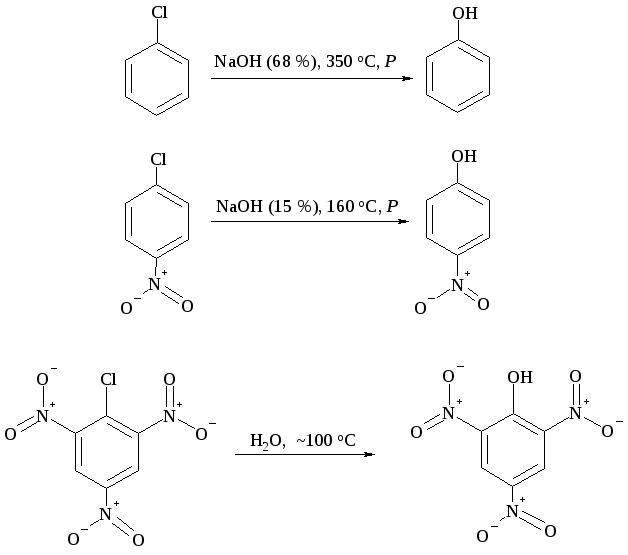
Другие электроноакцепторные группы, расположенные в орто-, пара-положениях, подобно нитрогруппе, активируют галоген. Наоборот, электронодонорные группы будут дезактивировать ароматическое кольцо в реакциях нуклеофильного замещения.
Бимолекулярное нуклеофильное замещение в ароматическом ядре включает две стадии.
Первая стадия - медленная: атака нуклеофильного реагента по атому углерода, связанному с галогеном, и образование -комплекса - карбаниона.
В карбанионе шесть -электронов делокализованы на р-орбиталях пяти атомов углерода, находящихся в sp2-гибридном состоянии; избыточная электронная плотность распределена между углеродами в орто-, пара-положениях кольца (I, II и III структуры) и кислородом нитрогуппы (IV).
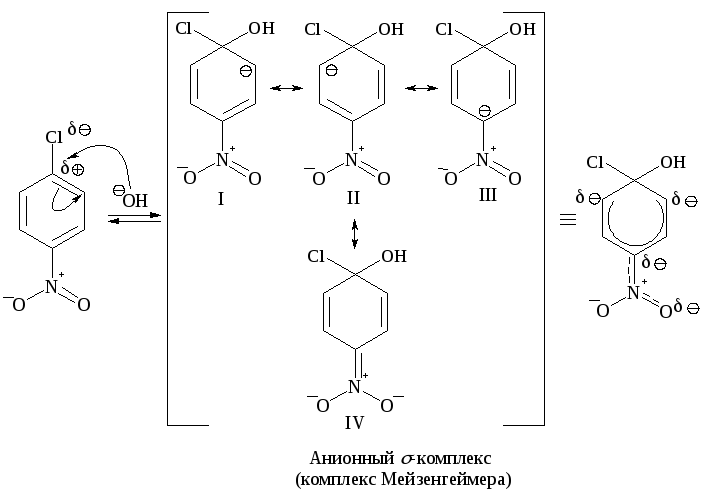
Вторая стадия - быстрая: отщепление аниона галогена, восстановление ароматического шести--электронного секстета.
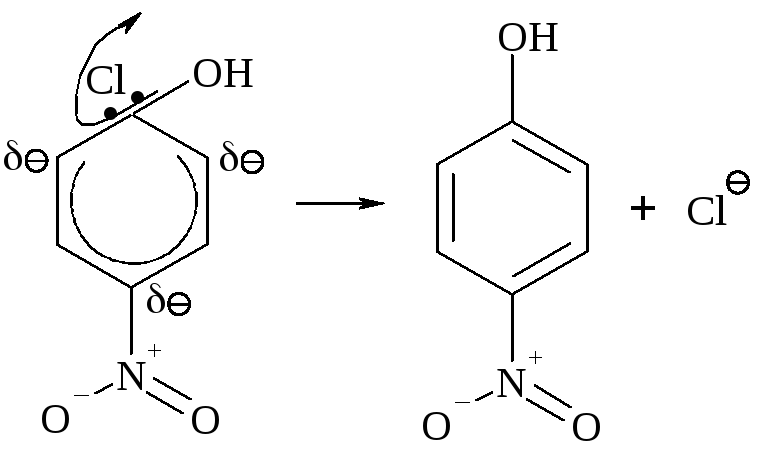
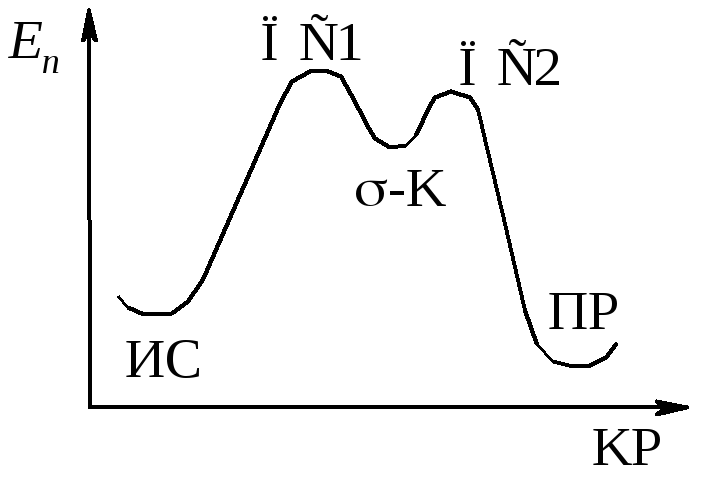
Рис. 12.1. Энергетическая диаграмма реакции SNAr
Реакция нуклеофильного замещения в ароматическом ядре протекает через две стадии: 1) нуклеофильного присоединения и 2) последующего отщепления аниона галогена подобно тому, как электрофильное замещение протекает через стадии: 1) электрофильного присоединения и 2) последующего отщепления протона (рис. 12.1).
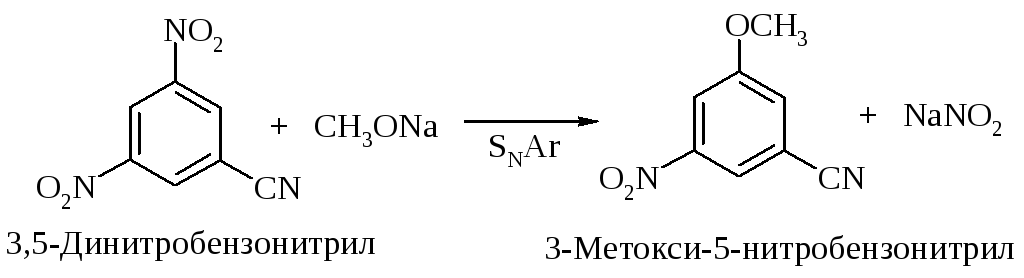
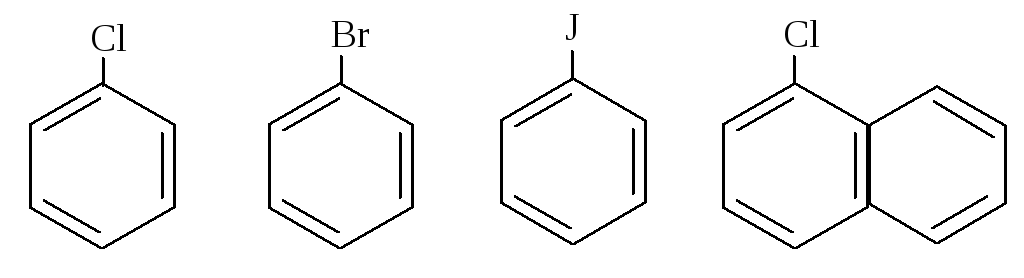
В реакциях SN2Ar наиболее реакционноспособными являются фторзамещенные арены. Например, относительная реакционная способность п-галогеннитробензолов по отношению к метоксиду натрия при 50 оС изменяется в следующем порядке: F (312) >> Cl (1) > Br (0,74) > I (0,36).
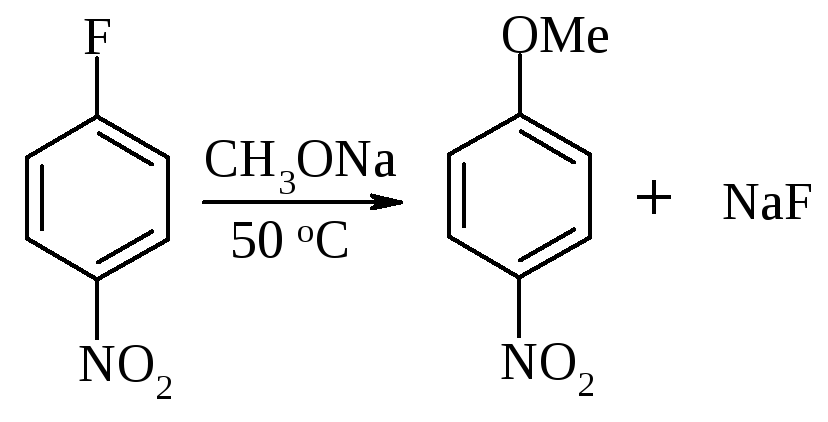
При нуклеофильном ароматическом замещении прочность связи С–Hal не играет решающей роли, поскольку разрыв связи происходит не на стадии, определяющей скорость замещения. Сильно электроотрицательный фтор стабилизирует переходное состояние скорость определяющей реакции присоединения более эффективно, чем другие галогены, и поэтому ускоряет реакцию.
Другие электроноакцепторные группы, такие как циано –CN, ацетил –COCH3, трифторметильная –CF3, также повышают реакционную способность кольца, но в меньшей степени.
В реакциях нуклеофильного ароматического замещения распространенными уходящими группами являются галогены, нитрогруппа –NO2, тозилатная –O–SO2–C6H4–CH3-п, алкилсульфонильная –SO2–R, сульфогруппа –SO3H.