
- •И.С. Колпащикова, е.Р. Кофанов, е.М. Алов углеводороды. Галогенпроизводные углеводородов
- •1. Алканы
- •1.1. Гомологический ряд, изомеры
- •Гомологический ряд алканов. Число структурных изомеров
- •1.2. Строение метана
- •1.3. Строение этана
- •1.4. Вращение вокруг простой углерод-углеродной связи. Конформации
- •1.5. Физические свойства
- •1.6. Химические свойства
- •1.6.1. Хлорирование и бромирование метана. Механизм реакции
- •1.6.2. Строение метильного радикала
- •1.6.3. Расчет изменения энергии в ходе реакции
- •1.6.4. Энергетическая диаграмма реакции. Связь энергии
- •Хлорирования метана
- •Бромирования метана
- •1.6.5. Причина различной реакционной способности галогенов
- •Зависимость реакционной способности галогенов от энергии связи h–Hal
- •1.6.6. Галогенирование высших алканов. Механизм
- •1.6.7. Медленная стадия. Энергетическая диаграмма
- •1.6.8. Причина различной устойчивости радикалов
- •1.6.9. Зависимость скорости образования радикалов
- •1.6.10. Расчет реакционной способности различных связей
- •1.6.11. Селективность в реакциях хлорирования
- •Малореакционного Br• с пропаном
- •1.6.12. Нитрование
- •1.6.13. Сульфоокисление и сульфохлорирование
- •1.6.14. Окисление
- •1.6.15. Термическое разложение алканов, крекинг
- •1.6.16. Ионные реакции алканов
- •1.7. Методы синтеза алканов
- •1.7.1. Гидрирование алкенов и алкинов
- •1.7.2. Реакция Вюрца
- •1.7.3. Гидрирование галогеналканов
- •2.2. Плоскополяризованный свет. Оптическая активность
- •2.3. Строение молекул и оптическая активность
- •2.4. Обозначение конфигураций
- •2.5. Соединения с несколькими хиральными центрами.
- •2.6. Методы разделения энантиомеров
- •3. Циклоалканы
- •3.1 Номенклатура. Изомерия
- •3.2. Физические свойства
- •3.3. Строение
- •Теплоты сгорания и энергии напряжения циклоалканов
- •3.4. Химические свойства
- •3.5. Способы получения
- •4.2. Строение этена
- •4.3. Физические свойства
- •Физические свойства алкенов
- •4.4. Химические свойства
- •4.4.1. Гидрирование. Теплота гидрирования
- •4.4.2. Теплота гидрирования и устойчивость алкенов
- •4.4.3. Присоединение галогенов
- •4.4.3.1. Механизм реакции
- •4.4.3.2. Реакционная способность галогенов в реакции АdЕ
- •4.4.4. Присоединение галогеноводородов
- •4.4.4.1. Механизм реакции
- •4.4.4.2. Направление электрофильного присоединения
- •К пропену
- •4.4.4.3. Реакционная способность и селективность
- •4.4.4.4. Перегруппировка
- •Механизм реакции
- •4.4.5. Присоединение бромистого водорода в присутствии
- •1. Инициирование:
- •2. Рост цепи:
- •3. Обрыв цепи:
- •4.4.6. Присоединение серной кислоты
- •4.4.7. Гидратация алкенов. Присоединение спиртов
- •4.4.8. Гидроборирование алкенов
- •4.4.9. Алкилирование алкенов
- •4.4.10. Полимеризация алкенов
- •4.4.11. Окисление
- •4.4.12. Реакция аллильного замещения. Галогенирование
- •4.5. Способы получения алкенов
- •Характеристики химических связей в молекуле алкинов
- •Характеристики связей с-н в алканах, алкенах и алкинах
- •5.2. Физические свойства
- •5.3. Химические свойства
- •5.3.1. Реакции присоединеня
- •5.3.1.1. Каталитическое гидрирование и восстановление
- •5.3.1.2. Реакции электрофильного присоединения Галогенирование
- •Гидрогалогенирование
- •Гидратация
- •5.3.1.3. Нуклеофильное присоединение
- •5.3.2. Кислотность алкинов
- •Константы кислотности некоторых соединений
- •5.3.3. Взаимодействие алкинов с карбонильными соединениями
- •5.3.4. Окисление алкинов
- •5.3.5. Радикальное присоединение бромоводорода
- •5.4. Способы получения
- •6. Диены
- •6.1. Устойчивость сопряженных диенов
- •Теплоты гидрирования алкенов и диенов
- •Гибридизация атомов углерода и длины простых углерод-углеродных связей
- •6.2. Химические свойства
- •6.2.1. Электрофильное присоединение
- •6.2.3. Диеновый синтез. Реакция Дильса-Альдера
- •6.2.4. Полимеризация
- •6.3. Способы получения
- •7. Арены
- •7.1. Сравнение свойств бензола со свойствами алкенов
- •Сравнение химических свойств циклогексена и бензола
- •7.2. Теплота гидрирования. Энергия резонанса
- •7.3. Строение бензола
- •7.4. Ароматичность
- •7.5. Физические свойства
- •Физические свойства аренов
- •7.6. Химические свойства
- •7.6.1. Электрофильное замещение
- •7.6.1.1. Нитрование
- •Превращения -комплекса
- •1.6.1.2. Галогенирование
- •7.6.1.3. Сульфирование
- •7.6.1.3. Алкилирование по Фриделю-Крафтсу
- •7.6.1.4. Ацилирование
- •7.6.1.5. Хлорметилирование
- •7.6.1.6. Формилирование
- •7.6.2. Свободнорадикальное замещение в боковой цепи аренов
- •7.6.3. Реакции окисления
- •7.7. Методы синтеза
- •8. Электрофильное замещение в производных
- •8.1. Влияние заместителей на реакционную способность
- •8.2. Механизм ориентации - влияние заместителей на выбор
- •Классификация заместителей. Электронные эффекты
- •9. Многоядерные ароматические соединения
- •9.1. Нафталин
- •9.1.1. Строение нафталина
- •9.1.2. Химические свойства
- •9.1.2.1. Реакции электрофильного замещения
- •9.1.2.2. Ориентация в реакциях электрофильного замещения
- •9.1.2.3. Восстановление и окисление нафталина
- •9.2. Антрацен и фенантрен
- •10. Гетероциклические соединения
- •10.1. Пятичленные гетероциклы
- •10.1.1. Строение
- •10.1.2. Химические свойства
- •10.1.3. Способы получения
- •10.2. Пиридин
- •10.2.1. Строение пиридина
- •10.2.2. Химические свойства
- •10.3. Хинолин
- •11. Галогеналканы
- •11.1. Нуклеофильное замещение
- •Реакции нуклеофильного замещения
- •11.1.1. Бимолекулярное нуклеофильное замещение
- •Бимолекулярного нуклеофильного замещения, sn2 - процесс согласованный одностадийный:
- •11.1.2. Мономолекулярное нуклеофильное замещение
- •Мономолекулярного нуклеофильного замещения. Sn1-двухстадийный процесс
- •Мономолекулярного нуклеофильного замещения
- •11.1.3. Сравнение реакций sn 1 и sn 2
- •Влияние условий реакции на относительное значение двух механизмов
- •11.1.4. Амбидентные ионы
- •11.2. Реакции отщепления (элиминирование)
- •11.2.1. Бимолекулярное отщепление е2
- •Состав продуктов е2-реакции 2-замещенных пентанов (под действием c2h5oөk)
- •Состав продуктов реакции трет-пентилбромида с алкоголятами калия roөk (70-75о с)
- •5.2.2. Мономолекулярное отщепление е1
- •11.2.3. Сравнение реакций нуклеофильного замещения и элиминирования
- •11.3. Методы синтеза галогеналканов
- •12.2. Нуклеофильное замещение, протекающее через стадию образования дегидробензола. Отщепление – присоединение
- •12.3. Бимолекулярное нуклеофильное замещение путем
- •12.4. Ориентация при нуклеофильном замещении
- •13. Магнийорганические соединения
- •13.1. Получение и строение магнийорганических соединений
- •13.2. Синтез спиртов и кислот
- •Оглавление
- •Углеводороды.
8.2. Механизм ориентации - влияние заместителей на выбор
места электрофильной атаки
Электронодонорные группы активируют все положения кольца, т.е. орто-, пара- и мета-положения становятся более реакционноспособными, чем любое положение в бензоле. Однако они активируют орто- и пара-положения сильнее, чем мета-положение.
Электроноакцепторные группы (кроме галогенов) дезактивируют все положения кольца, но особенно сильно - орто- и пара-положения.
Галогены составляют особую группу ориентантов, которая будет рассмотрена отдельно.

Следовательно, любая группа: - и активирующая, и дезактивирующая - самое сильное влияние оказывает на орто- и пара-положения. Это обусловлено тем, что именно в орто- и пара-положениях по отношению к углероду, присоединившему электрофил, возникает положительный заряд.
Поскольку медленной стадией реакции электрофильного замещения является стадия образования о-, м-, п--комплексов (карбокатионов), соотношение, в котором они образуются в этой медленной стадии, определяет количества о-, м-, п-изомерных продуктов реакции. Известно, что чем больше распределён заряд в карбокатионе, тем он устойчивее и тем быстрее образуется. Следовательно, главное направление реакции электрофильного замещения осуществляется через образование наиболее устойчивых карбокатионов (-комплексов).
Рассмотрим влияние электронодонорных групп на устойчивость образующихся в медленной стадии карбокатионов.
1). Влияние группы СН3–, проявляющей электронодонорный индукционный эффект.

Группа -СН3 подает электроны ко всем атомам кольца (+I - эффект), но наибольшее влияние она оказывает на тот атом, с которым непосредственно связана. Среди граничных структур I-III, изображающих орто--комплекс, есть структура I, в которой метильная группа подает электроны на углеродный атом, несущий положительный заряд, и за счёт этого в ней в большей степени, чем в II и III, распределяется положительный заряд. Структура I более устойчива, вклад её в резонансный гибрид наибольший. Аналогичен вклад структуры IV в пара--комплекс.
В мета--комплексе группа -СН3 не проявляет в такой же степени способность стабилизировать его: ни в одной из граничных структур VII-IX она не связана с положительно заряженным углеродным атомом.
Следовательно, из трех активированных комплексов наиболее устойчивыми являются о-, п--комплексы, в которых положительный заряд находится на атоме, несущем группу -CH3. Это значит, что энергии активации образования о-, п--комплексов ниже, чем энергия активации образования м--комплекса, продукты о-, п-замещения образуются в большем количестве, чем м-продукт.

2). Несколько другой тип стабилизации -комплекса характерен для групп, содержащих гетероатом атом с неподеленной электронной парой: -ОН, -ОR, -NН2, имеющих неподеленные электроны (р--сопряжение) и -CH=CH2; -С6Н5, содержащих -электроны (--сопряжение). Группы -ОН, -ОR, -NН2, -NНR, -NR2 проявляют электроноакцепторный индукционный эффект. Это означает, что атомы азота и кислорода, соединённые с углеродом ароматического кольца, оттягивают на себя электроны -связи вследствие большей электроотрицательности азота и кислорода по сравнению с углеродом. Однако эффект р--сопряжения этих групп преобладает над электроноакцепторным индукционным эффектом.
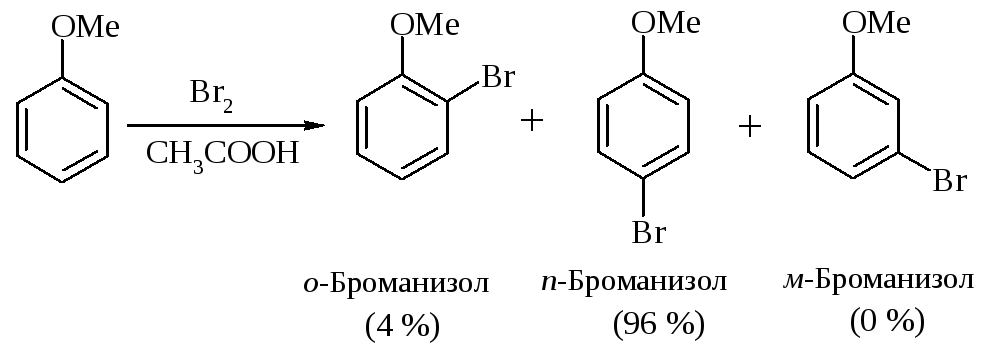
Рассмотрим строение -комплексов, образующихся при электрофильном замещении в анизоле.

-Комплекс, образующийся при атаке в орто-положение, представляет собой резонансный гибрид структур I-III, в которых положительный заряд распределен между атомами углерода, а также структуры IV, в которой положительный заряд находится на атоме кислорода. Структура IV особенно устойчива, поскольку каждый атом имеет завершённую электронную оболочку. Подобная картина возникает и при атаке в пара-положение.
Но в случае мета-атаки структура, подобная IV или VIII, в изображении -комплекса отсутствует. Следовательно, орто- и пара--комплексы более устойчивы, а значит, замещение идёт преимущественно в пара- и орто-положения.
Теперь сравним устойчивость -комплексов, образующихся при атаке в орто-, мета- и пара-положения бензольного кольца, содержащего электроноакцепторную группу.

-Комплексы, образующиеся при атаке в орто- пара- и мета-положения, менее устойчивы и образуются медленнее, чем карбокатион, возникающий при взаимодействии электрофила с бензолом. Это означает, что электроноакцепторные группы дезактивируют бензол в реакциях электрофильного замещения.
Сравнение граничных структур I-III, IV-VI и VII-IX приводит нас к выводу: из трёх -комплексов наименее устойчивы орто- и пара--комплексы, так как в структурах I и IV положительные заряды расположены на соседних атомах, вклад этих структур можно не учитывать, заряд в орто- и пара--комплексах распределён в меньшей степени, чем в мета--комплексе. Следовательно, замещение в орто- и пара-положения идёт медленнее, чем в мета-, и основным продуктом является мета-замещённое соединение.

Рассмотрение механизма ориентации показывает, что все электроноакцепторные (кроме галогенов) группы являются дезактивирующими мета-ориентантами, а все электронодонорные группы - активирующими орто-, пара-ориентантами (табл. 8.1).
Почему галогены ведут себя необычным образом? Благодаря резонансному эффекту (эффекту сопряжения) галогены являются орто-, пара-ориентантами.

Резонанс такого типа требует перекрывания 2р-орбиталей атома углерода с 3р-орбиталями атома хлора. Так как в сопряжение вовлекаются электроны различных квантовых уровней, это сопряжение не будет так эффективно, как сопряжение электронов углерода и азота, углерода и кислорода.
Таблица 8.1
