
- •И.С. Колпащикова, е.Р. Кофанов, е.М. Алов углеводороды. Галогенпроизводные углеводородов
- •1. Алканы
- •1.1. Гомологический ряд, изомеры
- •Гомологический ряд алканов. Число структурных изомеров
- •1.2. Строение метана
- •1.3. Строение этана
- •1.4. Вращение вокруг простой углерод-углеродной связи. Конформации
- •1.5. Физические свойства
- •1.6. Химические свойства
- •1.6.1. Хлорирование и бромирование метана. Механизм реакции
- •1.6.2. Строение метильного радикала
- •1.6.3. Расчет изменения энергии в ходе реакции
- •1.6.4. Энергетическая диаграмма реакции. Связь энергии
- •Хлорирования метана
- •Бромирования метана
- •1.6.5. Причина различной реакционной способности галогенов
- •Зависимость реакционной способности галогенов от энергии связи h–Hal
- •1.6.6. Галогенирование высших алканов. Механизм
- •1.6.7. Медленная стадия. Энергетическая диаграмма
- •1.6.8. Причина различной устойчивости радикалов
- •1.6.9. Зависимость скорости образования радикалов
- •1.6.10. Расчет реакционной способности различных связей
- •1.6.11. Селективность в реакциях хлорирования
- •Малореакционного Br• с пропаном
- •1.6.12. Нитрование
- •1.6.13. Сульфоокисление и сульфохлорирование
- •1.6.14. Окисление
- •1.6.15. Термическое разложение алканов, крекинг
- •1.6.16. Ионные реакции алканов
- •1.7. Методы синтеза алканов
- •1.7.1. Гидрирование алкенов и алкинов
- •1.7.2. Реакция Вюрца
- •1.7.3. Гидрирование галогеналканов
- •2.2. Плоскополяризованный свет. Оптическая активность
- •2.3. Строение молекул и оптическая активность
- •2.4. Обозначение конфигураций
- •2.5. Соединения с несколькими хиральными центрами.
- •2.6. Методы разделения энантиомеров
- •3. Циклоалканы
- •3.1 Номенклатура. Изомерия
- •3.2. Физические свойства
- •3.3. Строение
- •Теплоты сгорания и энергии напряжения циклоалканов
- •3.4. Химические свойства
- •3.5. Способы получения
- •4.2. Строение этена
- •4.3. Физические свойства
- •Физические свойства алкенов
- •4.4. Химические свойства
- •4.4.1. Гидрирование. Теплота гидрирования
- •4.4.2. Теплота гидрирования и устойчивость алкенов
- •4.4.3. Присоединение галогенов
- •4.4.3.1. Механизм реакции
- •4.4.3.2. Реакционная способность галогенов в реакции АdЕ
- •4.4.4. Присоединение галогеноводородов
- •4.4.4.1. Механизм реакции
- •4.4.4.2. Направление электрофильного присоединения
- •К пропену
- •4.4.4.3. Реакционная способность и селективность
- •4.4.4.4. Перегруппировка
- •Механизм реакции
- •4.4.5. Присоединение бромистого водорода в присутствии
- •1. Инициирование:
- •2. Рост цепи:
- •3. Обрыв цепи:
- •4.4.6. Присоединение серной кислоты
- •4.4.7. Гидратация алкенов. Присоединение спиртов
- •4.4.8. Гидроборирование алкенов
- •4.4.9. Алкилирование алкенов
- •4.4.10. Полимеризация алкенов
- •4.4.11. Окисление
- •4.4.12. Реакция аллильного замещения. Галогенирование
- •4.5. Способы получения алкенов
- •Характеристики химических связей в молекуле алкинов
- •Характеристики связей с-н в алканах, алкенах и алкинах
- •5.2. Физические свойства
- •5.3. Химические свойства
- •5.3.1. Реакции присоединеня
- •5.3.1.1. Каталитическое гидрирование и восстановление
- •5.3.1.2. Реакции электрофильного присоединения Галогенирование
- •Гидрогалогенирование
- •Гидратация
- •5.3.1.3. Нуклеофильное присоединение
- •5.3.2. Кислотность алкинов
- •Константы кислотности некоторых соединений
- •5.3.3. Взаимодействие алкинов с карбонильными соединениями
- •5.3.4. Окисление алкинов
- •5.3.5. Радикальное присоединение бромоводорода
- •5.4. Способы получения
- •6. Диены
- •6.1. Устойчивость сопряженных диенов
- •Теплоты гидрирования алкенов и диенов
- •Гибридизация атомов углерода и длины простых углерод-углеродных связей
- •6.2. Химические свойства
- •6.2.1. Электрофильное присоединение
- •6.2.3. Диеновый синтез. Реакция Дильса-Альдера
- •6.2.4. Полимеризация
- •6.3. Способы получения
- •7. Арены
- •7.1. Сравнение свойств бензола со свойствами алкенов
- •Сравнение химических свойств циклогексена и бензола
- •7.2. Теплота гидрирования. Энергия резонанса
- •7.3. Строение бензола
- •7.4. Ароматичность
- •7.5. Физические свойства
- •Физические свойства аренов
- •7.6. Химические свойства
- •7.6.1. Электрофильное замещение
- •7.6.1.1. Нитрование
- •Превращения -комплекса
- •1.6.1.2. Галогенирование
- •7.6.1.3. Сульфирование
- •7.6.1.3. Алкилирование по Фриделю-Крафтсу
- •7.6.1.4. Ацилирование
- •7.6.1.5. Хлорметилирование
- •7.6.1.6. Формилирование
- •7.6.2. Свободнорадикальное замещение в боковой цепи аренов
- •7.6.3. Реакции окисления
- •7.7. Методы синтеза
- •8. Электрофильное замещение в производных
- •8.1. Влияние заместителей на реакционную способность
- •8.2. Механизм ориентации - влияние заместителей на выбор
- •Классификация заместителей. Электронные эффекты
- •9. Многоядерные ароматические соединения
- •9.1. Нафталин
- •9.1.1. Строение нафталина
- •9.1.2. Химические свойства
- •9.1.2.1. Реакции электрофильного замещения
- •9.1.2.2. Ориентация в реакциях электрофильного замещения
- •9.1.2.3. Восстановление и окисление нафталина
- •9.2. Антрацен и фенантрен
- •10. Гетероциклические соединения
- •10.1. Пятичленные гетероциклы
- •10.1.1. Строение
- •10.1.2. Химические свойства
- •10.1.3. Способы получения
- •10.2. Пиридин
- •10.2.1. Строение пиридина
- •10.2.2. Химические свойства
- •10.3. Хинолин
- •11. Галогеналканы
- •11.1. Нуклеофильное замещение
- •Реакции нуклеофильного замещения
- •11.1.1. Бимолекулярное нуклеофильное замещение
- •Бимолекулярного нуклеофильного замещения, sn2 - процесс согласованный одностадийный:
- •11.1.2. Мономолекулярное нуклеофильное замещение
- •Мономолекулярного нуклеофильного замещения. Sn1-двухстадийный процесс
- •Мономолекулярного нуклеофильного замещения
- •11.1.3. Сравнение реакций sn 1 и sn 2
- •Влияние условий реакции на относительное значение двух механизмов
- •11.1.4. Амбидентные ионы
- •11.2. Реакции отщепления (элиминирование)
- •11.2.1. Бимолекулярное отщепление е2
- •Состав продуктов е2-реакции 2-замещенных пентанов (под действием c2h5oөk)
- •Состав продуктов реакции трет-пентилбромида с алкоголятами калия roөk (70-75о с)
- •5.2.2. Мономолекулярное отщепление е1
- •11.2.3. Сравнение реакций нуклеофильного замещения и элиминирования
- •11.3. Методы синтеза галогеналканов
- •12.2. Нуклеофильное замещение, протекающее через стадию образования дегидробензола. Отщепление – присоединение
- •12.3. Бимолекулярное нуклеофильное замещение путем
- •12.4. Ориентация при нуклеофильном замещении
- •13. Магнийорганические соединения
- •13.1. Получение и строение магнийорганических соединений
- •13.2. Синтез спиртов и кислот
- •Оглавление
- •Углеводороды.
4.4.4.2. Направление электрофильного присоединения
Пропен, присоединяя галогеноводород, может дать два продукта: 2-бромпропан и 1-бромпропан.
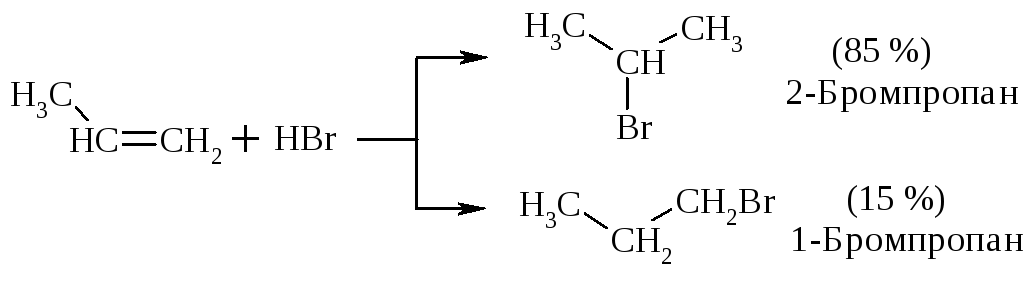
Установлено, что в продуктах реакции значительно преобладает 2-бромпропан. В 1869 г. В. Марковников, изучивший большое число таких присоединений, сформулировал правило:
-
Галогеноводороды, как и другие протонные кислоты, присоединяются к несимметричным алкенам таким образом, что водород присоединяется к атому углерода, несущему наибольшее число атомов водорода.
Рассмотрим двухстадийный механизм присоединения хлороводорода к алкенам: медленная стадия - образование карбокатиона, быстрая стадия - присоединение нуклеофила (ClΘ).
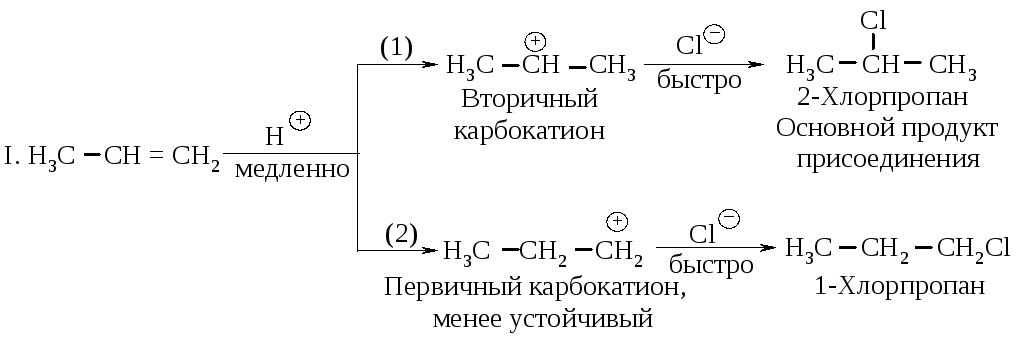
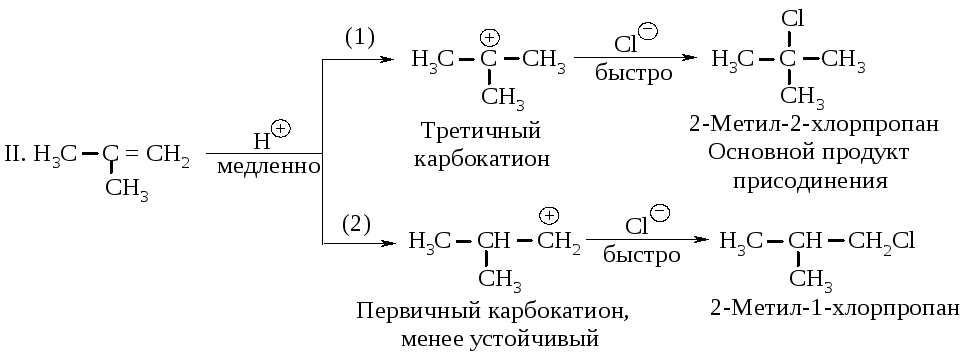
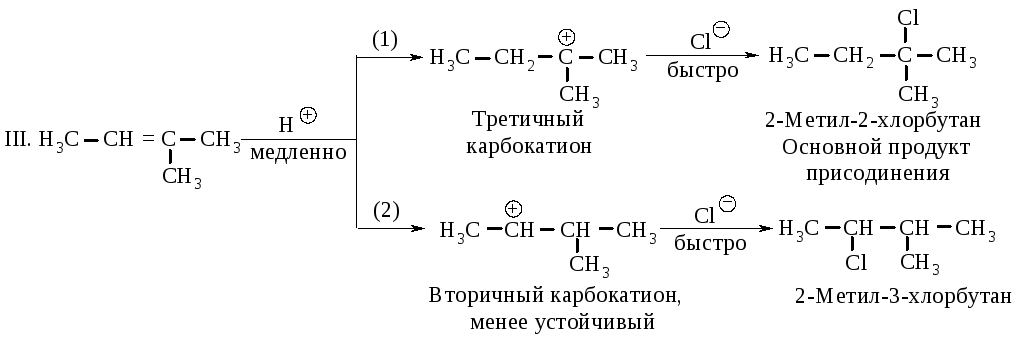
В соответствии с правилом Марковникова в этих реакциях реализуется преимущественно первый путь (1). Направление присоединения определяется относительными скоростями двух конкурирующих реакций медленной стадии - стадии образования карбокатионов.
Состав продуктов реакции показывает, что в первой стадии вторичный карбокатион образуется быстрее, чем первичный по реакции I, а третичный - быстрее, чем первичный и вторичный, как следует из реакций II и III.
-
Легкость образования карбокатионов увеличивается в следующей последовательности: первичный < вторичный < третичный.
С другой стороны, устойчивость карбокатионов возрастает в таком же порядке: первичный < вторичный < третичный. Такой порядок изменения устойчивости можно объяснить следующим образом. Согласно законам физики, устойчивость заряженной системы повышается при распределении заряда. Связь sp3-гибридизованного атома углерода с различными группами (X, Y) в той или иной степени поляризована из-за различной электроотрицательности элементов. Полярность этих связей сравнивается с полярностью связи C–H, выбранной в качестве стандарта. Перераспределение электронной плотности σ-связи под влиянием какой-либо группы по сравнению с распределением электронной плотности связи С–Н называется индукционным (индуктивным) эффектом (I).
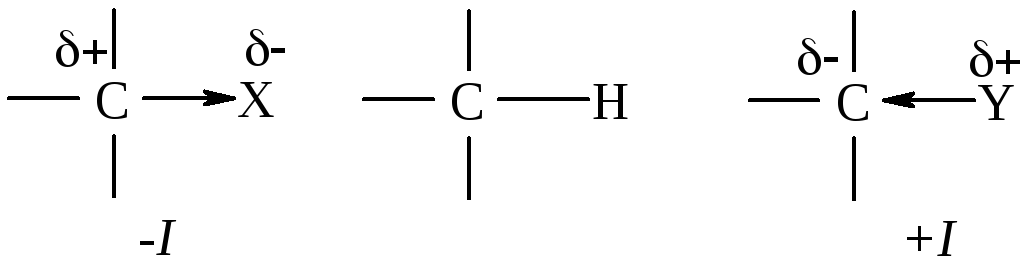
Группа X, которая притягивает пару электронов -связи сильнее, чем атом водорода, проявляет электроноакцепторный эффект (–I). Группа Y, которая отталкивает пару электронов -связи, проявляет электронодонорный эффект (+I).
Под влиянием заряда, образующегося на атоме углерода, поляризуются соседние связи, но этот эффект быстро затухает по цепи связей C–C.
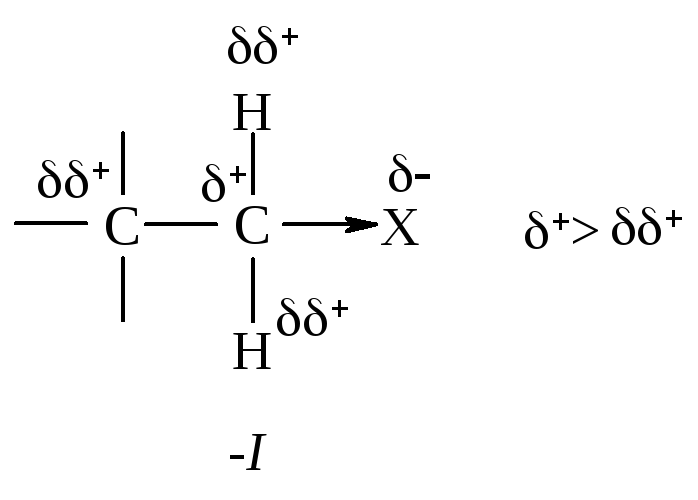
Алкильные группы имеют тенденцию подавать электроны по сравнению с атомом водорода, следовательно, алкильная группа проявляет электронодонорный индукционный эффект (+I). Подавая электроны на положительно заряженный атом углерода, алкильная группа в какой-то степени уменьшает его -заряд, сама при этом приобретает некоторый положительный заряд. В третичном карбокатионе положительный заряд распределен между третичным углеродом и тремя алкильными группами, поэтому третичный карбокатион наиболее устойчив. Наоборот, метильный - наименее устойчив, т.к. в нем заряд локализован на одном атоме углерода.
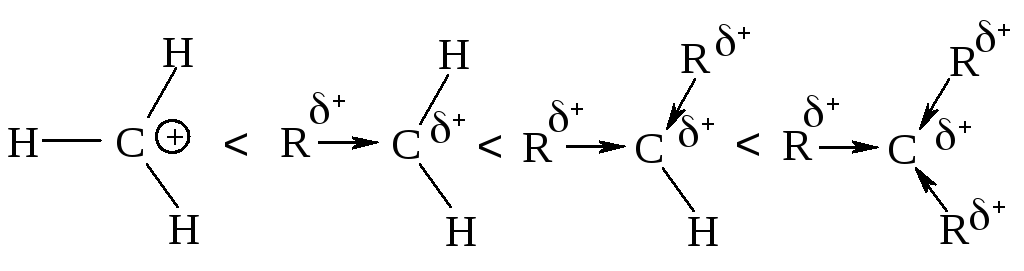
Устойчивость карбокатионов изменяется в таком же порядке, как и легкость, их образования.
-
Чем устойчивее карбокатион, тем легче он образуется.
К такому же выводу приводит нас и сравнение устойчивости переходных состояний, ведущих к образованию карбокатионов в медленной стадии.
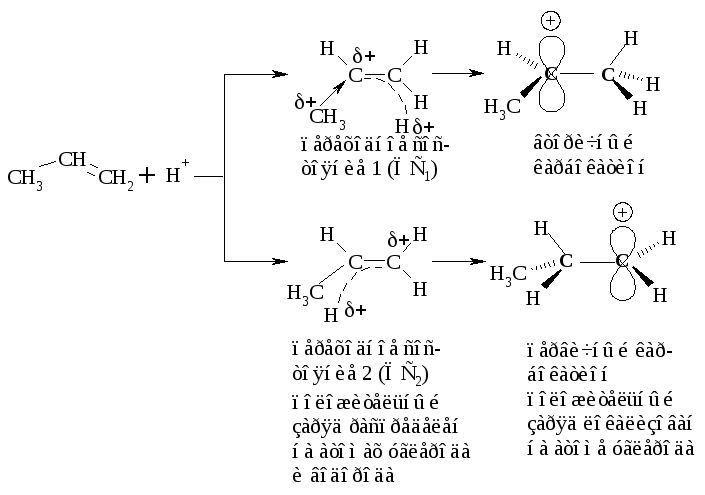
В первом случае (ПС1) электронодонорная группа –СН3 подает электроны и в некоторой степени погашает положительный заряд, образующийся на атоме углерода. Положительный заряд в переходном состоянии ПC1 распределяется в большей степени, чем в переходном состоянии ПС2. Это означает, что ПС1 более устойчиво, энергия активации Еа(1) меньше и реакция его образования протекает быстрее (рис. 4.9).
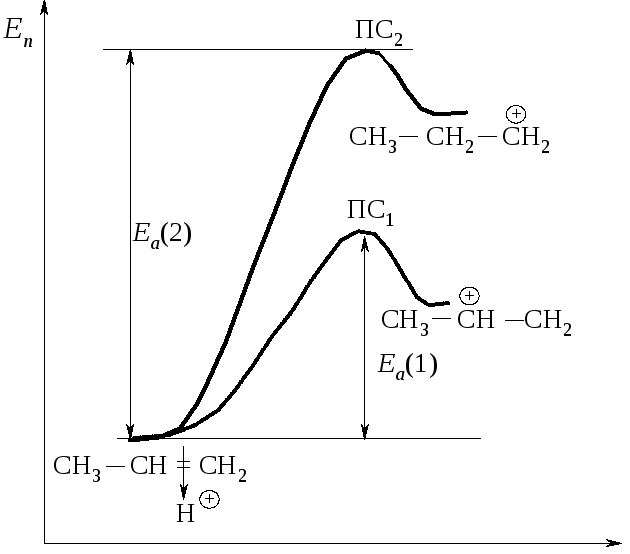
Рис. 4.9. Энергетическая диаграмма присоединения протона
