
- •Московский государственный университет прикладной биотехнологии
- •Лабораторный практикум по физике
- •Введение
- •4Ая страница
- •Раздел I. Термодинамика. Молекулярно-кинетические явления переноса.
- •Определение показателя адиабаты методом клемана-дезорма
- •I.Описание установки.
- •II. Методика работы
- •III. Порядок выполнения работы
- •IV. Обработка результатов измерений
- •V. Вывод:
- •Контрольные вопросы
- •Определение коэффициента вязкости жидкости по методу стокса
- •I. Описание установки. Приборы и принадлежности.
- •II. Методика работы.
- •III. Порядок измерений и таблица результатов.
- •IV. Обработка результатов измерений.
- •V. Вывод:
- •Определение коэффициента вязкости воздуха капиллярным методом (методом Пуазейля)
- •I. Описание установки:
- •II. Методика работы.
- •III. Порядок измерений.
- •IV. Обработка результатов измерений
- •Литература
- •Раздел II. Колебания. Волны.
- •Исследование затухающих и вынужденных колебаний
- •Упражнение 1
- •Порядок выполнения работы
- •Упражнение 2
- •I. Методика работы
- •II. Описание установки.
- •III. Порядок выполнения работы
- •IV. Обработка результатов измерений
- •V. Выводы к упражнению 2:
- •Лабораторная работа № 5 (1-11) определение скорости звука в твердых телах методом кундта
- •I. Описание установки.
- •II. Методика работы.
- •III. Порядок выполнения работы
- •IV. Обработка результатов измерений
- •Контрольные вопросы
- •Литература
- •Вопросы для защиты в форме круглого стола
- •Раздел III. Электростатика. Постоянный ток
- •Лабораторная работа № 6 (2-4) определение емкости конденсатора баллистическим гальванометром
- •Упражнение 1.
- •III. Порядок выполнения работы
- •Упражнение 2.
- •Порядок выполнения работы
- •Контрольные вопросы.
- •Лабораторная работа № 7 (2-1) измерение сопротивлений при помощи моста уитстона
- •Из формулы сопротивления для однородного проводника
- •Или, в зависимости от знака х, наоборот:
- •III. Порядок выполнения работы
- •Контрольные вопросы
- •Литература
- •Вопросы для защиты в форме круглого стола
- •Раздел IV. Электромагнетизм
- •Определение горизонтальной составляющей вектора индукции магнитного поля земли
- •I. Описание установки.
- •II. Методика работы.
- •III. Порядок выполнения работы
- •IV. Обработка результатов измерений
- •V. Вывод:
- •Контрольные вопросы
- •Лабораторная работа № 9 (2-15) определение кривой намагничиваия железа
- •I. Описание установки.
- •III. Порядок выполнения работы
- •IV. Обработка результатов измерений
- •Контрольные вопросы
- •Литература
- •Вопросы для защиты в форме круглого стола
- •Раздел V. Волновая оптика
- •Изучение явления интерференции света от двух когерентных источников (опыт Юнга)
- •III. Порядок выполнения работы
- •Контрольные вопросы.
- •Определение длин волн в спектре с помощью дифракционной решетки
- •I. Описание установки.
- •II. Методика работы.
- •III. Порядок выполнения работы
- •IV. Обработка результатов.
- •Контрольные вопросы
- •Изучение закона малюса
- •I. Описание установки.
- •II. Методика работы.
- •III. Порядок выполнения работы.
- •IV. Обработка результатов.
- •Контрольные вопросы
- •II. Методика работы.
- •Порядок выполнения работы
- •IV. Обработка результатов.
- •Контрольные вопросы.
- •Литература
- •Вопросы для защиты в форме круглого стола
- •Раздел VI. Квантовая оптика
- •Определение температуры нити накаливания с помощью яркостного пирометра
- •I. Описание установки.
- •II. Методика работы.
- •III. Порядок выполнения работы
- •IV. Обработка результатов.
- •Дополнительное задание.
- •Контрольные вопросы
- •Лабораторная работа № 14 (3-19) изучение фотоэлемента с внешним фотоэффектом
- •I. Описание установки
- •II. Методика работы
- •III. Порядок выполнения работы
- •Снятие вольтамперной характеристики
- •Снятие световой характеристики
- •Дополнительное задание
- •Контрольные вопросы
- •Ознакомление с работой газового лазера
- •Контрольные вопросы.
- •Литература
- •Вопросы для защиты в форме круглого стола
- •Приложение I. Погрешности прямых и косвенных измерений
- •2.Абсолютная и относительная погрешности
- •3.Доверительные границы. Доверительная вероятность (коэффициент надежности)
- •4.Задача обработки результатов наблюдений
- •5. Систематические и случайные погрешности
- •6. Однократные и многократные измерения а. Однократные измерения
- •Б. Многократные измерения
- •В. Сложение погрешностей
- •7.Обработка результатов прямых многократных наблюдений
- •А. Порядок операций при обработке результатов прямых многократных измерений
- •Б. Пример обработки результатов прямых многократных измерений
- •8. Обработка результатов косвенных измерений
- •А. Метод частных дифференциалов
- •Б. Метод дифференциала логарифма
- •В. Порядок операций при обработке результатов косвенных измерений
- •2. Округление погрешностей
- •3. Правила построения графиков экспериментальных зависимостей
- •Вопросы для защиты в форме круглого стола
Раздел I. Термодинамика. Молекулярно-кинетические явления переноса.
ВВЕДЕНИЕ
Общие положения
Состояние термодинамической (т-д) системы характеризуется макроскопическими физическими величинами, называемыми параметрами (объем, давление, температура, плотность и т.д.). Если параметры системы при взаимодействии её с окружающей средой не изменяются с течением времени, то состояние системы называют стационарным. В стационарном состоянии могут находиться: а) открытые системы – которые обмениваются и энергией, и веществом с окружающими системами;
б) закрытые системы – которые обмениваются только энергией;
в) изолированные системы – которые не обмениваются ни веществом, ни энергией с окружающими системами. Естественно, любая реальная т-д система не будет изолированной хотя бы потому, что её невозможно окружить оболочкой, не проводящей теплоту; изолированную систему можно рассматривать как удобную модель.
Биологические объекты являются открытыми т-д системами, они обмениваются с окружающей средой энергией и веществом.
Для закрытой т-д системы справедлив закон сохранения и превращения энергии, названный первым началом термодинамики: количество теплоты, переданное системе, идет на изменение внутренней энергии системы и на совершение системой работы:
Q=ΔU+A. (I.1)
Еще одной абстракцией является обратимый процесс, в котором после возвращения системы к исходному состоянию в ней и в окружающих телах не произошло никаких изменений. В исследованиях С. Карно (проводимых с целью нахождения условий для повышения к.п.д. тепловых машин) было установлено, что для обратимого процесса сумму приведенных количеств теплоты dQ/T можно представить как разность двух значений некоторой функции состояния системы, которую Р. Клаузиус назвал энтропией S:
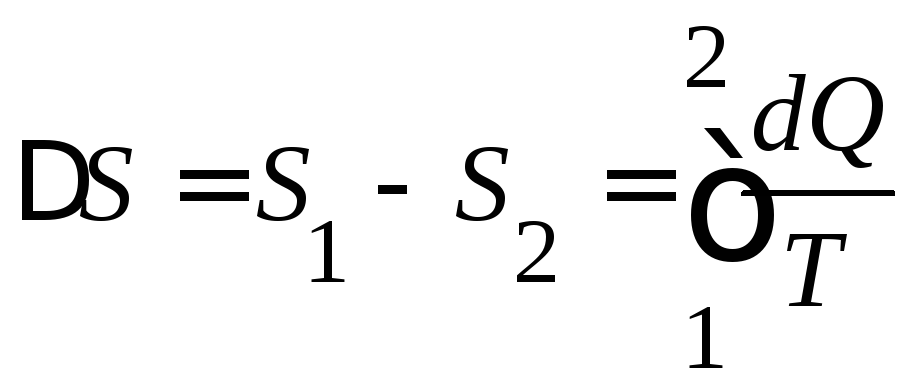 .
(I.2)
.
(I.2)
Если
процесс происходит в изолированной
системе (dQ=0),
то при обратимом процессе энтропия
сохраняется, а при необратимом возрастает
так, что полное изменение энтропии
системы положительно.
Или, второе
начало
т-д – энтропия
изолированной системы не может убывать
при любых происходящих в ней процессах:
![]() .
.
Увеличение энтропии не будет происходить беспредельно, т.к. температуры частей системы со временем выровняются, теплопередача между ними прекратится, и наступит равновесное состояние системы. При этом параметры системы будут неизменными по объему, а энтропия достигнет максимума.
С другой стороны, согласно молекулярно-кинетической теории, энтропию можно охарактеризовать как меру неупорядоченности частиц системы. Например, когда газ конденсируется или жидкость кристаллизуется при постоянной температуре, выделяется теплота (система не изолированная), и энтропия убывает. При этом происходит увеличение порядка в расположении частиц. Неупорядоченность системы численно характеризуется термодинамической вероятностью W – это число способов размещения частиц системы, при котором реализуется данное состояние системы (чем больше упорядоченность, тем меньше способов). Л. Больцман установил, что энтропия пропорциональна натуральному логарифму термодинамической вероятности:
S=k lnW, (I.3)
где k=1,38·10 -23 Дж/К – постоянная Больцмана.
Живой организм – развивающаяся система, однако в небольшом интервале времени её состояние принимают за стационарное, т.е. такое, при котором параметры мало изменяются во времени. И. Пригожин сформулировал принцип минимума производства энтропии: в стационарном состоянии системы скорость возникновения энтропии вследствие необратимых процессов положительна dS/dt>0 и имеет минимальное значение при данных внешних условиях, препятствующих достижению системой равновесного состояния.
Реальные процессы в природе и в технике являются неравновесными (в разных частях системы параметры имеют различные значения), а т-д системы – открытыми. В них происходят необратимые молекулярно-кинетические процессы, приводящие к изменению параметров системы во времени. Это так называемые явления переноса. К ним относятся: теплопроводность, диффузия, внутреннее трение.
Диффузией называется явление самопроизвольного взаимного проникновения и перемешивания частиц между частями объема системы. Это – перенос массы вещества, который вызывается различием концентрации вещества в различных частях объема. Явление диффузии в химически однородном газе подчиняется закону Фика:
![]() ,
(I.4)
,
(I.4)
где
jm–
плотность потока массы, т.е. масса
диффундирующего вещества, переносимая
за единицу времени через единичную
площадку, перпендикулярную оси ОХ, D
– коэффициент диффузии,
![]() – градиент плотности в направлении ОХ.
– градиент плотности в направлении ОХ.
Теплопроводность возникает при наличии разности температур, вызванной какими-либо внешними причинами. При этом молекулы в разных местах объема имеют разные кинетические энергии, и хаотическое тепловое движение молекул приводит к направленному переносу внутренней энергии из нагретых частей объема в более холодные. В простейшем случае одномерного переноса тепловой энергии вдоль оси ОХ в газе теплопроводность подчиняется уравнению Фурье:
![]() ,
(I.5)
,
(I.5)
где
jQ
– плотность теплового потока, которая
есть количество теплоты, переносимое
через единичную площадку, перпендикулярную
ОХ за единицу времени, К
– коэффициент теплопроводности,
![]() – градиент температуры в направлении
ОХ.
– градиент температуры в направлении
ОХ.
Внутреннее трение (вязкость) связано с возникновением сил трения между слоями газа или жидкости, перемещающимися параллельно друг другу с различными по величине скоростями. Со стороны слоя, движущегося быстрее, на более медленный слой действует ускоряющая сила, а медленные слои тормозят более быстрые. Силы трения, которые при этом возникают, направлены по касательной к поверхности соприкосновения слоев. Сила внутреннего трения между двумя слоями, движущимися с разными скоростями, подчинятся закону вязкого трения Ньютона:
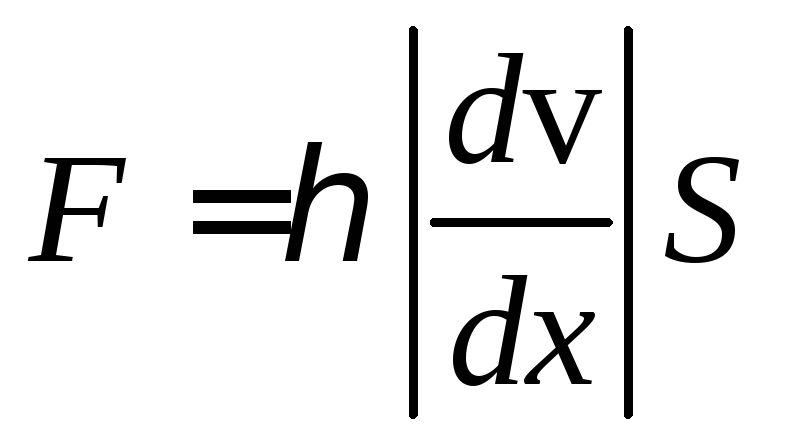 ,
(I.6)
,
(I.6)
где
η-
коэффициент
динамической вязкости (вязкость),
![]() – модуль
градиента
скорости в направлении ОХ, перпендикулярном
направлению движения, S
– площадь
соприкосновения слоев. Взаимодействие
двух слоев, согласно второму закону
Ньютона, можно представить как процесс
передачи
импульса
от одного слоя к другому, который за
единицу времени равен действующей силе:
– модуль
градиента
скорости в направлении ОХ, перпендикулярном
направлению движения, S
– площадь
соприкосновения слоев. Взаимодействие
двух слоев, согласно второму закону
Ньютона, можно представить как процесс
передачи
импульса
от одного слоя к другому, который за
единицу времени равен действующей силе:
![]() ,
(I.7)
,
(I.7)
где jp – плотность потока импульса.
Знак «минус» в уравнениях переноса означает, что процессы направлены навстречу градиентам и, таким образом, являются процессами выравнивания параметров и направлены на приведение системы в состояние равновесия. Таким образом, термодинамические системы вообще и биологические, в частности, обладают способностью к аутостабилизации, т.е. могут самостоятельно возвращаться в исходное состояние при небольших отклонениях от него, вызванных внешним воздействием. Это принцип Ле Шателье-Брауна, который гласит: внешнее воздействие, выводящее систему из состояния равновесия, или из стационарного состояния, вызывает в этой системе процессы, стремящиеся ослабить результат внешнего воздействия.
Жидкости, для которых вязкость зависит только от их природы и температуры, называют ньютоновскими жидкостями; к ним относят воду, водные растворы, некоторые низкомолекулярные органические жидкости (спирты, ацетон). Если коэффициент вязкости зависит от давления и градиента скорости, жидкости называют неньютоновскими; к ним относят высокомолекулярные органические соединения, суспензии, эмульсии. Кровь, будучи суспензией ее форменных элементов в белковом растворе – плазме, является неньютоновской жидкостью. Поэтому законы Ньютона и Бернулли применимы для крови лишь с определенным приближением. Коэффициент вязкости крови изменяется при патологических процессах (например, при анемии вязкость крови снижается, а при полицитемии – повышается).
При течении вязкой жидкости по трубам (крови по сосудам) наблюдается ламинарное, турбулентное или смешанное течение. При ламинарном, плавном, течении отсутствует перемешивание соседних слоев потока. Если скорость потока превышает определенную величину, то согласно закону Бернулли, в разных слоях из-за большого градиента скоростей возникает разность динамических давлений и происходит перемешивание слоев, возникают завихрения, движение становится турбулентным. Скорость, при которой ламинарное течение переходит в турбулентное, называют критической скоростью и определяют её из числа Рейнольдса Re:
 ,
(I.8)
,
(I.8)
где ρ – плотность жидкости, v – её скорость в центре трубы, Dc – диаметр трубы, η – вязкость. Например, для воды, текущей по гладкой цилиндрической трубе, Reкр =2300.
ЛАБОРАТОРНАЯ РАБОТА №1 (1-13)
