
- •Загальна хімія
- •Основні закони й поняття хімії
- •Предмет і завдання хімії
- •Місце хімії серед природничих наук
- •Фізичні та хімічні явища
- •Хімічна символіка. Знаки хімічних елементів та хімічні формули
- •Валентність
- •Визначення валентності за формулами хімічних сполук
- •Складання формул сполук з використанням валентності
- •Основні фізичні величини, які використовують у хімії
- •Основні кількісні закони хімії
- •Чисті речовини й суміші
- •Основні методи розділення сумішей
- •Перші спроби класифікації хімічних елементів
- •Періодичний закон Д. І. Менделєєва
- •Періодична система хімічних елементів
- •Будова атома
- •Склад атома
- •Ізотопи
- •Ядерні перетворення
- •Рух електронів в атомі. Орбіталі
- •Будова електронних оболонок та властивості хімічних елементів
- •Хімічний зв’язок і будова речовини
- •Умови виникнення хімічного зв’язку
- •Ковалентний зв’язок
- •Полярний і неполярний ковалентний зв’язок. Властивості хімічного зв’язку
- •Йонний зв’язок
- •Ступінь окиснення
- •Металічний зв’язок
- •Будова твердих речовин та їхні властивості
- •Хімічні реакції та закономірності їх перебігу
- •Класифікація хімічних реакцій
- •Тепловий ефект хімічної реакції. Термохімічні рівняння
- •Швидкість хімічної реакції
- •Каталіз і каталізатори
- •Хімічна рівновага
- •Розчини
- •Поняття про розчини
- •Розчинність. Кристалогідрати
- •Способи кількісного вираження складу розчинів
- •Електроліти та електролітична дисоціація
- •Сильні та слабкі електроліти
- •Йонні рівняння реакцій
- •Окисники й відновники
- •Електроліз розчинів та розплавів електролітів
- •Основні класи неорганічних сполук
- •Оксиди
- •Класифікація оксидів
- •Добування оксидів
- •Хімічні властивості оксидів
- •Кислоти
- •Хімічні властивості кислот
- •Добування кислот
- •Основи
- •Хімічні властивості основ
- •Добування основ
- •Витискувальний ряд металів
- •Генетичний зв’язок між класами неорганічних сполук
- •Хімія елементів
- •Гідроген. Водень. Вода
- •Гідроген
- •Вода
- •Галогени
- •Характеристика хімічних елементів
- •Прості речовини
- •Деякі сполуки галогенів
- •Оксигеновмісні кислоти хлору
- •Хлороводень і хлоридна кислота
- •Оксиген. Сульфур
- •Характеристика хімічних елементів
- •Прості речовини
- •Гідроген пероксид
- •Сірководень
- •Оксиди сульфуру
- •Сульфатна кислота
- •Сульфати
- •Нітроген. Фосфор
- •Характеристика хімічних елементів
- •Прості речовини
- •Хімічні властивості простих речовин
- •Методи добування простих речовин
- •Застосування простих речовин
- •Амоніак
- •Оксиди нітрогену
- •Нітратна кислота
- •Нітрати
- •Кругообіг Нітрогену в природі
- •Оксиди Фосфору
- •Ортофосфатна кислота
- •Мінеральні добрива
- •Карбон. Силіцій
- •Характеристика хімічних елементів
- •Прості речовини
- •Хімічні властивості простих речовин
- •Методи добування простих речовин
- •Застосування вуглецю та кремнію
- •Оксиди карбону та силіцію
- •Карбонати
- •Силікати
- •Кругообіг карбону в природі
- •Загальна характеристика металів
- •Загальні фізичні властивості металів
- •Загальні хімічні властивості металів
- •Загальні способи добування металів
- •Корозія металів
- •Сплави. Доменне виробництво чавуну
- •Деякі представники металів
- •Загальна характеристика лужних металів
- •Натрій і калій
- •Кальцій
- •Алюміній
- •Ферум
- •Органічна хімія
- •Розмаїття і класифікація органічних речовин
- •Виникнення органічної хімії
- •Поняття про органічні речовини
- •Класифікація органічних сполук
- •Загальна характеристика органічних сполук
- •Порівняльна характеристика органічних і неорганічних сполук
- •Хімічна структура та хімічна будова
- •Брутто, структурні та електронні формули сполук
- •Явище ізомерії
- •Ізомери
- •Класифікація органічних сполук
- •Насичені вуглеводні. Алкани
- •Гомологічний ряд алканів
- •Ізомерія алканів
- •Номенклатура вуглеводнів
- •Будова алканів
- •Фізичні властивості алканів
- •Хімічні властивості алканів
- •Методи добування алканів
- •Алкени
- •Гомологічний ряд алкенів
- •Ізомерія алкенів
- •Номенклатура алкенів
- •Будова алкенів
- •Фізичні властивості алкенів
- •Добування алкенів
- •Хімічні властивості алкенів
- •Поняття про полімери
- •Гомологічний ряд алкінів
- •Ізомерія й номенклатура
- •Будова алкінів
- •Фізичні властивості алкінів
- •Добування алкінів
- •Хімічні властивості алкінів
- •Ароматичні вуглеводні (Арени)
- •Поняття про ароматичні сполуки
- •Будова бензену
- •Гомологічний ряд аренів
- •Номенклатура та ізомерія
- •Фізичні властивості аренів
- •Добування аренів
- •Хімічні властивості аренів
- •Правила орієнтації (заміщення) у бензеновому кільці
- •Природні джерела і застосування вуглеводнів
- •Спирти й феноли
- •Гомологічний ряд спиртів
- •Ізомерія та класифікація спиртів
- •Номенклатура спиртів
- •Фізичні властивості спиртів
- •Методи добування спиртів
- •Хімічні властивості спиртів
- •Застосування спиртів
- •Вплив спиртів на організм людини
- •Поняття про феноли
- •Фізичні властивості фенолу
- •Добування фенолів
- •Хімічні властивості фенолів
- •Застосування фенолу
- •Альдегіди
- •Поняття про альдегіди
- •Гомологічний ряд і номенклатура альдегідів
- •Фізичні властивості альдегідів
- •Хімічні властивості альдегідів
- •Добування альдегідів
- •Застосування альдегідів
- •Карбонові кислоти
- •Поняття про карбонові кислоти
- •Класифікація карбонових кислот
- •Гомологічний ряд і номенклатура карбонових кислот
- •Фізичні властивості карбонових кислот
- •Хімічні властивості карбонових кислот
- •Застосування карбонових кислот
- •Естери, жири та мило
- •Поняття про естери
- •Фізичні властивості та застосування естерів
- •Добування естерів та їхня номенклатура
- •Хімічні властивості естерів
- •Жири
- •Хімічні властивості жирів
- •Мило
- •Вуглеводи
- •Поняття про вуглеводи та їхня класифікація
- •Глюкоза
- •Хімічні властивості глюкози
- •Сахароза
- •Крохмаль і целюлоза
- •Штучні волокна
- •Нітрогеновмісні сполуки
- •Амінокислоти й білки
- •Номенклатура та ізомерія амінокислот
- •Фізичні властивості амінокислот
- •Хімічні властивості амінокислот
- •Добування амінокислот
- •Будова білків
- •Хімічні властивості білків
- •Біологічна роль білків
- •Нуклеїнові кислоти
- •Словник термінів
2. Окиснення метану.
Метод добування формальдегіду з метану складається, в основному, з кількох стадій: 1) шляхом взаємодії метану з водною парою добувають водний газ (суміш водню й карбон(ІІ) оксиду CO); 2) із нього синтезують метиловий спирт; 3) потім спирт окиснюють у мурашиний альдегід:
CH4 + H2O  CO + H2
CO + H2  CH3OH
CH3OH 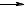 CH2O
CH2O
3. Реакція Кучерова.
Основним способом добування оцтового альдегідуєреакціягідратаціїацетиленузаметодом М.Г. Кучерова в присутності солей Меркурію(II).
У ході реакції гідратації спочатку утворюється вініловий спирт CH2 = CH −OH . Однак така сполука є нестійкою (оскільки гідроксильна група з’єднана з атомом Карбону, що утворює подвійний зв’язок). Унаслідок цього відбувається ізомеризація в оцтовий альдегід:
|
|
−CHO. |
CH ≡ CH +H2O → CH2 = CH −OH → CH3 |
||
4. Окиснення етилену киснем. |
|
|
Добування альдегіду |
окисненням |
етилену |
в присутності хлоридів Паладію (PdCl2 ) та Купруму (CuCl) сьогодні вважають найпрогресивнішим способом:
2CH2 = CH2 +O2 →2CH3 −CHO.
застосування альдегідів
Найбільш поширеними серед альдегідів є формальдегід та ацетальдегід.
Формальдегід
Застосовують у виробництві термореактивних пластмас, феноло-формальдегідних та сечовиноформальдегідних смол.
Формальдегід є біологічно активною речовиною: під його впливом відбувається згортання (денатурація) білка. На цьому ґрунтується його (точніше його водного розчину — формаліну) застосування як засобу для дезінфекції, як дубильного засобу та консерванта для анатомічних препаратів. Формаліном називають 37—40% водний розчин формальдегіду, до якого як інгібітор полімеризації додають 6—15% метанолу. У медицині також використовують похідні формальдегіду — гексаметилентетрамін (уротропін).
ацетальдегід
Найважливіші застосування оцтового альдегіду ґрунтуються на використанні його реакцій окиснення та відновлення. За допомогою першої з них добувають оцтову кислоту, за допомогою другої у деяких країнах — етиловий спирт. Основне застосування оцтового альдегіду — добування оцтової кислоти.
Інші альдегіди в промисловості застосовують не так часто. Деякі альдегіди, які мають приємний запах, використовують у парфумерії та косметиці.
карБОнОві кислОти
поняття про карбонові кислоти
Оскільки органічні кислоти, так само, як і решта органічних сполук, мають у своєму складі вуглеводневий кістяк, то всі органічні кислоти називають карбоновими кислотами. Карбонові кислоти належать до оксигеновмісних органічних сполук і мають у своєму складі функціональну групу, що визначає їхню приналежність до кислот.
|
|
O |
функціональна група |
|
C |
|
OH
У кислот функціональна група поєднує в собі карбонільну та гідроксильну групи — COOH. Цю групу називають карбоксильною групою.
класифікація карбонових кислот
Класифікація за вмістом Оксигену: оскільки до складу функціональної групи кислот входять атоми Оксигену, то всі карбонові кислоти належать до оксигеновмісних кислот.
Класифікація за силою кислот: усі карбонові кислоти є слабкими кислотами. Причому зі збільшенням вуглеводневого радикала сила кислот зменшується. Фактично найсильнішою
карбоновоюкислотоюєтрифтороцтова (CF3COOH),
що є кислотою середньої сили (pKa = 0,23).
Класифікація за основністю кислот: так само,
як неорганічні кислоти, органічні поділяють за основністю. Причому основність кислот визначається кількістю карбоксильних груп. Винятком є найпростіша двохосновна карбонова кислота —
карбонатна. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
Одноосновні кислоти |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||||
|
|
H3C |
|
|
C |
|
|
|
|
H3C |
|
|
CH2 |
C |
OH |
|||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
оцтова |
|
|
|
|
|
|
пропіонова |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||||
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
|
|
CH |
|
|
C |
|
|
|
|
|||||||
|
H2C |
|
|
CH |
|
|
C |
|
|
|
|
|
|
OH |
||||||||||||||||
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
OH |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
акрилова |
|
|
|
|
|
|
|
|
молочна |
||||||||||||||||||||
|
|
O |
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
CH |
|
C |
||||||||
|
|
|
OH |
|
|
|
|
OH |
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
бензойна |
саліцилова |
|
|
|
|
|
|
|
|
корична |
|||||||||||||||||||
189

|
Двохосновні кислоти |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
O |
|
|
|
|
||||||||||
|
|
HO |
|
|
|
|
C |
|
|
|
|
|
|
|
|
C |
|
|
C |
OH |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
HO |
|
|
|
|
|||||||||||||
|
|
|
|
карбонатна |
|
|
|
|
|
щавлева |
|||||||||||||||||||||||||
|
O |
|
|
|
|
|
|
|
|
|
|
O |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||||
|
|
C |
|
|
|
CH2 |
|
C |
|
C |
|
|
|
|
CH2 |
|
|
|
CH2 |
|
C |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
HO |
|
|
|
|
|
|
|
|
|
|
OH |
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|||||||
|
|
малонова |
|
|
бурштинова |
||||||||||||||||||||||||||||||
|
O |
|
|
|
|
|
|
|
|
|
|
|
O |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||||
|
|
C |
|
|
(CH2)4 |
C |
|
|
|
C |
|
|
|
(CH2)6 |
C |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
HO |
|
|
|
|
|
|
|
|
|
|
|
OH |
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|||||
|
|
адипінова |
|
|
|
коркова |
|
|
|||||||||||||||||||||||||||
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
C |
|
|
CH |
|
|
CH |
|
C |
|
C |
|
|
|
|
CH |
|
CH2 |
C |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
OH OH |
|
|
|
OH |
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
винна |
|
|
|
яблучна |
|
|
|||||||||||||||||||||||||||
O
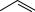
 C
C OH
OH
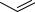
 C
C OH
OH
O
фталева
Трьохосновні кислоти
|
|
O |
C |
OH |
|||||
O |
|
|
|
|
O |
||||
|
|
|
|||||||
C |
|
CH2 |
|
C |
|
CH2 |
C |
||
|
|
|
|||||||
HO |
|
|
|
|
OH |
||||
OH |
|||||||||
|
|
|
|
|
|
||||
лимонна
Класифікація за вуглеводневим радикалом: карбонові кислоти можна класифікувати за вуглеводневим радикалом — насичені, ненасичені (акрилова) та ароматичні (бензойна, фталева, корична, саліцилова).
Назва карбонових кислот та їхніх солей
Формула |
|
|
назва IUPAC |
|
тривіальна назва |
назва солей |
|||
|
|
|
|
|
|
|
|
|
|
HCOOH |
|
|
Метанова |
Мурашина |
|
Форміат (метаноат) |
|||
|
|
|
|
|
|
|
|
|
|
CH3COOH |
|
|
Етанова |
Оцтова |
|
Ацетат (етаноат) |
|||
|
|
|
|
|
|
|
|
|
|
CH3CH2COOH |
|
|
Пропанова |
Пропіонова |
|
Пропіонат (пропаноат) |
|||
|
|
|
|
|
|
|
|
|
|
CH3 (CH2 )2 COOH |
|
|
Бутанова |
Масляна |
|
Бутират (бутаноат) |
|||
|
|
|
|
|
|
|
|
||
CH3 (CH2 )3 COOH |
|
|
Пентанова |
Валеріанова |
|
Валерат (пентаноат) |
|||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
CH3 (CH2 )4 COOH |
|
|
Гексанова |
Капронова |
|
Капронат (гексаноат) |
|||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
CH3 (CH2 )14 COOH |
|
|
Гексадеканова |
Пальмітинова |
|
Пальмітат |
|||
|
|
|
|
|
|
|
|
||
CH3 (CH2 )16 COOH |
|
|
Октадеканова |
Стеаринова |
|
Стеарат |
|||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
||
CH3 (CH2 ) −CH = CH −(CH2 ) COOH |
Октадеценова |
Олеїнова |
|
Олеат |
|||||
7 |
|
7 |
|
|
|
|
|
|
|
|
|
Фізичні властивості карбонових кислот |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
Формула |
|
назва |
|
Тпл, °с |
|
Ткип, °с |
|
розчинність у воді |
|
|
|
|
|
|
|
|
|
||
HCOOH |
|
Мурашина |
|
8,2 |
|
100,7 |
Необмежено розчиняється |
||
|
|
|
|
|
|
|
|
||
CH3COOH |
|
Оцтова |
|
16,6 |
|
117,7 |
Необмежено розчиняється |
||
C2H5COOH |
|
Пропіонова |
|
–20,8 |
|
140,8 |
Необмежено розчиняється |
||
C3H7COOH |
|
Масляна |
|
–5,3 |
|
163,3 |
Добре розчиняється |
||
C4H9COOH |
|
Валеріанова |
|
–34,5 |
|
186,4 |
Погано розчиняється |
||
C5H11COOH |
|
Капронова |
|
–3,9 |
|
205,3 |
Погано розчиняється (1%) |
||
C15H31COOH |
|
Пальмітинова |
|
52,5 |
|
390 |
Не розчиняється |
||
C17H35COOH |
|
Стеаринова |
|
71,0 |
|
432 |
Не розчиняється |
||
190
гомологічний ряд і номенклатура карбонових кислот
Правила складання назв карбонових кислот за міжнародною номенклатурою аналогічні до правил для спиртів, альдегідів та вуглеводнів. Назва кислоти походить від назви відповідного вуглеводню додаванням суфікса -ова до назви алкану. У зв’язку з тим, що багато карбонових кислот були відкриті задовго до прийняття правил міжнародної номенклатури, більшість із них мають тривіальні назви, які ми наводимо в таблиці.
Загальна формула гомологічного ряду одноосновних насичених карбонових кислот: (CnH2n + 1COOH або CnH2nO2).
Фізичні властивості карбонових кислот
На відміну від альдегідів, уже перший член ряду — мурашина кислота — рідина з досить високою температурою кипіння, початкові члени ряду мають різкий запах, пропіонова має запах поту, запах масляної кислоти відчувається при підгоранні їжі на сковороді, запах інших рідких кислот так само неприємний. Карбонові кислоти із числом атомів Карбону більшим від 10 є твердими речовинами.
Оскільки в молекулах кислот одночасно присутні і негативно, і позитивно заряджені атоми, то можуть утворитися подвійні молекули — димери з двома водневими зв’язками:
|
|
|
O ... H |
|
O |
||
|
|
|
|
||||
H |
C |
|
C |
|
C |
|
CH3 |
|
|
||||||
|
|||||||
3 |
|
|
|
|
|
|
|
OH ... O
Природно, що в такому разі асоціація молекул виявляється більш міцною, ніж при наявності одного водневого зв’язку. У зв’язку із цим температури кипіння й плавлення кислот більші, ніж у відповідних їм спиртів чи альдегідів.
хімічні властивості карбонових кислот
1.Вплив кислот на індикатори за рахунок дисо ціації на йони:
CH3COOH CH3COO− +H+. 2. Взаємодія з металами:
Zn +2CH3COOH →Zn(CH3COO)2 +H2. 3. Взаємодія з оксидами металів:
MgO +2CH3COOH → Mg(CH3COO)2 +H2O. 4. Взаємодія з лугами:
CH3COOH +NaOH → CH3COONa +H2O.
5. Горіння:
Як і більшість органічних сполук, карбонові кислоти дуже добре горять, причому чим більшим є вуглеводневий радикал, тим більша ймовірність протікання реакції горіння з виділенням сажі (вільного вуглецю):
CH3COOH +2O2 →2CO2 +H2O ,
C17H35COOH +8O2 →17C +18H2O.
6.Реакція естерифікації.
Карбонові кислоти здатні взаємодіяти зі спир-
тами з утворенням естерів:
|
|
|
|
O |
|
|
|
|||
H3C |
|
C |
|
|
|
|||||
|
|
|
|
|||||||
|
|
|
|
OH + H |
|
O |
|
CH2 |
CH3 |
|
|
|
|
|
|
||||||
|
|
|
|
|
O |
|
|
|
||
|
|
H C |
|
C |
|
+ H2O |
||||
|
|
|
|
|||||||
3 |
|
|
|
|
|
|
|
|||
OCH2 CH3
Реакція естерифікації відбувається в присутності сульфатної кислоти, яка в цьому разі відіграє роль каталізатора та водовідіймальної речовини. Роль водовідіймальної речовини в цьому разі полягає в полегшенні протікання реакції та зміщенні рівноваги в бік утворення продуктів реакції.
7. Взаємодія з хлором.
Під впливом карбоксильної групи в молекулі карбонової кислоти збільшується рухливість атомів Гідрогену, які стоять при атомі Карбону у вуглеводневому радикалі, що є сусідом карбоксильної групи (в α-положенні). Саме тому ці атоми Гідрогену можуть легко заміщатися (наприклад, галогенами):
|
|
H |
O |
|
|
|
H |
O |
||||
|
|
|
|
|
|
|
|
|
|
|
||
H |
|
C |
|
C + Cl2 |
|
H |
|
C |
|
C + HCl |
||
|
|
|
|
|
||||||||
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
OH |
||
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
H |
|
|
|
Cl |
||||||
|
|
|
|
|
|
|
||||||
застосування карбонових кислот
1.з астосування мурашиної кислоти.
Оскільки при нагріванні мурашиної кислоти
зоцтовою виділяється чадний газ, то її часто використовують у лабораторії для добування чистого чадного газу.
Мурашину кислоту широко використовують в органічному синтезі, як протраву при фарбуванні текстилю, у бджільництві проти вароатозу, для добування пестицидів тощо. У медицині мурашину кислоту застосовують у вигляді 1% спиртового розчину (мурашиний спирт) як розтирку при невралгіях, міозитах та інших захворюваннях.
2.з астосування оцтової кислоти.
Оцтова кислота належить до найбільш використовуваних з органічних кислот. У цьому сенсі її можна порівняти із сульфатною кислотою.
191
